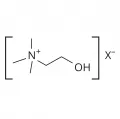
Холин
Холи́н (от греч. χολή – жёлчь), гидроксид 2-гидроксиэтил(триметил)аммония, четвертичное аммониевое основание. Входит в состав фосфатидилхолинов и сфингомиелинов; из него также образуется нейромедиатор ацетилхолин. Донор метильных групп в биохимических реакциях метилирования (например, при биосинтезе метионина). Холин синтезируется бактериями, растениями и животными, однако у последних (в том числе и у человека) в недостаточном количестве, необходимо дополнительное его поступление с пищей. Ранее холин относили к витаминам, однако сегодня считают его лишь витаминоподобным веществом.
История открытия и исследования
Впервые был выделен в 1849 г. из свиной желчи немецким биохимиком А. Штреккером, но название своё получил только в 1862 г., когда учёный выделил его повторно, определил элементный состав и назвал «холин».
В период с 1850 по 1867 г. о выделении холина сообщали и другие исследователи, но называли полученное ими вещество иначе: синкалин, нейрин (позднее так же стали называть производное холина – гидроксид триметилвиниламмония). А в 1867 г. немецкий химик А. Байер определил структуру холина и доказал, что все эти новые соединения являются одним и тем же веществом.
В начале 1930-х гг. канадский исследователь Ч. Г. Бест обнаружил, что холин, входящий в состав лецитина (жироподобного органического вещества, выделенного в 1850 г. французским химиком Т. Н. Гобле из тканей мозга и икры карпов), обладает гепатопротекторным эффектом, так как предотвращает ожирение печени у подопытных животных, находящихся на специальной диете. А в 1998 г. Национальная медицинская академия (США) опубликовала нормы суточного потребления холина как жизненно важного питательного вещества и рекомендации по его содержанию в рационе человека.
Химия холина
Холин представляет собой белое кристаллическое гигроскопичное вещество (молярная масса 121,18 г/моль, температура плавления с разложением 180 °С), обладающее выраженными щелочными свойствами и характерным «аминным» запахом (запах триметиламина, напоминающий зловоние гниющего мяса или рыбы).
В лабораторных условиях холин можно получить путем метилирования 2-аминоэтанола метилиодидом (CH₃I) или в результате конденсации триметиламина с этиленоксидом или этиленхлоргидрином.
Дегидратация холина приводит к образованию токсичного нейрина (гидроксид триметилвиниламмония), присутствие которого в тканях говорит об их разрушении, некрозе. Холин хорошо растворяется в воде (раствор остаётся стабильным до 70 °С) и этиловом спирте, хуже – в ацетоне, хлороформе и амиловом спирте, нерастворим в бензоле, сероуглероде, диэтиловом эфире и др.
Свободный холин – сильное основание (pKb=5,06) и химически нестабилен, в водных растворах он быстро разлагается, образуя токсичные этиленгликоли, триметиламин и т. п. Поэтому в живых организмах уровень свободного холина (в виде холин-О-сульфата) в тканях и биологических жидкостях очень низкий, в основном он находится в ковалентно связанной, неионизированной форме. Он входит в состав фосфолипидов, липопротеинов очень низкой плотности (ЛПОНП), цитозин-дифосфат-холина (ЦДФ-холина) и др. Это позволяет также запасать его на случай дефицита эндогенного холина.
Метаболизм холина
У растений холин синтезируется из серина в ходе следующих реакций:
Декарбоксилирование серина при помощи фермента сериндекарбоксилазы до этаноламина.
Метилирование при помощи фермента метилтрансферазы три раза подряд с образованием свободного холина, который потом включается в состав фосфолипидов. Метильную группу предоставляет S-аденозил-L-метионин, превращаясь при этом в S-аденозил-L-гомоцистеин.
Аналогичным образом холин синтезируют бактерии, в том числе и кишечные. Причём себя они обеспечивают холином полностью, а излишки вырабатываемого ими холина попадают в просвет кишечника и усваиваются организмом хозяина.
У людей и животных синтез эндогенного холина проходит в основном в гепатоцитах по пути фосфатидилэтаноламин-N-метилтрансферазы (ФЭМТ-путь), в ходе которого из 3-фосфоглицерата образуются такие промежуточные соединения, как фосфатидная кислота, фосфатидилсерин и фосфатидилэтаноламин, который с помощью ФЭМТ проходит через три этапа метилирования, образуя в итоге фосфатидилхолин.
Наиболее высоко содержание холина в нервной ткани, в печени, почках и в миокарде. Холин-содержащие биомолекулы (фосфолипиды, глицерофосфохолины и др.) транспортируются кровью в составе липопротеинов. Свободный холин в силу своей водорастворимости и высокой полярности не может проникнуть сквозь двуслойную фосфолипидную мембрану клеток и их органелл и нуждается в трансмембранных ионных белках-транспортёрах. Таковыми являются белок SLC5A7, участвующий в синтезе ацетилхолина в центральной нервной системе, специализированные белки семейства CTL (choline transporters) и белки семейства OCT (organic cation transporters).
Биология холина
Холин является предшественником фосфолипидов – сфингомиелинов и фосфатидилхолинов, которые являются необходимым структурным компонентом клеточных мембран, а кроме того, формируют липидные рафты – участки клеточной мембраны, с помощью которых происходит координация клеточных процессов, сборка сигнальных молекул, регуляция работы рецепторов и мембранных белков, передачи нервных импульсов. На фосфатидилхолины приходится 70–95 % фосфолипидов ЛПОНП. Фосфатидилхолины также задействованы в производстве лёгочного сурфактанта и входят в состав желчи, обеспечивая всасывание липидов в кишечнике.
Из холина образуется нейромедиатор ацетилхолин, участвующий в реализации таких функций, как нервно-мышечная передача и возбуждение большой группы нейронов, имеющих холинэргические синапсы. В частности, данные нейроны необходимы для формирования воспоминаний и протекания ряда других психических процессов. Генетические дефекты белка-транспортёра SLC5A7 у человека связаны с врождённым нарушением производства ацетилхолина и патологической слабостью мышц, в том числе и дыхательных, что приводит к ранней смерти.
У животных и человека из холина в ходе ряда реакций синтезируется триметилглицин, необходимый для осморегуляции и являющийся субстратом для фермента бетаин-гомоцистеин-S-метилтрансферазы, который запускает реакцию метилирования гомоцистеина до метионина – предшественника S-аденозилметионина, играющего важную роль в реакциях метилирования и, соответственно, в регуляции экспрессии генов (эпигенетической регуляции).
Холин в питании и медицине
Биосинтез холина у животных ограничен, поэтому он должен поступать с пищей. Наиболее богаты холином мясо, рыба, яичный желток, соевая мука, а также грудное молоко. Нехватка холина, обладающего выраженным липотропным действием, в сочетании с белковой недостаточностью может вызывать жировую дегенерацию печени и способствовать развитию цирроза. Суточная потребность человека в холине не менее 250 мг.
Дефицит холина, связанный с питанием, встречается крайне редко, чаще причины кроются в заболеваниях, приводящих к нехватке холина и, соответственно, триметилглицина. Избыточное потребление экзогенного холина приводит к снижению артериального давления, диарее, а также к появлению характерного «рыбного» запаха, который говорит о триметиламинурии.
Хлорид холина используется в медицине для лечения заболеваний печени и атеросклероза. Альфосцерат холина является холиномиметиком, который назначается при неврологических заболеваниях, связанных с нарушением мозгового кровообращения, снижением памяти и т. п. Теофиллинат холина назначают при заболеваниях лёгких. Салицилат холина является анальгетиком и анапиретиком.