Metisilin
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
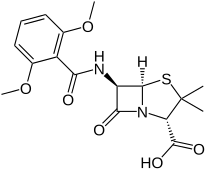
| (2S,5R,6R)-6-(2,6-dimetoksibenzamido)-3,3-dimetil-7-okso-4-tia-1-azabisiklo[3.2.0]heptana-2-asam karboksilat | |
| Data klinis | |
| Kat. kehamilan | ? |
| Status hukum | ? |
| Rute | IV |
| Data farmakokinetik | |
| Bioavailabilitas | Tidak diserap secara oral |
| Metabolisme | Hati, 20–40% |
| Waktu paruh | 25–60 menit |
| Ekskresi | Ginjal |
| Pengenal | |
| Nomor CAS | 61-32-5 |
| Kode ATC | J01CF03 QJ51CF03 |
| PubChem | CID 6087 |
| DrugBank | DB01603 |
| ChemSpider | 5862 |
| UNII | Q91FH1328A |
| ChEMBL | CHEMBL575 |
| Data kimia | |
| Rumus | C17H20N2O6S |
| SMILES | eMolecules & PubChem |
Metisilin adalah antibiotik spektrum sempit dari kelas penisilin. Metisilin ditemukan pada tahun 1960.[1]
Sejarah
[sunting | sunting sumber]Metisilin dikembangkan oleh Beecham pada tahun 1959.[2] Sebelumnya digunakan untuk mengobati infeksi yang disebabkan oleh bakteri gram-positif yang rentan, khususnya penghasil penisilinase seperti Staphylococcus aureus yang mungkin resisten terhadap sebagian besar penisilin.
Perannya dalam terapi sebagian besar telah digantikan oleh oksasilin (digunakan untuk uji kerentanan antimikroba klinis), flukloksasilin, dan dikloksasilin, namun istilah Staphylococcus aureus yang resisten terhadap metisilin (MRSA) terus digunakan untuk menggambarkan strain S. aureus yang resisten terhadap semua penisilin.[3]
Kegunaan dalam medis
[sunting | sunting sumber]Dibandingkan dengan penisilin lain yang menghadapi resistansi antimikroba karena
Spektrum aktivitas
[sunting | sunting sumber]Pada suatu waktu, metisilin digunakan untuk mengobati infeksi yang disebabkan oleh bakteri gram-positif tertentu termasuk Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus pyogenes, dan Streptococcus pneumoniae. Metisilin hanya efektif melawan 50% Staphylococcus aureus saja.
Resistensi terhadap metisilin terjadi melalui aktivasi gen mecA protein pengikat penisilin bakteri (PBP) yang baru. Ini mengkodekan protein PBP2a. PBP2a bekerja dengan cara yang mirip dengan PBP lainnya, namun PBP2a mengikat
Data kerentanan ini diberikan pada beberapa bakteri yang penting secara medis:
- Staphylococcus aureus: 0,125 – >100 g/ml
- Staphylococcus aureus yang resisten terhadap metisilin: 15,6 – >1000
μ g/ml - Streptococcus pneumoniae: 0,39
μ g/ml[4]
Mekanisme kerja
[sunting | sunting sumber]Seperti antibiotik beta-laktam lainnya, metisilin bekerja dengan menghambat sintesis dinding sel bakteri. Ini menghambat hubungan silang antara rantai polimer peptidoglikan linier yang membentuk komponen utama dinding sel bakteri gram positif. Hal ini dilakukan dengan mengikat dan menghambat secara kompetitif enzim transpeptidase (juga dikenal sebagai protein pengikat penisilin (PBP)). Glikopeptida pengikat silang PBP ini (D-alanil-alanin), membentuk dinding sel peptidoglikan. Metisilin dan antibiotik
Metisilin sebenarnya adalah antibiotik
Kimia medisinal
[sunting | sunting sumber]Metisilin resisten terhadap beta-laktamase, yaitu enzim yang disekresi oleh banyak bakteri yang resisten terhadap antibiotik beta-laktam. Kehadiran gugus orto-dimetoksifenil yang melekat langsung pada gugus karbonil rantai samping inti penisilin memfasilitasi resistensi
Referensi
[sunting | sunting sumber]- ^ Walker SR (2012). Trends and Changes in Drug Research and Development. Springer Science & Business Media. hlm. 109. ISBN 9789400926592.
- ^ Dutfield, Graham (30 July 2009). Intellectual property rights and the life science industries: past, present and future. World Scientific. hlm. 140–. ISBN 978-981-283-227-6. Diakses tanggal 18 November 2010.
- ^ Newsom SW (November 2004). "MRSA--past, present, future". Journal of the Royal Society of Medicine. 97 (11): 509–10. doi:10.1177/014107680409701101. PMC 1079642
 . PMID 15520143.
. PMID 15520143.
- ^ "Methicillin Sodium Susceptibility and Concentration (MIC) Data" (PDF). TOKU-E.
- ^ Gladwin M, Trattler B (2004). Clinical Microbiology made ridiculously simple (edisi ke-3rd). Miami: MedMaster, Inc.
