Anidride solforica
| Anidride solforica | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| triossido di zolfo | |
| Nomi alternativi | |
| anidride solforica | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SO3 |
| Massa molecolare (u) | 80,06 |
| Aspetto | solido cristallino incolore (forma |
| Numero CAS | |
| Numero EINECS | 231-197-3 |
| PubChem | 24682 |
| SMILES | O=S(=O)=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,97 (forma |
| Solubilità in acqua | reagisce |
| Temperatura di fusione | 62,2 °C (335,35 K) (forma |
| Temperatura di ebollizione | decompone a 50 °C (323,15 K) (forma |
| Tensione di vapore (Pa) a 293,15 K | 37333 (forma |
| Proprietà termochimiche | |
| −397,77 | |
| S0m(J·K−1mol−1) | 256,77 |
| C0p,m(J·K−1mol−1) | 24,02 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
   
| |
| pericolo | |
| Frasi H | 271 - 314 - 330 - 350 |
| Consigli P | 201 - 220 - 260 - 280 - 284 - 305+351+338 [1] |
Il triossido di zolfo o anidride solforica è un composto chimico corrosivo che reagendo con acqua produce acido solforico, essendo la sua anidride. Esiste in tre forme: le forme
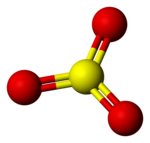
Dal punto di vista strutturale si tratta di una molecola trigonale planare (stato gassoso) ipervalente. Il doppio legame S=O misura 142 pm.
Forme strutturali
[modifica | modifica wikitesto]
La molecola
Il riscaldamento dell'anidride solforica
L'anidride solforica è fortemente igroscopica e il calore di idratazione sviluppato è in grado di infiammare materiali quali il legno e il cotone.[2]
Proprietà chimiche
[modifica | modifica wikitesto]La reazione di formazione di una mole di anidride solforica (P = 1 atm, T = 298,15 K) a partire dagli elementi nei rispettivi stati standard è:
che condotta in una bomba calorimetrica (a volume costante), sviluppa 397 kJ per ogni mole di SO3 che si forma.
L'anidride solforica reagisce con l'acqua producendo acido solforico:
con sviluppo di 87,895 kJ/mol. Alla temperatura di circa 340 °C si instaura un equilibrio in cui tutte e tre le specie sono presenti in concentrazioni significative.
Il triossido di zolfo reagisce col dicloruro di zolfo producendo l'importante reagente cloruro di tionile:
L'equilibrio di dissociazione gassosa
assume un ruolo di un certo rilievo termodinamico a temperature superiori a 779 °C.
Reagisce con i solfiti per dare tiosolfati.
Sintesi e usi
[modifica | modifica wikitesto]A livello di laboratorio è possibile ottenere l'anidride solforica effettuando la pirolisi del bisolfato di sodio, processo che consta in due stadi in cui l'intermedio di reazione è il pirosolfato di sodio:
- a T = 315 °C:
- a T = 460 °C:
La sintesi industriale prevede invece l'ossidazione dell'anidride solforosa prodotta normalmente dalla combustione della pirite o dello zolfo, con ossigeno atmosferico a temperature comprese tra i 400-600 °C e in presenza dei catalizzatori pentossido di vanadio (V2O5) o platino.
Gli usi principali riguardano la sintesi dell'acido solforico e dell'oleum; nel primo caso il gas viene assorbito in torri contenenti una soluzione concentrata di acido solforico al 98-98,3% se si vuole ottenere acido solforico al 100% mentre nel secondo caso si è soliti utilizzare acido solforico puro. Il triossido di zolfo viene anche utilizzato come agente solfonante in particolare nell'industria dei coloranti.
In alternativa, è possibile sintetizzare l'anidride solforica in laboratorio attraverso il riscaldamento di una miscela di anidride fosforica e acido solforico, secondo il seguente equilibrio:
Il risultato sarà anidride solforica gassosa, che per l'utilizzo deve essere quindi condensata, e acido fosforico.
Precauzioni e rischi
[modifica | modifica wikitesto]L'anidride solforica è un composto chimico molto pericoloso a causa della sua reattività.
Essa infatti fuma fortemente all'aria ed esercita un'energica azione disidratante su molte sostanze organiche, carbonizzandole. Se inalata, può reagire con l'acqua delle mucose nasali e della saliva trasformandola in acido solforico (H2SO4).
Può inoltre provocare il cancro (H350).
Note
[modifica | modifica wikitesto]Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file sull'anidride solforica
Wikimedia Commons contiene immagini o altri file sull'anidride solforica
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) sulfur trioxide, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Preparazione dell'anidride solforica, su itchiavari.org.
| Controllo di autorità | Thesaurus BNCF 31222 · LCCN (EN) sh96009016 · GND (DE) 4180436-3 · J9U (EN, HE) 987007563777005171 |
|---|






