Osoon
|
Algemeen | |
|---|---|
| Naam | Osoon |
| IUSTC-naam | trisuurstof |
 |
 |
| Chemiese formule | O3 |
| Molêre massa | 48.0 [g/mol] |
| CAS-nommer | 10028-15-6[1] |
| Voorkoms | ligteblou gas |
| Reuk | skerp |
| Fasegedrag | |
| Smeltpunt | -193 °C[1] |
| Kookpunt | -112 °C[1] |
| Digtheid | 1,6*lug[1] |
| Oplosbaarheid | 570 mg/L water 20 °C suiwere osoon[1] |
| Termodinamies | |
| 142.7 [kJ/mol][2] | |
| Henry se konstante | 1.17 x 10-2[mol/L.atm] - 2400[K][3] |
|
Suur-basis eienskappe | |
| pKa | |
|
Veiligheid | |
| Flitspunt | N/A |
| LD50 | 12,6 dpm, 3 uur (muis)[1] |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
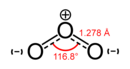
Osoon (O3) is 'n reaktiewe allotroop van suurstof. 'n Osoonmolekuul is 'n polêre molekuul wat uit drie kovalentgebonde suurstofatome bestaan. Dit is 'n irriterende, giftige gas met 'n ligteblou kleur teen standaardtemperatuur en -druk. Dit word 'n donkerblou vloeistof onder -112 °C en 'n donkerblou vastestof onder -193 °C.
Atmosfeer
[wysig | wysig bron]Osoon kom in die osoonlaag in die boonste gedeelte van die stratosfeer van die aarde voor, wat laasgenoemde se natuurlike beskerming teen die son se ultravioletstraling (hoë energiestraling) is. Osoon in die stratosfeer is dus "goeie osoon" wat die son se ultravioletstraling absorbeer en sodoende die mense, diere en plante teen die hoë energiestraling beskerm. Die vorming van ozone in die stratosfeer is 'n fotochemiese proses. Suurstof neem energie op deur absorpsie van 'n foton en dissosieer:
'n Suurstofatoom reageer met 'n suurstof molekuul, maar hierdie reaksie vereis dat 'n derde molekuul M die oorskot aan energie kan wegdra [2]
Die ultraviolette straling van die son en suurstofatome kan osoon ook weer vernietig:

'n Ewewigskonsentrasie van osoon sal so vorm, veral omdat die vernietiging nie baie vinnig verloop nie. Tydens die winter sal egter aan die pole die osoonkonsentrasie terugloop omdat daar lang tyd geen sonlig meer is nie, maar die terugloop is nie baie vinnig nie
Die aanwesigheid van freon uit spuitbusse en koelkaste in die atmosfeer het dit egter verander omdat chlooratome wat ontstaan deur fotodissosiasie van freon as 'n katalisator vir die afbraakproses optree. Dit veroorsaak die osoongat bo die pole.
Een stap is byvoorbeeld:
Bo die pole is die temperatuur soms baie laag (190K) en die yskristalle in die atmosfeer versterk die katalitiese effekte.
Daar word ook osoon in die troposfeer aangetref. Maar anders is die osoon in die osoonlaag, is hierdie "slegte osoon" wat skadelik is vir asemhalende wesens. Die het 'n irriterende effek op die mens se neus, keel en oë, en beskadig longweefsel en plante.
Verwysings
[wysig | wysig bron]- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 "Ozone Solutions Inc. Safety Data Sheet" (PDF) (in Engels). Geargiveer vanaf die oorspronklike (PDF) op 11 Julie 2019. Besoek op 20 Januarie 2016.
- ↑ 2,0 2,1 "U. Waterloo (Cdn)" (in Engels). Geargiveer vanaf die oorspronklike op 10 November 2018. Besoek op 21 Januarie 2016.
- ↑ Sander.






