CSNK1E
Izoforma epsilon kazein-kinaze I ili CK1
Aminokiselinska sekvenca
[uredi | uredi izvor]Dužina polipeptidnog lanca je aminokiselina, a molekulska težina Da.
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MELRVGNKYR | LGRKIGSGSF | GDIYLGANIA | SGEEVAIKLE | CVKTKHPQLH | ||||
| IESKFYKMMQ | GGVGIPSIKW | CGAEGDYNVM | VMELLGPSLE | DLFNFCSRKF | ||||
| SLKTVLLLAD | QMISRIEYIH | SKNFIHRDVK | PDNFLMGLGK | KGNLVYIIDF | ||||
| GLAKKYRDAR | THQHIPYREN | KNLTGTARYA | SINTHLGIEQ | SRRDDLESLG | ||||
| YVLMYFNLGS | LPWQGLKAAT | KRQKYERISE | KKMSTPIEVL | CKGYPSEFST | ||||
| YLNFCRSLRF | DDKPDYSYLR | QLFRNLFHRQ | GFSYDYVFDW | NMLKFGAARN | ||||
| PEDVDRERRE | HEREERMGQL | RGSATRALPP | GPPTGATANR | LRSAAEPVAS | ||||
| TPASRIQPAG | NTSPRAISRV | DRERKVSMRL | HRGAPANVSS | SDLTGRQEVS | ||||
| RIPASQTSVP | FDHLGK |
Snimanje strukture
[uredi | uredi izvor]Snimanje strukture CK1
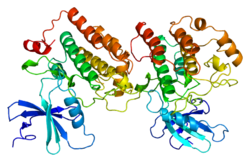
Struktura
[uredi | uredi izvor]Trodimenzijske strukture katalitskih domena CK1
CK1
Funkcija
[uredi | uredi izvor]Enzimska funkcija
[uredi | uredi izvor]Protein kodiran epsilon genom kazein-kinaze 1 je serin/treonin protein kinaza i član porodice proteina kazein-kinaza I, čiji su članovi uključeni u kontrolu citoplazmatskih i jedarnih procesa, uključujući replikaciju i popravak DNK. Kao i drugi članovi porodice proteinkih kazein-kinaza 1, kazein-kinaza 1 epsilon prepoznaje Ser (p)XXSer/Thr motiv za fosforilacije.[10] Nalazi se u citoplazmi kao monomer i može fosforilirati razne proteine, uključujući i samog sebe. Ova autofosforilacija događa se u proteinskim C-terminalnom domenu, regiji za koju se vjeruje da se ponaša kao pseudosubstrat i inhibira aktivnost kinaze.[7][11][12]
Cirkadijski sat
[uredi | uredi izvor]Protein kazein kinaze 1 epsilon je dio sisarskog oscilatora, grupe proteina koji održavaju ćelije na otprilike 24-satnom rasporedu.[13] Ovaj oscilator, ili "cirkadijski sat", sastoji se od petlja povratne informacije o transkripciji–translaciji (TTFL) u kojoj nekoliko proteina djeluje u tandemu, od kojih svaki reguliše ekspresiju drugih kako bi se stvorio otprilike 24-satni ciklus nivoa iRNK i proteina.[14] TTFL takođe generira otprilike 24-satne ritmove izlaza kao što su nivoi oslobađanja ćelijskih hormona.[15] Dnevne oscilacije transkripcija proteina i iRNK uočene su u mnogim ćelijama, uključujući glavni sat sisara poznat kao suprahijazmatsko jezgro (SCN).[16] Međutim, za razliku od većine proteina cirkadijskog ritma koji osciliraju u svojoj ekspresiji, kazein-kinaza 1 epsilon je konstitutivno aktivna.[15]
Osnovni proteini koji čine TTFL sisara uključuju Period (PER), kriptohrom (CRY), BMAL1, CLOCK i kazein-kinazu 1 epsilon.[17] BMAL1 i CLOCK rade na povećanju transkripcije PER i CRY, formiranjem heterodimera i vezivanjem na domene E-kutija uzvodno od sekvenci kodiranja gena PER i CRY.[17] Nivoi PER i CRY regulisani su negativnom povratnom spregom, što znači da potiskuju sopstvenu transkripciju.[17] Fosforilacija PER proteina pomoću CK1
Kao što je prethodno pomenuto, C-terminalni domen kazein-kinaze 1 epsilon ponaša se kao pseudosubstrat kada je fosforiliran, inhibirajući aktivnost kinaze.[7][11] Domen C-terminala je također pokazao da je defosforiliran pomoću fosfataze kao što je protein-fosfataza 1 (PP1) in vitro i u kulturi ćelija, koja regulira nivoe aktivne kazein-kinaze in vivo.[7][14][23] Važeća teorija cirkadijskih ritmova pretpostavlja da je ovaj ciklus fosforilacije/defosforilacije kazein-kinaze 1 epsilon važan u modulaciji perioda cirkadijskih ritmova u ćeliji, uz povećanu fosforilaciju koja smanjuje aktivnost kazein-kinaze 1 i uz naknadno povećanje aktivnog CRY i PER) i defosforilacija kazein-kinaze 1 epsilon, što rezultira aktivnijom kinazom (i nižim nivoima aktivnog CRY i PER).[14]
Kod miševa se pokazalo da kazein-kinaza 1 epsilon fosforilira i PER1 i PER2, kao i CRY1 i CRY2.[15] Kazein-kinaza 1 rezultira cikličkom ekspresijom proteina oscilatora sisara, što omogućava mjerače vremena (sisarske oscilatore) za ćeliju:[24]
| Nivo proteina | Međurezultat | Odgođeni rezultat | |
|---|---|---|---|
| Zora (7 sati ujutro) | Niska koncentracija proteina PER i CRY [25] | Per i Cry (gen) aktivno transkribovani i stimulirani transkripcijski faktori BMAL1 i CLOCK | N/A |
| Sumrak (19 sati) | Visoka koncentracija proteina PER i CRY[25] | Visoki nivoi proteina PER i CRY potiskuju transkripciju Per i Cry (gena) | Kazein-kinaza 1 epsilon fosforilira PER i CRY, označavajući protein za razgradnju: koncentracija PER i CRY proteina se smanjuje. |
Interakcije
[uredi | uredi izvor]Pokazalo se da kazein-kinaza 1 epsilon reaguje sa PER1,[20] PER2, CRY1, CRY2, BMAL1, CLOCK, NPAS2 i AXIN1.[7][26] PER1, PER2 i BMAL1 mogu biti direktno fosforilirani pomoću CK1ɛ, dok PER3, CRY1 i CRY2 mogu biti fosforilirani samo pomoću CK1ɛ kada su povezani sa PER1 ili PER2.[13]
Inhibitori
[uredi | uredi izvor]Biotehnološke kompanije su proizvele nekoliko inhibitora kako bi olakšale istraživanje o funkciji kazein-kinaze 1 epsilon. Testiranje sa CK1
Pf-670462 i PF-4800567
[uredi | uredi izvor]PF-670462, koji je razvio Pfizer, dobro je okarakterisan inhibitor i CK1
IC261
[uredi | uredi izvor]IC261 je inhibitor koji cilja na ATP-vezujuće mjesto i CK1
Ostali
[uredi | uredi izvor]Za ostale CK1 inhibitore, kao što su D4476 i analozi pirazolopiridina, od kojih oba ciljaju CK1
Također pogledajte
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000213923 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000022433 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Fish KJ, Cegielska A, Getman ME, Landes GM, Virshup DM (June 1995). "Isolation and characterization of human casein kinase I epsilon (CKI), a novel member of the CKI gene family". The Journal of Biological Chemistry. 270 (25): 14875–83. doi:10.1074/jbc.270.25.14875. PMID 7797465.
- ^ Sakanaka C, Leong P, Xu L, Harrison SD, Williams LT (October 1999). "Casein kinase iepsilon in the wnt pathway: regulation of beta-catenin function". Proceedings of the National Academy of Sciences of the United States of America. 96 (22): 12548–52. doi:10.1073/pnas.96.22.12548. PMC 22983. PMID 10535959.
- ^ a b c d e f g h i Knippschild U, Gocht A, Wolff S, Huber N, Löhler J, Stöter M (June 2005). "The casein kinase 1 family: participation in multiple cellular processes in eukaryotes". Cellular Signalling. 17 (6): 675–89. doi:10.1016/j.cellsig.2004.12.011. PMID 15722192.
- ^ a b c d e f g h i j k Yang Y, Xu T, Zhang Y, Qin X (February 2017). "Molecular basis for the regulation of the circadian clock kinases CK1
δ and CK1ε ". Cellular Signalling. 31: 58–65. doi:10.1016/j.cellsig.2016.12.010. PMID 28057520. - ^ a b c d "NCBI CDD CDD Conserved Protein Domain STKc_CK1_delta_epsilon". www.ncbi.nlm.nih.gov. Pristupljeno 2019-04-11.
- ^ Niefind K, Guerra B, Pinna LA, Issinger OG, Schomburg D (May 1998). "Crystal structure of the catalytic subunit of protein kinase CK2 from Zea mays at 2.1 A resolution". The EMBO Journal. 17 (9): 2451–62. doi:10.1093/emboj/17.9.2451. PMC 1170587. PMID 9564028.
- ^ a b Graves PR, Roach PJ (September 1995). "Role of COOH-terminal phosphorylation in the regulation of casein kinase I delta". The Journal of Biological Chemistry. 270 (37): 21689–94. doi:10.1074/jbc.270.37.21689. PMID 7665585.
- ^ Klimczak LJ, Farini D, Lin C, Ponti D, Cashmore AR, Giuliano G (October 1995). "Multiple isoforms of Arabidopsis casein kinase I combine conserved catalytic domains with variable carboxyl-terminal extensions". Plant Physiology. 109 (2): 687–96. doi:10.1104/pp.109.2.687. PMC 157637. PMID 7480353.
- ^ a b c d Etchegaray JP, Machida KK, Noton E, Constance CM, Dallmann R, Di Napoli MN, DeBruyne JP, Lambert CM, Yu EA, Reppert SM, Weaver DR (July 2009). "Casein kinase 1 delta regulates the pace of the mammalian circadian clock". Molecular and Cellular Biology. 29 (14): 3853–66. doi:10.1128/MCB.00338-09. PMC 2704743. PMID 19414593.
- ^ a b c Richards J, Gumz ML (September 2012). "Advances in understanding the peripheral circadian clocks". FASEB Journal. 26 (9): 3602–13. doi:10.1096/fj.12-203554. PMC 3425819. PMID 22661008.
- ^ a b c Ko CH, Takahashi JS (October 2006). "Molecular components of the mammalian circadian clock". Human Molecular Genetics. 15 Spec No 2 (suppl 2): R271-7. doi:10.1093/hmg/ddl207. PMID 16987893.
- ^ Meijer JH, Michel S, Vanderleest HT, Rohling JH (December 2010). "Daily and seasonal adaptation of the circadian clock requires plasticity of the SCN neuronal network". The European Journal of Neuroscience. 32 (12): 2143–51. doi:10.1111/j.1460-9568.2010.07522.x. PMID 21143668. S2CID 12754517.
- ^ a b c Takahashi JS (March 2017). "Transcriptional architecture of the mammalian circadian clock". Nature Reviews Genetics. 18 (3): 164–179. doi:10.1038/nrg.2016.150. PMC 5501165. PMID 27990019.
- ^ Blau J (July 2008). "PERspective on PER phosphorylation". Genes & Development. 22 (13): 1737–40. doi:10.1101/gad.1696408. PMC 2732424. PMID 18593875.
- ^ Akashi M, Tsuchiya Y, Yoshino T, Nishida E (March 2002). "Control of intracellular dynamics of mammalian period proteins by casein kinase I epsilon (CKIepsilon) and CKIdelta in cultured cells". Molecular and Cellular Biology. 22 (6): 1693–703. doi:10.1128/MCB.22.6.1693-1703.2002. PMC 135601. PMID 11865049.
- ^ a b Vielhaber E, Eide E, Rivers A, Gao ZH, Virshup DM (July 2000). "Nuclear entry of the circadian regulator mPER1 is controlled by mammalian casein kinase I epsilon". Molecular and Cellular Biology. 20 (13): 4888–99. doi:10.1128/MCB.20.13.4888-4899.2000. PMC 85940. PMID 10848614.
- ^ Liu N, Zhang EE (2016-09-23). "Phosphorylation Regulating the Ratio of Intracellular CRY1 Protein Determines the Circadian Period". Frontiers in Neurology. 7: 159. doi:10.3389/fneur.2016.00159. PMC 5033960. PMID 27721804.
- ^ Yoo SH, Mohawk JA, Siepka SM, Shan Y, Huh SK, Hong HK, Kornblum I, Kumar V, Koike N, Xu M, Nussbaum J, Liu X, Chen Z, Chen ZJ, Green CB, Takahashi JS (February 2013). "Competing E3 ubiquitin ligases govern circadian periodicity by degradation of CRY in nucleus and cytoplasm". Cell. 152 (5): 1091–105. doi:10.1016/j.cell.2013.01.055. PMC 3694781. PMID 23452855.
- ^ Gietzen KF, Virshup DM (November 1999). "Identification of inhibitory autophosphorylation sites in casein kinase I epsilon". The Journal of Biological Chemistry. 274 (45): 32063–70. doi:10.1074/jbc.274.45.32063. PMID 10542239.
- ^ Eide EJ, Kang H, Crapo S, Gallego M, Virshup DM (2005). "Casein kinase I in the mammalian circadian clock". Methods in Enzymology. 393: 408–18. doi:10.1016/S0076-6879(05)93019-X. ISBN 9780121827984. PMC 1513158. PMID 15817302.
- ^ a b Partch CL, Green CB, Takahashi JS (February 2014). "Molecular architecture of the mammalian circadian clock". Trends in Cell Biology. 24 (2): 90–9. doi:10.1016/j.tcb.2013.07.002. PMC 3946763. PMID 23916625.
- ^ Zhang Y, Qiu WJ, Chan SC, Han J, He X, Lin SC (May 2002). "Casein kinase I and casein kinase II differentially regulate axin function in Wnt and JNK pathways". The Journal of Biological Chemistry. 277 (20): 17706–12. doi:10.1074/jbc.M111982200. PMID 11884395.
- ^ Smadja Storz S, Tovin A, Mracek P, Alon S, Foulkes NS, Gothilf Y (2013-01-21). "Casein kinase 1
δ activity: a key element in the zebrafish circadian timing system". PLOS ONE. 8 (1): e54189. Bibcode:2013PLoSO...854189S. doi:10.1371/journal.pone.0054189. PMC 3549995. PMID 23349822. - ^ a b Badura L, Swanson T, Adamowicz W, Adams J, Cianfrogna J, Fisher K, Holland J, Kleiman R, Nelson F, Reynolds L, St Germain K, Schaeffer E, Tate B, Sprouse J (August 2007). "An inhibitor of casein kinase I epsilon induces phase delays in circadian rhythms under free-running and entrained conditions". The Journal of Pharmacology and Experimental Therapeutics. 322 (2): 730–8. doi:10.1124/jpet.107.122846. PMID 17502429. S2CID 85875627.
- ^ a b Kon N, Sugiyama Y, Yoshitane H, Kameshita I, Fukada Y (2015-07-25). "Cell-based inhibitor screening identifies multiple protein kinases important for circadian clock oscillations". Communicative & Integrative Biology. 8 (4): e982405. doi:10.4161/19420889.2014.982405. PMC 4594307. PMID 26478783.
- ^ Knippschild U, Krüger M, Richter J, Xu P, García-Reyes B, Peifer C, Halekotte J, Bakulev V, Bischof J (2014). "The CK1 Family: Contribution to Cellular Stress Response and Its Role in Carcinogenesis". Frontiers in Oncology (jezik: engleski). 4: 96. doi:10.3389/fonc.2014.00096. PMC 4032983. PMID 24904820.