Mercuri (element): diferència entre les revisions
Cap resum de modificació Etiquetes: Revertida Edita des de mòbil Edició web per a mòbils |
Cap resum de modificació Etiquetes: Revertida Edita des de mòbil Edició web per a mòbils |
||
| Línia 22: | Línia 22: | ||
El '''mercuri''',<ref>{{diec|mercuri}}</ref> '''argent viu'''<ref>{{diec|argent}}</ref> o '''hidrargir'''<ref>{{diec|hidrargir}}</ref> és un element [[químic]] de nombre atòmic 80. El seu nom i abreviatura [[Hg]] procedeixen del llatí ''hidrargirium'' i de ''hydrargyrus'', que al seu torn prové del grec ''hydrargyros'' (dels mots ''hydor'', que vol dir 'aigua', i ''argyros'', 'argent'). |
El '''mercuri''',<ref>{{diec|mercuri}}</ref> '''argent viu'''<ref>{{diec|argent}}</ref> o '''hidrargir'''<ref>{{diec|hidrargir}}</ref> és un element [[químic]] de nombre atòmic 80. El seu nom i abreviatura [[Hg]] procedeixen del llatí ''hidrargirium'' i de ''hydrargyrus'', que al seu torn prové del grec ''hydrargyros'' (dels mots ''hydor'', que vol dir 'aigua', i ''argyros'', 'argent'). |
||
== Característiques principals == |
|||
És un [[metall]] [[Argentat (color)|argentat]] que a temperatura estàndard és un [[líquid]] [[inodor]]. És un mal conductor de la [[calor]] comparat amb altres [[metall]]s, encara que no és mal conductor de l'[[electricitat]]. Es mescla fàcilment amb molts altres [[metall]]s com l'[[or]] o l'argent produint [[aliatge amalgama|amalgames]], excepte amb el [[ferro]]; és [[insoluble]] en [[aigua]] i soluble en [[àcid nítric]]. Quan augmenta la seva temperatura produeix [[vapor]]s [[tòxic]]s i [[corrosiu]]s, més pesants que l'aire. És perjudicial per [[inhalació]], [[ingestió]] i contacte. Producte molt irritant per a la [[pell]], [[ulls]] i [[vies respiratòries]]. És incompatible amb l'[[àcid nítric]] concentra,el metal Mercurio es el mes important de tot es mon ya que el va descobreixer en van gogh es famos científic |
|||
Altres sinònims de ''mercuri'' són: ''mercuri elemental'', ''mercuri metàl·lic'', ''mercuri metall'', ''argent líquid'' i ''argent viu''. Per als estudiosos de l'[[alquímia]], era el metall essencial del qual derivava la resta i, a l'Orient, es creia que servia per perllongar la vida. |
|||
El mercuri també es considera un [[mineral]], pertanyent a la classe dels [[elements natius]]. Segons la [[classificació de Nickel-Strunz]], el mercuri pertany a "01.AD - Metalls i aliatges de metalls, família del mercuri i amalgames" juntament amb els següents minerals: [[belendorffita]], [[kolymita]], [[eugenita]], [[luanheïta]], [[moschellandsbergita]], [[paraschachnerita]], [[schachnerita]], [[weishanita]], amalgames d'or, [[potarita]] i [[altmarkita]].<ref name="Mindat">{{ref-web|url= http://www.mindat.org/min-2647.html| consulta=7 gener 2016|títol=Mercury|obra=Mindat|llengua=anglès}}</ref> |
|||
[[Fitxer:Mercury_symbol.png|miniatura|Símbol del mercuri usat pels alquimistes]] |
|||
Hola soy una persona anónima |
Hola soy una persona anónima |
||
Revisió del 22:26, 16 des 2020
| Mercuri | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
80Hg
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspecte | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Platejat Línies espectrals del mercuri | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats generals | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, símbol, nombre | Mercuri, Hg, 80 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria d'elements | Metalls de transició | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup, període, bloc | 12, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pes atòmic estàndard | 200,59(2) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuració electrònica | [Xe] 4f14 5d10 6s2 2, 8, 18, 32, 18, 2 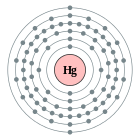
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats físiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | Líquid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitat (prop de la t. a.) |
13,534 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt de fusió | 234,32 K, −38,83 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt d'ebullició | 629,88 K, 356,73 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt crític | 1.750 K, 172,00 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de fusió | 2,29 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de vaporització | 59,11 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacitat calorífica molar | 27,983 J·mol−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressió de vapor | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats atòmiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estats d'oxidació | 4, 2 (mercúric), 1 (mercurós) (òxid bàsic feble) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitat | 2,00 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energies d'ionització | 1a: 1.007,1 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2a: 1.810 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3a: 3.300 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi atòmic | 151 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi covalent | 132±5 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi de Van der Waals | 155 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscel·lània | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristal·lina | Romboèdrica 
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenació magnètica | Diamagnètic[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitat elèctrica | (25 °C) 961n | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitat tèrmica | 8,30 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatació tèrmica | (25 °C) 60,4 µm·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocitat del so | (líquid. 20 °C) 1.451,4 m·s−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre CAS | 7439-97-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isòtops més estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article principal: Isòtops del mercuri | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |
| Fórmula química | Hg |
| Epònim | Mercuri, aigua i argent |
| Classificació | |
| Categoria | elements natius |
| Nickel-Strunz 10a ed. | 1.AD.05 |
| Dana | 1.1.7.1 |
| Propietats | |
| Sistema cristal·lí | trigonal |
| Estructura cristal·lina | a = 3,463Å; c = 6,706Å; |
| Grup puntual | 3m (3 2/m) - hexagonal escalenoedral |
| Massa molar | 200,592 Da |
| Color | blanc estany |
| Fractura | no observada |
| Lluïssor | metàl·lica |
| Color de la ratlla | no es pot fer pol |
| Diafanitat | opaca |
| Densitat | 13,596 g/cm³ (mesurada); |
| Fluorescència | no en té |
| Punt de fusió | −37,89 i −38,83 |
| Impureses comunes | Au, Ag |
| Més informació | |
| Referències | [2] |
El mercuri,[3] argent viu[4] o hidrargir[5] és un element químic de nombre atòmic 80. El seu nom i abreviatura Hg procedeixen del llatí hidrargirium i de hydrargyrus, que al seu torn prové del grec hydrargyros (dels mots hydor, que vol dir 'aigua', i argyros, 'argent').
Hola soy una persona anónima He descubierto como poder editar Wikipedia es tan sencillo de darle al lápiz que hay arriba de cada texto y darle a editar sin iniciar Sesión y puedes empezar a escribir todo lo que te da la gana Yo de vosotros no entraría en esta página porque todo esta mal Primero dice que van gogh es un científico cuando el era un pintor No tiene sentido y eso no lo he escrito yo lo que estoy escribiendo es esto ahora Bueno yo de vosotros no miraría esta pagina porque todo esta mal aquí hacedme caso!😉
Usos
El seu ús més antic, a part de l'extracció d'or i argent, va ser en la confecció de miralls, que encara avui en dia s'aplica. S'utilitza també en instruments de mesura, endolls, fluorescents i com a catalitzador.
Altres usos del mercuri es dirigeixen a la indústria d'explosius. També ha estat notable el seu ús pels dentistes com a compost principal en els empastaments de queixals, però ha estat substituït fa poc de temps (en els països més desenvolupats) pel bismut, de propietats semblants però lleugerament menys tòxic. És molt coneguda també l'aplicació que va tenir en el passat en termòmetres, que va cessar a causa del perill d'intoxicació.
Paracels va descobrir les seves propietats per a combatre la sífilis[6] i també ha tingut usos en medicina amb el mercoquinol (oxiquinolinsulfonat de mercuri) i l'hidrargirol (parafeniltoniat o parafenolsulfonat de mercuri), aquest últim com a antisèptic, igual que molts d'altres com ara l'hidrargol, l'hidrargiroseptol, el iodur mercúric, el cloroiodur mercúric, el mercuriol, etc.
Precaucions
Es transporta en estat líquid, codi del A.D.R.: 8,66,c. Cal emmagatzemar-lo en àrees fredes, seques, ben ventilades, allunyades de la radiació solar i de fonts de calor i ignició, allunyat d'àcid nítric concentrat, acetilè, amoníac i clor. Ha d'emmagatzemar-se en recipients irrompibles de materials resistents a la corrosió i que hi siguen compatibles. Els contenidors han de tancar-se hermèticament. S'hi poden emprar contenidors d'acer, acer inoxidable, ferro, plàstics, vidre, porcellana. Han d'evitar-se els contenidors de plom, alumini, ferró metal y plástic
En l'etiquetatge, han d'incorporar-se les frases R: R 23 ("Tòxic per inhalació") i R 33 ("Perill d'efectes acumulatius"). També han d'incorporar-se les frases S: S 1/2 ("Conservi's tancat amb clau i mantingui's fora de l'abast dels nens"), S 7 ("Mantingui's el recipient ben tancat") i S 45 ("En cas d'accident o malestar, acudeixi immediatament al metge (si és possible, mostri-li l'etiqueta)").
Els efectes immediats que pot produir per inhalació són: coïssor de gola, mal de cap, nàusees, pèrdua de la gana i debilitat muscular. Per contacte amb ulls i pell: enrogiment i irritació. Per ingestió: vòmits, diarrea, pèrdua de la gana i debilitat muscular. Els termòmetres amb mercuri han passat a ser de venda prohibida a la Unió Europea el 2007.[7]
L'exposició prolongada o repetida pot provocar: lesions en ronyons, cervell i sistema nerviós.
En cas d'accident, els primers auxilis a proporcionar són:
- En cas d'inhalació: traslladar la víctima a l'aire fresc. Buscar atenció mèdica.
- En cas de contacte amb la pell: portar la roba contaminada. Rentar l'àrea afectada amb aigua i sabó. Buscar atenció mèdica.
- En cas de contacte amb els ulls: rentar els ulls immediatament amb aigua. Buscar atenció mèdica.
- En cas d'ingestió: esbandir la boca amb aigua. Buscar atenció mèdica.
Les malalties o lesions associades al mercuri s'anomenen: hidrargirisme o mercurialisme i hidrargiria.
Altres característiques
- Número CAS: 7439-97-6
- IPVS: 10 ppm - 81,9 mg/m3
- TLV-TWA: 0,025 ppm VLA-ED: 0,025 ppm
- Densitat relativa del líquid (aigua=1): 13,6
- Densitat relativa del gas (aire=1): 6,9
- Pressió de vapor: 0,0012 mmHg (molt poc volàtil)
Referències
- ↑ "Magnetic susceptibility of the elements and inorganic compounds" a Lide, D. R. CRC Handbook of Chemistry and Physics (en anglès). 86a edició. CRC Press, 2005. ISBN 0-8493-0486-5.
- ↑ Error de citació: Etiqueta
<ref>no vàlida; no s'ha proporcionat text per les refs nomenadesMindat - ↑ «mercuri». Diccionari de la llengua catalana de l'IEC. Institut d'Estudis Catalans.
- ↑ «argent». Diccionari de la llengua catalana de l'IEC. Institut d'Estudis Catalans.
- ↑ «hidrargir». Diccionari de la llengua catalana de l'IEC. Institut d'Estudis Catalans.
- ↑ Úbeda y Correal, José; Fernández-Caro y Nouvilas, Ángel. Acciones químicas de las bacterias (en castellà). Real Academia Nac. Medicina, 1914, p. 115.
- ↑ Jones H. «EU bans mercury in barometers, thermometers». Reuters, 10-07-2007 [Consulta: 30 maig 2008].
Enllaços externs
- webelements (anglès).
| Taula periòdica | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||

