Enllaç per pont d'hidrogen
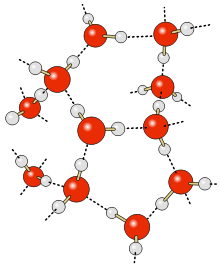
Un enllaç per pont d'hidrogen és una forma d'associació entre un àtom electronegatiu i un àtom d'hidrogen enllaçat amb enllaç covalent a un segon àtom relativament electronegatiu. És una interacció electroestàtica augmentada per la petita grandària de l'hidrogen, que permet la proximitat dels dipols o càrregues que interactuen. Els dos àtoms electronegatius solen ser (però no necessàriament) de la primera fila de la taula periòdica, és a dir, N, O o F. Els enllaços per pont d'hidrogen poden ser intermoleculars o intramoleculars.[1]
Història
[modifica]El 1939 el químic estatunidenc Linus Pauling (1901–1994) dedicà un capítol a l'enllaç per pont d'hidrogen en el seu famós llibre The nature of chemical bond (La naturalesa de l'enllaç químic), on indicà que la primera referència a aquest tipus d'interacció és a un article publicat al Journal of the Chemical Society el 1912, titulat The state of amines in aqueous solution,[2] els quals autors són els químics anglesos Tom Sidney Moore i T. F. Winmill. En la segona part de l'article, Moore interpreta els valors obtinguts per Winmill de constants d'ionització de diversos hidroclorurs d'amines, en particular el fet que el trimetilamoni és una base més feble que el tetrametilamoni, proposant l'existència d'algun tipus de força feble d'interacció.[3] Gilbert Newton Lewis (1875–1946), per la seva banda, indicà que el concepte d'enllaç per pont d'hidrogen es deu al químic estatunidenc Maurice Loyal Huggins (1897–1981) en la seva tesi de postgrau (no publicada) del 1919 dirigida per Lewis a la Universitat de Califòrnia a Berkeley, i el primer article publicat sobre l'enllaç d'hidrogen es deu als químics estatunidencs Wendell Mitchell Latimer (1893–1955) i Worth Huff Rodebush (1887–1959) el 1920,[4][5] del mateix grup de recerca que citaren Huggins. En aquest article explicaren l'enllaç per pont d'hidrogen suposant que l'àtom d'hidrogen pot compartir dues parelles d'electrons, en contra de la regla de l'octet del mateix Lewis. En aquell moment no existia cap mètode experimental per comprovar aquesta hipòtesi i els investigadors confiaren en la seva imaginació i càlculs termodinàmics senzills per interpretar les seves observacions sobre desviacions de llei de Raoult, punts anormals de fusió i ebullició, reducció de la solubilitat, moments dipolars anormals i altres propietats. Huggins indicà que la «valència secundària» utilitzada per Werner a la teoria de Lewis de l'enllaç covalent per compartició de parelles d'electrons entre dos àtoms (o ions) pot ser formada utilitzant un «parell solitari» en les capes de valència d'un dels àtoms enllaçats.[6]

Després de 1925 es disposà de l'anàlisi d'estructures mitjançant raigs X i estructures cristal·lines d'una sèrie de compostos amb enllaços d'hidrogen es publicaren, malgrat que les interpretacions no sempre foren correctes. L'estudi de l'«enllaç per pont d'hidrogen» s'inicià després de 1930. El 1931 Pauling publicà un article[7] sobre la naturalesa de l'enllaç químic on discutí la naturalesa de l'enllaç a l'ió [H:F:H] ̄ utilitzant el terme «enllaç d'hidrogen». També assignà aquests enllaços als àtoms d'oxigen i nitrogen. Huggins, el 1931, discutí la conducció d'ions d'hidrogen i hidroxils en aigua. El científic irlandès John Desmond Bernal (1901–1971) i l'anglès Ralph H. Fowler (1889–1944) en un article del 1933 descrigueren les propietats de l'aigua en relació amb la seva estructura en estat líquid i sòlid introduint una coordinació tetraèdrica de la molècula d'aigua en aigua líquida i el polimorfisme del gel. En aquest moment la recollida de dades a baixa temperatura per a cristalls no estava disponible per a la determinació de l'estructura. Tanmateix s'utilitzaren espectres Raman dependents de la temperatura i canvis en les propietats físiques de l'aigua i el gel (densitat, polaritat) sobre la temperatura per verificar les seves hipòtesis encara que no s'utilitzà el terme «enllaç d'hidrogen». El 1931 i 1933 Astbury et al. van publicar dos articles relacionats amb la difracció de raigs X de fibra de polipèptids de seda, cabell i llana, però amb falta d'explicació dels canvis estructurals, induïts pel plegament i desplegament d'un polipèptid cadena per enllaços d'hidrogen; el terme «pont d'hidrogen àtoms» s'utilitzava únicament. No obstant això, els autors van reconèixer el maridatge de grups d'aminoàmino secundaris polars i carbonílics il'estructura proposada era essencialment la mateixa que conegut avui.[6]
En el període de dos anys (1935-1936) es publicaren quatre articles bàsics sobre els enllaços per pont d'hidrogen. Pauling explicà els enllaços per pont d'hidrogen en aigua i gel.[8] Bernal i Megaw descrigueren «enllaços hidroxils» en hidròxids de metalls, minerals i aigua, introduint distinció entre O–H···O–H i O–H···O=C. Dos articles foren publicats per Huggins, Hydrogen bridges in organic compounds i Hydrogen bridges in ice and water. L'enllaç per pont d'hidrogen fou clarament introduït com una interacció important en la química estructural en un capítol del llibre de Pauling The nature of the chemical bond[9] el 1939. Els dos treballs històrics d'alta rellevància que assenyalaren el paper de l'enllaç per pont d'hidrogen en estructures de molècules biològiques estan relacionats amb els plegaments de proteïnes, l'hèlix alfa dels estatunidencs Pauling, Robert B. Corey (1897–1971) i Herman R. Branson (1914–1995) del 1951[10] i amb l'estructura de l'ADN de l'estatunidenc James D. Watson (1928–) i l'anglès Francis H. C. Crick (1916–2004) del 1953.[11][6]
Característiques
[modifica]
L'enllaç per pont d'hidrogen és una interacció amb un àtom d'hidrogen situat entre un parell d'altres àtoms que tenen una alta afinitat per als electrons, són molt electronegatius; aquest enllaç és més feble que un enllaç iònic o que un covalent, però més fort que d'altres forces intermoleculars com les forces de van der Waals, aproximadament 10 vegades més fort que les altres tipus de forces intermoleculars. Els enllaços d'hidrogen poden existir entre àtoms en diferents molècules o en parts de la mateixa molècula. Alhora d'interpretar l'enllaç per pont d'hidrogen cal tenir en compte dues componets:

- Component iònica. Un àtom de la parella (el donant), generalment un àtom de fluor, oxigen o nitrogen, s'uneix mitjançant enllaç covalent a un àtom d'hidrogen (F–H, ―O–H o =N–H). Els electrons que constitueixen l'enllaç són compartits de forma desigual ja que l'alta electronegativitat d'aquests elements fa que els electrons de l'enllaç estiguin desplaçats cap a l'àtom electronegatiu i l'hidrogen presenti una lleugera càrrega positiva. L'altre àtom de la parella, també típicament F, O o N, té una parella d'electrons no compartits, el que li dona una lleugera càrrega negativa. Es produeix, per tant, una atracció electroestàtica entre l'hidrogen i l'àtom acceptor d'una altra molècula o zona de la mateixa molècula. Aquesta interacció pot representar-se per A–H··· B, on A i B són àtoms de qualsevol dels tres elements esmentats anteriorment i l'àtom d'hidrogen es troba sobre una línia recta entre els nuclis d'A i B, A–H representa un enllaç covalent i H···B un enllaç per pont d'hidrogen.[12]

Estructura de la doble hèlix d'ADN on els enllaços per pont d'hidrogen es representen amb línies de punts - Component covalent. Una d'elles interpreta l'enllaç en el marc de la teoria dels orbitals moleculars. A l'enllaç A–H participa un orbital atòmic de l'element A i un orbital atòmic 1s de l'hidrogen; i la parella solitària d'electrons a B ocupa un orbital atòmic de B. Quan els tres àtoms estan alineats, aquests tres orbitals atòmics poden superposar-se i formar tres orbitals moleculars: un d'enllaçant, un de no-enllaçant i un antienllaçant. Hi ha quatre electrons per allotjar (dos de l'enllaç A―H original i dos de la parella solitària). Ocupen els orbitals moleculars enllaçant i no-enllaçant, deixant vacant l'orbital antienllaçant. Per tant, l'efecte net és reduir l'energia de l'agrupació AHB i, per tant, constituir un enllaç intermolecular. Una vegada més, en trobar-se amb l'enllaç d'hidrogen, un es troba amb un gir en l'actitud convencional; la pregunta que planteja aquesta interpretació no és per què es produeix aquest enllaç, sinó per què no es produeix de manera més general. L'explicació rau en la petita grandària de l'àtom d'hidrogen, que permet que l'equilibri d'energies en l'esquema d'orbitals moleculars sigui favorable a l'enllaç.[13]
L'enllaç per pont d'hidrogen és responsable, per exemple, de l'existència de l'aigua com a líquid a temperatures normals quan, a causa de la seva baixa massa molar, l'aigua hauria d'estar en estat de gas. L'aigua també és un bon dissolvent per als compostos iònics i molts altres perquè forma fàcilment enllaços per pont d'hidrogen amb el solut. L'enllaç per pont d'hidrogen també és responsable de l'existència com a sòlids de moltes molècules orgàniques que contenen grups hidroxils (–OH); els glúcids glucosa i sacarosa en són exemples. Els enllaços per pont d'hidrogen entre aminoàcids en una molècula de proteïna lineal determina la forma en què es plega en la seva configuració funcional. Els enllaços per pont d'hidrogen entre bases nitrogenades en nucleòtids en les dues cadenes d'ADN (parells de guanina amb citosina, adenina amb timina) donen lloc a l'estructura de doble hèlix que és crucial per a la transmissió d'informació genètica.[12][13]
Tipus
[modifica]| Fort | Moderat | Feble | |
|---|---|---|---|
| Energia d'enllaç
(kJ/mol) |
63–167 | 17–63 | <17 |
| Exemples | [F···H···F]–
[N···H···N]+ P–OH···O=P |
O–H···O=C
N–H···O=C O–H···O–C |
C–H···O
N–H···F–C O–H··· |
| Longitud X–H (Å) | 0,05–0,2 | 0,01–0,05 | ≤0,01 |
| Longitud H···A (Å) | 1,2–1,5 | 1,5–2,2 | 2,0–3,0 |
| Covalència | Pronunciada | Feble | Inexistent |
| Electrostàtic | Significant | Dominant | Moderat |
Els enllaços per pont d'hidrogen es classifiquen principalment en funció de la força de la interacció mesurada per la intensitat de l'energia d'enllaç al complex. Normalment es distingeixen tres classes: enllaços febles, moderats i forts, amb límits energètics al voltant de 2 i 15 kcal/mol (els enllaços covalents són molt més forts, entre 30 i 120 kcal/mol).[15]
Febles
[modifica]Els enllaços d'hidrogen febles impliquen grups poc polars X–H en donants de protons, com els grups C–H o P–H, o acceptors febles polars, com la molècula N₂ del complex N₂···HF. A més, els enllaços d'hidrogen on X–H s'adhereix a un enllaç
Moderats
[modifica]
El grup de substàncies amb enllaços moderats d'hidrogen és el majoritari. El dímer d'aigua o el dímer de fluorur d'hidrogen són exemples típics d'aquest grup. Altres parelles conegudes d'aquest grup són els àcids carboxílics, les parelles de bases als àcids nucleics i els enllaços típics per pont d'hidrogen que es formen dins o entre proteïnes.[15] Són responsables dels elevats punts de fusió i ebullició d'importants substàncies com l'aigua i l'amoníac.
Forts
[modifica]Els enllaços d'hidrogen forts impliquen espècies iòniques. Alguns exemples són Cl–⋯H₂O, F–⋯H₂O, H₃O+⋯H₂O i F–⋯HF amb energies d'interacció d'uns 15, 30, 35 i 40 kcal/mol, respectivament. En el cas de l'últim complex, l'enllaç és tan fort que aquest complex també es podria classificar com un enllaç químic. A més, la distància H⋯F- d'aproximadament 1,3 Å està més a prop de les distàncies típiques dels enllaços químics (aproximadament 1 Å) que de les distàncies d'enllaç d'hidrogen H⋯Y (aproximadament 2 Å). Els enllaços d'hidrogen forts donen com a resultat una distorsió significativa de l'estructura del monòmer. L'enllaç H–F en F–⋯HF és de la mateixa longitud que l'enllaç d'hidrogen F–⋯H (és a dir, el complex és centrosimètric). Així, la distància F–H s'incrementa de 0,93 Åa 1,30 Å sobre la formació de dímers. Aquest és, però, un cas extrem. Per a F–⋯H₂O la distància O–H enllaçada amb hidrogen augmenta al voltant de 0,1 Å del seu valor de monòmer aïllat per equilibri de 0,96 Å, i aquesta mida d'elongació és típica per als sistemes iònics. L'enllaç d'hidrogen entre ions i aigua és el mecanisme principal dels processos d'hidratació.[15]
Referències
[modifica]- ↑ Chemistry (IUPAC), The International Union of Pure and Applied. «IUPAC - Hydrogen bond (H02899)». [Consulta: 5 juny 2021].
- ↑ Moore, Tom Sidney; Winmill, Thomas Field «CLXXVII.—The state of amines in aqueous solution» (en anglès). Journal of the Chemical Society, Transactions, 101, 1912, pàg. 1635–1676. DOI: 10.1039/CT9120101635. ISSN: 0368-1645.
- ↑ Goymer, Patrick «100 years of the hydrogen bond» (en anglès). Nature Chemistry, 4, 11, 11-2012, pàg. 863–864. DOI: 10.1038/nchem.1482. ISSN: 1755-4349.
- ↑ Latimer, Wendell M.; Rodebush, Worth H. «Polarity and Ionization from the Standpoint of the Lewis Theory of Valence». Journal of the American Chemical Society, 42, 7, 01-07-1920, pàg. 1419–1433. DOI: 10.1021/ja01452a015. ISSN: 0002-7863.
- ↑ «Latimer and Rodebush on the Hydrogen Bond». [Consulta: 7 juny 2021].
- ↑ 6,0 6,1 6,2 Kojić-Prodić, B.; Molcanov, K. «The Nature of Hydrogen Bond: New Iinsights Into Old Theories». Acta Chimica Slovenica, 55, 2008, pàg. 692-708.
- ↑ Pauling, Linus. «The Nature of the Chemical Bond. Application of Results Obtained from the Quantum Mechanics and from a Theory of Paramagnetic Susceptibility to the Structure of Molecules». Journal of the American Chemical Society, 53, 4, 4-1931, pàg. 1367–1400. DOI: 10.1021/ja01355a027. ISSN: 0002-7863.
- ↑ Pauling, L.C. «The Structure and Entropy of Ice and of Other Crystals with Some Randomness of Atomic Arrangement». Journal of the American Chemical Society, 57, 12, 1935, pàg. 2680-2684.
- ↑ Linus., Pauling,. The nature of the chemical bond and the structure of molecules and crystals : an introduction to modern structural chemistry. Cornell Univ. Press, [ca. 2010]. ISBN 978-0-8014-0333-0.
- ↑ Pauling, L.; Corey, R. B.; Branson, H. R. «The structure of proteins: Two hydrogen-bonded helical configurations of the polypeptide chain» (en anglès). Proceedings of the National Academy of Sciences, 37, 4, 01-04-1951, pàg. 205–211. DOI: 10.1073/pnas.37.4.205. ISSN: 0027-8424. PMC: PMC1063337. PMID: 14816373.
- ↑ Watson, J. D.; Crick, F. H. C. «Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid» (en anglès). Nature, 171, 4356, 4-1953, pàg. 737–738. DOI: 10.1038/171737a0. ISSN: 1476-4687.
- ↑ 12,0 12,1 «Hydrogen bonding» (en anglès). Encyclopædia Britannica, 2003.
- ↑ 13,0 13,1 «Chemical bonding» (en anglès). Encyclopædia Britannica, 2003.
- ↑ MacLeod, J.M.; Rosei, F. «Directed Assembly of Nanostructures» (en anglès). Comprehensive Nanoscience and Technology, 01-01-2011, pàg. 13–68. DOI: 10.1016/B978-0-12-374396-1.00098-2.
- ↑ 15,0 15,1 15,2 15,3 Szalewicz, K. «Hydrogen Bond». A: Encyclopedia of Physical Science and Technology. 3a. Academic Press, 2003, p. 505-538.
- ↑ Desiraju, G. R.. The weak hydrogen bond : in structural chemistry and biology. Oxford: Oxford University Press, 1999. ISBN 978-0-19-170820-6.
