Oganessó
| Oganessó | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
118Og
| |||||||||||||
| |||||||||||||
| Aspecte | |||||||||||||
| Desconegut | |||||||||||||
| Propietats generals | |||||||||||||
| Nom, símbol, nombre | oganessó, Og, 118 | ||||||||||||
| Grup, període, bloc | 18, 7, p | ||||||||||||
| Pes atòmic estàndard | [294] | ||||||||||||
| Configuració electrònica | [Rn] 5f14 6d10 7s2 7p6[1] (predicció) 2, 8, 18, 32, 32, 18, 8 (predicció)[1] 
| ||||||||||||
| Propietats físiques | |||||||||||||
| Fase | Sòlid (predicció) | ||||||||||||
| Densitat (prop de la t. a.) |
13,65 (predicció)[2] g·cm−3 | ||||||||||||
| Punt d'ebullició | 350 ± 30 (extrapolació)[1] K, 80 ± 30 °C | ||||||||||||
| Punt crític | 439 (extrapolació)[3] K, 6,8[3] MPa | ||||||||||||
| Entalpia de fusió | 23,5 (extrapolació)[3] kJ·mol−1 | ||||||||||||
| Entalpia de vaporització | 19,4 (extrapolació)[3] kJ·mol−1 | ||||||||||||
| Propietats atòmiques | |||||||||||||
| Estats d'oxidació | −1 (predicció),[4] 0, +2[5], +4[5], +6[4] | ||||||||||||
| Energies d'ionització | 1a: 75 ± 155 (extrapolació)[1] kJ·mol−1 | ||||||||||||
| 2a: 1,450 (extrapolació)[6] kJ·mol−1 | |||||||||||||
| Radi atòmic | 152 (predicció)[2] pm | ||||||||||||
| Radi covalent | 157 (predicció)[7] pm | ||||||||||||
| Miscel·lània | |||||||||||||
| Nombre CAS | 54144-19-3[8] | ||||||||||||
| Isòtops més estables | |||||||||||||
| Article principal: Isòtops de l'oganessó | |||||||||||||
| |||||||||||||
L'oganessó és l'element químic sintètic de símbol Og i nombre atòmic 118. Fou sintetitzat per primera vegada el 2002 per un equip mixt de científics russos i estatunidencs a l'Institut Unificat de Recerca Nuclear (IURN) de Dubnà, prop de Moscou (Rússia). El desembre del 2015 fou reconegut pel Grup de Treball Conjunt de la Unió Internacional de Química Pura i Aplicada (IUPAC) i la Unió Internacional de Física Pura i Aplicada (IUPAP), juntament amb tres altres elements nous. El 28 de novembre del 2016 li fou assignat un nom formalment.[10] El nom fou triat en honor de Iuri Oganessian, que ha contribuït de manera important al descobriment dels elements més pesants de la taula periòdica. Era tan sols la segona vegada a la història que un element rebia el nom d'un científic viu en el moment de l'anomenament, després del seaborgi, i és l'únic element anomenat en honor d'una persona viva avui en dia.[11]
L'àtom d'oganessó és radioactiu i molt inestable i des del 2005 tan sols se n'han detectat cinc (possiblement sis) de l'isòtop oganessó 294,[12] cosa que ha limitat molt els experiments per determinar-ne les propietats i els compostos que pot formar. Tanmateix, els càlculs teòrics han ofert moltes prediccions, incloent-n'hi algunes de sorprenents. Per exemple, malgrat que l'oganessó forma part del grup 18 (gasos nobles), és possible que sigui força reactiu, a diferència dels altres elements d'aquest grup.[13] Abans es creia que en condicions normals és un gas, però ara es considera probable que sigui un sòlid a causa dels efectes relativistes.[13] En la taula periòdica, és un element del bloc p i l'últim del període 7.
Història
[modifica]Intents fallits
[modifica]A finals del 1998, el físic polonès Robert Smolańczuk publicà càlculs sobre la fusió de nuclis atòmics per sintetitzar àtoms superpesants, incloent-hi l'element 118.[14] Els seus càlculs suggerien que seria possible crear l'element 118 fusionant plom amb criptó en condicions molt controlades.[14]
El 1999, investigadors del Laboratori Nacional Lawrence de Berkeley utilitzaren aquestes prediccions i anunciaren el descobriment dels elements 116 i 118, en un article publicat a Physical Review Letters,[15] i molt aviat els resultats foren recollits a Science.[16] Els investigadors afirmaven haver dut a terme la reacció
L'any següent, publicaren una retracció després que investigadors d'altres laboratoris fossin incapaços de repetir els resultats, igual que el mateix laboratori de Berkeley.[17] El juny del 2002, el director del laboratori anuncià que l'al·legació inicial del descobriment d'aquests dos elements s'havia basat en dades inventades per l'autor principal Víktor Ninov.[18]
Pretès descobriment
[modifica]La primera pretesa desintegració d'àtoms d'oganessó fou observada a l'Institut Unificat de Recerca Nuclear (IURN) de Dubna (Rússia) el 2002.[19] El 9 d'octubre del 2006, investigadors del IURN i el Laboratori Nacional Lawrence de Berkeley de Califòrnia, que treballaven al IURN a Dubna, anunciaren[9] que havien detectat indirectament un total de tres (possiblement quatre) nuclis d'oganessó 294 (un o dos el 2002[20] i dos més el 2005) produïts per mitjà de col·lisions d'àtoms de californi-249 amb ions de calci-48:[21][22][23][24][25]
Tanmateix, l'any 2011, la IUPAC va avaluar els resultats obtinguts l'any 2006 per la col·laboració Dubna-Livermore i va considerar que no satisfeien els criteris per considerar descobert l'oganessó.[26]

L'experiment que serví per produir la primera pretesa instància enregistrada de síntesi d'oganessó va durar quatre mesos, al cap dels quals s'havia bombardejat l'objectiu de californi amb 4×1019 ions de calci.[8] S'ha de tenir en compte que la probabilitat que es produeixi la reacció de fusió és extremament baixa, ja que el tall de secció de fusió és molt petit, de ~0.3–0.6 pb = (3–6)×10−41 m² exactament. La possibilitat que les deteccions fossin esdeveniments aleatoris, el que implicaria falsos positius, s'estimà en menys d'una part entre 100.000.[27]
En els experiments, s'observà la desintegració alfa de tres àtoms d'oganessó. També es proposà una quarta desintegració per fissió espontània directa. Es calculà un període de semidesintegració de 0,89 ms: el 294Og es converteix en 290Lv per desintegració alfa. Com que només hi havia tres nuclis, aquesta aproximació té una gran incertesa, de 0,89+1,07−0,31 ms.[9]
La identificació dels nuclis de 294Og fou verificada creant per separat el suposat nucli fill 290Lv mitjançant el bombardeig de 245Cm amb ions de 48Ca,
i comprovant que la desintegració del 290Lv concordava amb la cadena de desintegració dels nuclis de 294Og.[9] El nucli fill 290Lv és molt inestable, i es desintegra en 286Fl. Aquest nucli pot patir o bé fissió espontània o bé desintegració alfa en 282Cn, que sofreix fissió espontània.[9]
En un model de tunelització quàntica, es predigué que la semivida de desintegració alfa del 294Og seria 0,66+0,23−0,18 ms[28] i el valor Q experimental fou publicat el 2004.[29] El càlcul amb valors Q teòrics del model macroscòpic-microscòpic de Muntian–Hofman–Patyk–Sobiczewski dona uns resultats un xic baixos però comparables.[30]
Nom
[modifica]Fins a la dècada del 1960, l'oganessó era conegut com a «eka-emanació» («emanació» és l'antic nom del radó).[31] El 1979 la IUPAC publicà recomanacions segons les quals l'element havia de dir-se «ununocti»,[32] un nom sistemàtic, com a pantònim fins que es confirmi el descobriment de l'element i la IUPAC decideixi un nom.
Abans de la retracció del 2002, els investigadors de Berkeley tenien la intenció d'anomenar l'element «ghiorsi» (Gh) en honor d'Albert Ghiorso (un dels membres principals de l'equip d'investigació).[33]
Els descobridors russos publicaren la seva síntesi el 2006. El 2007, el cap de l'institut rus afirmà que l'equip estava valorant dos noms pel nou element: «flerovi», en honor de Gueorgui Fliórov, el fundador del laboratori d'investigació a Dubnà; i «moscovi», en honor de l'óblast de Moscou, on es troba Dubnà.[34] També afirmà que tot i que l'element fou descobert en col·laboració amb els estatunidencs, que proporcionaren la diana de californi, seria just que l'element fos anomenat en honor de Rússia, car el Laboratori Fliórov de Reaccions Nuclears del IURN tenia les úniques instal·lacions del món que podien assolir aquest resultat.[35][36] Més endavant es proposaren aquests noms per als elements 114 (flerovi) i 116 (moscovi).[37] A més a més, finalment es proposaren els noms «livermori» per a l'element 116[38] i «moscovi» per a l'element 115.[39]
Estabilitat del nucli i isòtops
[modifica]
No hi ha cap element de nombre atòmic superior a 82 (després del plom) que tingui isòtops estables. L'estabilitat del nucli disminueix amb l'augment del nombre atòmic, de manera que tots els isòtops amb un nombre atòmic per sobre de 101 es desintegren radioactivament amb un període de semidesintegració inferior a un dia. Tanmateix, per motius que encara no estan ben compresos, els elements entre el 110 i el 114 tenen una estabilitat nuclear lleugerament més alta, que porta a l'aparició del que en física nuclear es coneix com a «illa d'estabilitat». Aquest concepte, proposat pel professor de la UC Berkeley Glenn Seaborg, explica per què els elements superpesants tenen una semivida més llarga del que s'havia predit.[40] L'oganessó és radioactiu i té un període de semidesintegració que sembla de menys d'un mil·lisegon. Tanmateix, aquesta durada supera alguns valors predits,[28][41] fet que consolida la idea d'aquesta «illa d'estabilitat».[42]
Els càlculs amb un model de tunelització quàntica prediuen l'existència de diversos isòtops de l'element 118 rics en neutrons, amb una semivida propera a 1 ms.[43][44]
Els càlculs teòrics sobre les rutes sintètiques i la semivida d'altres isòtops han mostrat que alguns podrien ser lleugerament més estables que l'isòtop sintetitzat 294Og, sent els més probables 293Og, 295Og, 296Og, 297Og, 298Og, 300Og i 302Og.[28][45] D'aquests, el 297Og sembla representar la millor probabilitat d'obtenir nuclis més longeus,[28][45] per la qual cosa podria esdevenir l'objecte de futur treball amb aquest element. Alguns isòtops amb molts més neutrons, com ara alguns situats al voltant del 313Og, també podrien oferir nuclis més longeus.[46]
Propietats atòmiques i físiques calculades
[modifica]L'oganessó és un membre del grup 18, els elements de valència zero. Els membres d'aquest grup són habitualment inerts a les reaccions químiques més comunes (per exemple, la combustió), car la capa de valència externa està completament ocupada per vuit electrons. Això produeix una configuració estable d'energia mínima en què els electrons exteriors estan enllaçats fermament.[47] Es creu que, de manera similar, l'oganessó té una capa de valència exterior tancada, en què els electrons de valència estan distribuïts en una configuració 7s²7p⁶.[48]
Per consegüent, alguns s'esperen que l'oganessó tingui propietats físiques i químiques semblants a les dels altres membres del seu grup, sent especialment similar al gas noble que té a sobre a la taula periòdica, el radó.[49] Seguint la tendència periòdica, caldria esperar-se que l'oganessó fos un xic més reactiu que el radó. Tanmateix, els càlculs teòrics han indicat que seria bastant reactiu, de manera que probablement no se'l pot considerar un gas noble.[5] A més de ser molt més reactiu que el radó, l'oganessó pot ser encara més reactiu que els elements 114 i 112.[48] El motiu de l'increment aparent de l'activitat química de l'element 118 en comparació amb el radó és una desestabilització energètica i una expansió radial de l'última subcapa 7p ocupada.[50] Més concretament, les considerables interaccions espín-òrbita entre els electrons 7p amb els electrons 7s² interns porten efectivament a una segona capa de valència que es tanca a l'element 114, i una reducció significativa de l'estabilització de la capa tancada de l'element 118.[50] També s'ha calculat que l'oganessó, a diferència dels altres gasos nobles, s'uneix a un electró, alliberant energia; en altres paraules, té una afinitat electrònica positiva.[51][52][53]
S'espera que l'oganessó tingui una polaritzabilitat molt superior a la de qualsevol dels elements que el precedeixen a la taula periòdica: gairebé el doble que la del radó.[50] Extrapolant sobre la base dels altres gasos nobles, s'espera que l'oganessó tingui un punt d'ebullició entre 320 i 380 K,[50] una xifra molt diferent dels valors estimats prèviament (263 K[6] o 247 K).[54] Fins i tot tenint en compte l'elevat grau d'incertesa d'aquests càlculs, sembla altament improbable que l'oganessó sigui un gas en condicions estàndard.[50] Tenint en compte que l'interval de temperatures en què els altres gasos passen a ser líquids és molt reduït, de només entre 2 i 9 kèlvins, aquest element hauria de ser un sòlid en condicions estàndard. Tanmateix, si l'oganessó formés un gas en condicions estàndard, seria una de les substàncies més denses que són gasoses en aquestes condicions (encara que fos monoatòmic com els altres gasos nobles).
A causa de la seva alta polaritzabilitat, s'espera que l'oganessó tingui una energia d'ionització anormalment baixa (semblant a la del plom, que és un 70% de la del radó[55] i significativament inferior a la de l'element 114)[56] i una fase condensada d'estat estàndard.[57]
Compostos predits
[modifica]
Encara no s'han sintetitzat compostos d'oganessó, però s'han fet càlculs sobre compostos teòrics des del 1964.[31] S'espera que, si l'energia d'ionització d'aquest element és prou alta, serà difícil d'oxidar i, per tant, l'estat d'oxidació més comú serà 0 (com en els altres gasos nobles).[58]
Els càlculs sobre la molècula diatòmica Og₂ indiquen una interacció d'enllaç més o menys equivalent a la que es calcula pel Hg₂, i una energia de dissociació de 6 kJ/mol, aproximadament quatre vegades la del Rn₂. Però el més sorprenent és que s'ha calculat que tindria una longitud d'enllaç 0,16 Å més curta que la del Rn₂, cosa que indicaria una interacció d'enllaç significativa.[50] D'altra banda, el compost OgH+ tindria una energia de dissociació (en altres paraules, l'afinitat protònica del Og) inferior a la del RnH+.
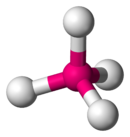
L'enllaç entre l'oganessó i l'hidrogen en el OgH es preveu molt lax i se'l podria considerar una interacció de van der Waals pura en lloc d'un autèntic enllaç químic.[55] D'altra banda, amb els elements molt electronegatius, sembla que l'oganessó formaria compostos més estables que, per exemple, l'element 112 o l'element 114.[55] S'ha predit que existeixen els estats d'oxidació estables +2 i +4 en els fluorurs OgF₂ i OgF₄.[59] Això és un resultat de les mateixes interaccions espín-òrbita que farien que l'oganessó sigui particularment reactiu. Per exemple, es demostrà que la reacció de Og amb F₂ per formar el compost OgF₂ alliberaria una energia de 106 kcal/mol, de les quals aproximadament 46 kcal/mol derivarien d'aquestes interaccions.[55] En comparació, la interacció espín-òrbita de la molècula similar RnF₂ és d'aproximadament 10 kcal/mol sobre una energia de formació de 49 kcal/mol.[55] La mateixa interacció estabilitzaria la configuració tetraèdrica Td del OgF₄, diferent de la configuració planar quadrada D4h del XF₄ i el RnF₄.[59] El més probable és que l'enllaç Og–F sigui iònic i no pas covalent, fent que els compostos de OgFn siguin no volàtils.[5][60] A diferència dels altres gasos nobles, es prediu que l'oganessó és prou electropositiu per formar un enllaç Og–Cl amb el clor.[5]
Com que mai no s'han produït més de quatre àtoms d'oganessó, actualment no té cap ús fora de la investigació científica bàsica. Si mai se n'ajuntés una quantitat suficient en un mateix lloc, representaria un risc radioactiu.[61]
Referències
[modifica]- ↑ 1,0 1,1 1,2 1,3 Nash, 2005, p. 3.493–3.500.
- ↑ 2,0 2,1 «Moskowium». Apsidium.
- ↑ 3,0 3,1 3,2 3,3 Eichler, R.; Eichler, B. Thermochemical Properties of the Elements Rn, 112, 114, and 118. Paul Scherrer Institut.
- ↑ 4,0 4,1 Haire, Richard G. «Transactinides and the future elements». A: Morss, Norman M.; Edelstein; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements. 3a ed.. Dordrecht (Països Baixos): Springer Science+Business Media, 2006, p. 1724. ISBN 1-4020-3555-1.
- ↑ 5,0 5,1 5,2 5,3 5,4 Kaldor, Uzi; Wilson, Stephen. Theoretical Chemistry and Physics of Heavy and Superheavy Elements. Springer, 2003, p. 105. ISBN 140201371X.
- ↑ 6,0 6,1 Seaborg, Glenn Theodore. Modern Alchemy. World Scientific, 1994, p. 172. ISBN 9810214405.
- ↑ Chemical Data. Oganesson - Og, Royal Chemical Society
- ↑ 8,0 8,1 «Oganesson». WebElements Periodic Table.
- ↑ 9,0 9,1 9,2 9,3 9,4 9,5 Oganessian, Iu. Ts.; Utyonkov, V.K.; Lobanov, Yu.V.; Abdullin, F.Sh.; Polyakov, A.N.; Sagaidak, R.N.; Shirokovsky, I.V.; Tsyganov, Yu.S.; Voinov, Yu.S.; Gulbekian, G.G.; Bogomolov, S.L.; B. N. Gikal, A. N. Mezentsev, S. Iliev; Subbotin, V.G.; Sukhov, A.M.; Subotic, K; Zagrebaev, V.I.; Vostokin, G.K.; Itkis, M. G.; Moody, K.J; Patin, J.B.; Shaughnessy, D.A.; Stoyer, M.A.; Stoyer, N.J.; Wilk, P.A.; Kenneally, J.M.; Landrum, J.H.; Wild, J.H.; and Lougheed, R.W. «Synthesis of the isotopes of elements 118 and 116 in the 249Cf and 245Cm+48Ca fusion reactions». Physical Review C, 74, 4, 09-10-2006, pàg. 044602. Bibcode: 2006PhRvC..74d4602O. DOI: 10.1103/PhysRevC.74.044602.
- ↑ «IUPAC Announces the Names of the Elements 113, 115, 117, and 118» (en anglès). IUPAC, 30-11-2016 [Consulta: 1r desembre 2016].
- ↑ Institut d'Estudis Catalans. «La taula periòdica parla català», 19-07-2017. [Consulta: 3 juliol 2020].
- ↑ «The Top 6 Physics Stories of 2006» (en anglès). Discover Magazine, 7 gener 2007. Arxivat de l'original el 12 octubre 2007.
- ↑ 13,0 13,1 Chapman, 2018, p. 796.
- ↑ 14,0 14,1 Smolanczuk, R. «Production mechanism of superheavy nuclei in cold fusion reactions» (en anglès). Physical Review C, 59, 5, 1999, pàg. 2634–2639. DOI: 10.1103/PhysRevC.59.2634.
- ↑ Ninov, Víktor [et al]. «Observation of Superheavy Nuclei Produced in the Reaction of 86Krypton with 208Lead». Physical Review Letters, 83, 1999, pàg. 1104–1107. DOI: 10.1103/PhysRevLett.83.1104.
- ↑ Service, R. F. «Berkeley Crew Bags Element 118». Science, 284, 1999, pàg. 1751. DOI: 10.1126/science.284.5421.1751.
- ↑ Public Affairs Department «Results of element 118 experiment retracted». Berkeley Lab, 21-07-2001 [Consulta: 18 gener 2008].
- ↑ Dalton, Rex «Misconduct: The stars who fell to Earth». Nature, 420, 6.917, 2002, pàg. 728–729. DOI: 10.1038/420728a. PMID: 12490902.
- ↑ Oganessian, I. T. et al. «Results from the first 249Cf+48Ca experiment» (en rus). JINR Communication [JINR, Dubna], 2002.
- ↑ Oganessian, I. T. et al. «Element 118: results from the first 249Californium + 48Calcium experiment». Communication of the Joint Institute for Nuclear Research, 2002. Arxivat de l'original el 2011-07-22. [Consulta: 18 gener 2008].
- ↑ «Livermore scientists team with Russia to discover element 118». Livermore press release, 03-12-2006 [Consulta: 18 gener 2008]. «Còpia arxivada». Arxivat de l'original el 2010-05-27. [Consulta: 15 octubre 2009].
- ↑ Oganessian, I. T. «Synthesis and decay properties of superheavy elements». Pure Appl. Chem., 78, 2006, pàg. 889–904. DOI: 10.1351/pac200678050889.
- ↑ Sanderson, K. «Heaviest element made - again». Nature News. Nature, 2006. DOI: 10.1038/news061016-4.
- ↑ Schewe, P. and Stein, B. «Elements 116 and 118 Are Discovered». Physics News Update. American Institute of Physics, 17-10-2006. Arxivat de l'original el 2013-12-03. [Consulta: 18 gener 2008].
- ↑ Weiss, R. «Scientists Announce Creation of Atomic Element, the Heaviest Yet». Washington Post, 17-10-2006. [Consulta: 18 gener 2008].
- ↑ Barber, Robert C.; Karol, Paul J.; Nakahara, Hiromichi [et al]. «Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)». Pure and Applied Chemistry, 2011, pàg. 1. DOI: 10.1351/PAC-REP-10-05-01.
- ↑ «Element 118 Detected, With Confidence». Chemical and Engineering news, 17-10-2006. [Consulta: 18 gener 2008]. «"Diria que estem molt segurs."»
- ↑ 28,0 28,1 28,2 28,3 Chowdhury, Roy P.; Samanta, C.; Basu, D. N. «
α decay half-lives of new superheavy elements». Phys. Rev. C, 73, 2006, pàg. 014612. DOI: 10.1103/PhysRevC.73.014612. - ↑ Oganessian, I. T. et al. «Measurements of cross sections and decay properties of the isotopes of elements 112, 114, and 116 produced in the fusion reactions 233, 238U, 242Pu, and 248Cm+48Ca». Phys. Rev. C, 70, 2004, pàg. 064609. DOI: 10.1103/PhysRevC.70.064609.
- ↑ Samanta, C.; Chowdhury, R. P.; Basu, D.N. «Predictions of alpha decay half lives of heavy and superheavy elements» (en anglès). Nucl. Phys. A, 789, 2007, pàg. 142–154. DOI: 10.1016/j.nuclphysa.2007.04.001.
- ↑ 31,0 31,1 Grosse, A. V. «Some physical and chemical properties of element 118 (Eka-Em) and element 86 (Em)». Journal of Inorganic and Nuclear Chemistry. Elsevier Science Ltd., 27, 3, 1965, pàg. 509–19. DOI: 10.1016/0022-1902(65)80255-X.
- ↑ Chatt, J. «Recommendations for the Naming of Elements of Atomic Numbers Greater than 100». Pure Appl. Chem., 51, 1979, pàg. 381–384. DOI: 10.1351/pac197951020381.
- ↑ «Discovery of New Elements Makes Front Page News». Berkeley Lab Research Review Summer 1999, 1999. [Consulta: 18 gener 2008].
- ↑ «New chemical elements discovered in Russia's Science City», 12-02-2007. [Consulta: 9 febrer 2008].
- ↑ NewsInfo. «Periodic table has expanded» (en rus). Rambler, 17-10-2006. [Consulta: 18 gener 2008].
- ↑ Yemel'yanova, Asya. «118th element will be named in Russian» (en rus). vesti.ru, 17-12-2006. [Consulta: 18 gener 2008].
- ↑ «Российские физики предложат назвать 116 химический элемент московием» (en rus). rian.ru, 2011. [Consulta: 8 maig 2011].
- ↑ «News: Start of the Name Approval Process for the Elements of Atomic Number 114 and 116» (en anglès). Unió Internacional de Química Pura i Aplicada. Arxivat de l'original el 2 de març 2012. [Consulta: 2 desembre 2011].
- ↑ «IUPAC Is Naming The Four New Elements Nihonium, Moscovium, Tennessine, And Oganesson» (en anglès). IUPAC, 08-06-2016. [Consulta: 8 juny 2016].
- ↑ Considine, Glenn D.; Kulik, Peter H. Van Nostrand's scientific encyclopedia. 9a ed.. Wiley-Interscience, 2002. ISBN 9780471332305. OCLC 223349096.
- ↑ Oganessian, I. T. «Heaviest nuclei from 48Ca-induced reactions». Journal of Physics G: Nuclear and Particle Physics, 34, 2007, pàg. R165–R242. DOI: 10.1088/0954-3899/34/4/R01.
- ↑ «New Element Isolated Only Briefly». The Daily Californian, 18-10-2006. Arxivat de l'original el 8 d’octubre 2008. [Consulta: 18 octubre 2006].
- ↑ Chowdhury, Roy P.; Samanta, C.; Basu, D. N. «Search for long lived heaviest nuclei beyond the valley of stability». Physical Reviews C, 77, 2008, pàg. 044603. DOI: 10.1103/PhysRevC.77.044603.
- ↑ Chowdhury, R. P.; Samanta, C.; Basu, D.N. «Nuclear half-lives for
α -radioactivity of elements with 100 ≤ Z ≤ 130». Atomic Data and Nuclear Data Tables, 94, 6, 2008, pàg. 781–806. arXiv: 0802.4161. Bibcode: 2008ADNDT..94..781C. DOI: 10.1016/j.adt.2008.01.003. - ↑ 45,0 45,1 Royer, G.; Zbiri, K.; Bonilla, C. «Entrance channels and alpha decay half-lives of the heaviest elements». Nuclear Physics A, 730, 2004, pàg. 355–376. DOI: 10.1016/j.nuclphysa.2003.11.010.
- ↑ Duarte, S. B.; Tavares, O. A. P.; Gonçalves, M. [et al]. «Half-life predictions for decay modes of superheavy nuclei». Journal of Physics G: Nuclear and Particle Physics, 30, 2004, pàg. 1487–1494. DOI: 10.1088/0954-3899/30/10/014.
- ↑ Bader, Richard F.W. «An Introduction to the Electronic Structure of Atoms and Molecules». McMaster University. [Consulta: 18 gener 2008].
- ↑ 48,0 48,1 Nash, 2005, p. 3.493.
- ↑ «Ununoctium (Uuo) - Chemical properties, Health and Environmental effects». Lenntech. [Consulta: 18 gener 2008].
- ↑ 50,0 50,1 50,2 50,3 50,4 50,5 Nash, 2005, p. 3.497.
- ↑ Goidenko, Igor; Labzowsky, Leonti; Eliav, Ephraim [et al]. «QED corrections to the binding energy of the eka-radon (Z=118) negative ion». Physical Review A, 67, 2003, pàg. 020102(R). DOI: 10.1103/PhysRevA.67.020102.
- ↑ Eliav, Ephraim; Kaldor, Uzi «Element 118: The First Rare Gas with an Electron Affinity». Physical Review Letters, 77, 27, 1996, pàg. 5350. DOI: 10.1103/PhysRevLett.77.5350.
- ↑ Tanmateix, s'ha demostrat que les correccions electrodinamicoquàntiques són bastant significatives a l'hora de reduir aquesta afinitat (minvant la unió en l'anió Uuo− en un 9%) confirmant així la importància d'aquestes correccions en àtoms superpesants. Vegeu Pyykko
- ↑ Takahashi, N. «Boiling points of the superheavy elements 117 and 118». Journal of Radioanalytical and Nuclear Chemistry, 251, 2, 2002, pàg. 299–301. DOI: 10.1023/A:1014880730282.
- ↑ 55,0 55,1 55,2 55,3 55,4 Han, Young-Kyu; Bae, Cheolbeom; Son, Sang-Kil [et al]. «Spin–orbit effects on the transactinide p-block element monohydrides MH (M=element 113–118)». Journal of Chemical Physics, 112, 6, 2000, pàg. 2684. DOI: 10.1063/1.480842.
- ↑ Nash, Clinton S. «Spin-Orbit Effects, VSEPR Theory, and the Electronic Structures of Heavy and Superheavy Group IVA Hydrides and Group VIIIA Tetrafluorides. A Partial Role Reversal for Elements 114 and 118». Journal of Physical Chemistry A, 1999, 3, 1999, pàg. 402–410. DOI: 10.1021/jp982735k.
- ↑ Nash, 2005, p. 3.499.
- ↑ «Ununoctium: Binary Compounds». WebElements Periodic Table. [Consulta: 18 gener 2008].
- ↑ 59,0 59,1 Han, Young-Kyu; Lee, Yoon Sup «Structures of RgFn (Rg = Xe, Rn, and Element 118. n = 2, 4.) Calculated by Two-component Spin-Orbit Methods. A Spin-Orbit Induced Isomer of (118)F₄». Journal of Physical Chemistry A, 103, 8, 1999, pàg. 1104–1108. DOI: 10.1021/jp983665k.
- ↑ Pitzer, Kenneth S. «Fluorides of radon and element 118». Journal of the Chemical Society, Chemical Communications, 1975, pàg. 760–761. DOI: 10.1039/C3975000760b.
- ↑ «Ununoctium: Biological information». WebElements Periodic Table. [Consulta: 18 gener 2008].
Bibliografia
[modifica]- Chapman, K. «The oganesson odyssey» (en anglès). Nature Chemistry, 10, 2018, pàg. 796. DOI: 10.1038/s41557-018-0098-4.
- Nash, C. S. «Atomic and Molecular Properties of Elements 112, 114, and 118» (en anglès). Journal of Physical Chemistry A, 109, 15, 2005, pàg. 3.493–3.500. DOI: 10.1021/jp050736o. PMID: 16833687.
Enllaços externs
[modifica]- webelements.com - Og (anglès)
- It's Elemental: Ununoctium (anglès)
- On the Claims for Discovery of Elements 110, 111, 112, 114, 116, and 118 (informe tècnic de la IUPAC) (anglès)
| Taula periòdica | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||

