Tellurtrioxid
Tellurtrioxid ist eine chemische Verbindung und das Anhydrid der Orthotellursäure H6TeO6.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
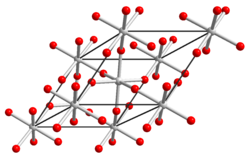
| |||||||||||||||||||
| _ Te6+ _ O2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tellurtrioxid | ||||||||||||||||||
| Andere Namen |
Tellur(VI)-oxid | ||||||||||||||||||
| Verhältnisformel | TeO3 | ||||||||||||||||||
| Kurzbeschreibung |
weißlich bis gelb-orangefarbener Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 175,60 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
5,07 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Eigenschaften
BearbeitenEs ist ein gelber, trigonal/rhomboedrisch kristallisierender Feststoff und existiert in zwei Modifikationen, der röntgenamorphen gelb-orangen
Gewinnung und Darstellung
BearbeitenDie gelb-orange Form entsteht bei der Entwässerung der Orthotellursäure bei ca. 300–320 °C.[6] Die gelbe Farbe kommt durch Elektronenübertrag des Sauerstoffs auf das Tellur („Charge-Transfer“) zustande. Die graue
Einzelnachweise
Bearbeiten- ↑ a b Webelements.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Doktorarbeit RWTH Aachen.
- ↑ M.A.K. Ahmed, H. Fjellvåg, A. Kjekshus: Synthesis, structure and thermal stability of tellurium oxides and oxide sulfate formed from reactions in refluxing sulfuric acid. In: Journal of the Chemical Society, Dalton Transactions, 2000, S. 4542–4549, doi:10.1039/B005688J.
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry, 2nd ed., vol. 1, Academic Press 1963, S. 450–451.