Keratine
Keratin (von griechisch κέρας kéras „Horn“, Genitiv kératos) ist ein Sammelbegriff für verschiedene wasserunlösliche Faserproteine, die von Tieren gebildet werden und die Hornsubstanz charakterisieren. Entsprechend ihrer molekularen Konformation als
Keratine sind der Hauptbestandteil von Säugetierhaaren, Finger- und Zehennägeln, Krallen, Klauen, Hufen, Hörnern, Nasenhörnern der Nashörner, Stacheln der Igel, Barten der Wale, Schnäbeln und Federn der Vögel, Hornschuppen und äußerer Panzerbedeckung der Reptilien. Sie bilden die Intermediärfilamente verschiedener Epithelgewebe, einschließlich der Epidermis, und sorgen unter anderem für mechanische Widerstandsfähigkeit.[1]
Struktur und Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ihre Faserstruktur verstärkt die Festigkeit der Keratine: Die einzelnen Aminosäureketten bilden eine rechtsgängige
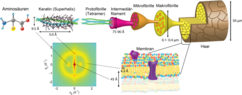
Vor der Verhornung sowie allgemein in Epithelien der Wirbeltiere und anderer Tiergruppen liegen
| A (neutral- basisch) |
B (sauer) |
Vorkommen | Pathologie |
|---|---|---|---|
| KRT1, KRT2 | KRT9, KRT10 | mehrschichtig-verhornendes Epithel (Epidermis) | Ichthyosis hystrix Curth-Macklin; bullöse kongenitale ichthyosiforme Erythrodermie Brocq (EHK); keratosis palmoplantaris striata III; weitere Ichthyosen (BCIE; AEI; CRIE) |
| KRT3 | KRT12 | Hornhaut (Cornea) | Korneale Dystrophie |
| KRT4 | KRT13 | mehrschichtig-unverhorntes Epithel | Naevus spongiosus albus |
| KRT5 | KRT14, KRT15 | Basalzellen komplexer Epithelien sowie Myoepithelzellen | Epidermolysis bullosa simplex; Dowling-Degos-Krankheit; Naegeli-Syndrom |
| KRT6A | KRT16, KRT17 | mehrschichtig-unverhorntes Plattenepithel, Proliferation | Pachyonychia congenita; div. Nävus, Keratoderma |
| KRT7 | KRT19 | einschichtiges Epithel, luminale Drüsenzellen | |
| KRT8 | KRT18, KRT20 | einschichtiges Epithel, luminale Drüsenzellen |

Ein Beispiel für ein

Technische Verwendung
[Bearbeiten | Quelltext bearbeiten]Aus keratinhaltigen Naturstoffen werden L-Cystein, L-Tyrosin und andere proteinogene Aminosäuren im technischen Maßstab hergestellt. Dazu werden die Naturstoffe zuerst mit Salzsäure hydrolysiert. Das Hydrolysat wird mit Ammoniak neutralisiert. Die L-Aminosäuren werden dann aufgrund ihrer unterschiedlichen Löslichkeiten abgetrennt oder nach dem Prinzip der Ionenaustausch-Chromatographie isoliert.[2]
Verwendung finden Keratinprodukte (z. B. Schafwollvliese[3]) beim Abbau von Formaldehyd. Hier hat das deutsche Wollforschungsinstitut an der RWTH Aachen zusammen mit dem eco Institut Köln in langfristiger Forschungsarbeit den Nachweis erbracht, dass solche Produkte in der Lage sind, Formaldehyd aus der Raumluft zu entfernen. Formaldehydbelastete Kindergärten, Schulen und Privathäuser (viele Fertighäuser der 1970er- und 1980er-Jahre) wurden seit den 1990er Jahren auf diese Weise bereits saniert.[4][5]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Justin T. Jacob, Pierre A. Coulombe, Raymond Kwan, M. Bishr Omary: Types I and II Keratin Intermediate Filaments. In: Cold Spring Harbor Perspectives in Biology. Band 10, Nr. 4, 2. April 2018, ISSN 1943-0264, S. a018275, doi:10.1101/cshperspect.a018275, PMID 29610398, PMC 5880164 (freier Volltext).
- ↑ Bernd Hoppe, Jürgen Martens: Aminosäuren – Herstellung und Gewinnung. In: Chemie in unserer Zeit. 1984, Bd. 18, S. 73–86.
- ↑ Schafwolle-Dämmstoffe. Wecobis-Portal des BMI, abgerufen am 4. Dezember 2020.
- ↑ Robert Sweredjuk, Gabriele Wortmann, Gerd Zwiener, Fritz Doppelmayer: Schafwolle als reaktives Sorbens für Luftschadstoffe im Innenraum. (PDF; 201 kB).
- ↑ G. Wortmann, G. Zwiener, R. Sweredjiuk, F. Doppelmayer, F. J. Wortmann: Sorption of indoor air pollutants by sheep’s wool: Formaldehyde as an example. In: Proceedings of the International Wool Textile Organization. Report CTF 3, Florenz, Juni 1999.