Efecto anomérico
En química orgánica, el efecto anomérico o efecto Edward-Lemieux es un efecto estereoelectrónico que describe la tendencia de los sustituyentes heteroatómicos adyacentes a un heteroátomo en un anillo de ciclohexano a preferir la orientación axial en vez de la orientación ecuatorial menos cubierta, que se esperaría a partir de consideraciones estéricas.[1] Este efecto fue observado originalmente en anillos de piranosa por J. T. Edward en 1955; en aquel tiempo, N.-J. Chii y Raymond U. Lemieux comenzaron a estudiar el equilibrio de anomerización de los derivados totalmente acetilados de algunas aldohexopiranosas. El término "efecto anomérico" fue introducido en 1958.[2] El efecto anomérico obtuvo su nombre a partir del término usado para designar el carbono C-1 de una piranosa, el carbono anomérico. Los isómeros que difieren sólo en la configuración del carbono anomérico son denominados anómeros
El efecto anomérico puede ser generalizado a cualquier sistema con la fórmula general R-Y-C-Z, donde Y es un átomo con uno o más pares libres de electrones, y Z es un átomo de alta electronegatividad. La magnitud del efecto anomérico se estima de 1-2 kcal/mol en el caso de los azúcares. En este caso general, la molécula no necesita ser cíclica. Por ejemplo, una molécula pequeña que exhiba el efecto anomérico y suele ser usada para estudios teóricos es el dimetoximetano. En el caso del dimetoxietano, el confórmero gauche tiene una energía 3-5 kcal/mol menor en energía (por tanto, más estable) que la conformación trans: aproximadamente dos veces tan grande como el efecto en los azúcares, porque hay dos enlaces capaces de rotar que son afectados.
Orígenes físicos[editar]
Se han propuesto algunas explicaciones para el efecto anomérico.
La explicación más simple es que la configuración ecuatorial tiene los dipolos de ambos heteroátomos parcialmente alineados, y por tanto repeliéndose mutuamente. En contraste, la configuración axial tiene los dipolos aproximadamente opuesto, representando entonces un estado de menor energía y más estable.

En 1989, los estudios de modelamiento molecular de Box sobre los sacáridos, y el análisis de la información cristalográfica del Cambridge Crystallographic Database usando mecánica molecular basada en el programa STR3DI32, condujeron a un refinamiento de la hipótesis dipolar al mostrar que las repulsiones dipolares originalmente sugeridas, estaban reforzadas por enlaces de hidrógeno C-H···O significativos, estabilizantes, que involucran al grupo funcional acetal.[3] Cálculos de orbitales moleculares más recientes son consistentes con esta hipótesis.[4] Este análisis más comprensivo de los orígenes del efecto anomérico ha llevado también a un mejor entendimiento del efecto anomérico reverso, relacionado al primero e igualmente confuso.[5]
Una explicación alternativa y ampliamente aceptada es que hay una interacción de estabilización (hiperconjugación) entre el par electrónico no compartido de un heteroátomo (
el átomo endocíclico en un anillo de azúcar) y el orbital
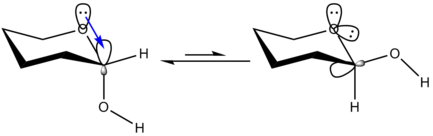
Algunos autores también cuestionan la validez de este modelo, basándose en los resultados de la teoría de los átomos en las moléculas.[6]
Aunque la mayoría de los estudios sobre los efectos anoméricos han sido de naturaleza teórica, la hipótesis n–
Véase también[editar]
Referencias[editar]
- ↑ Unión Internacional de Química Pura y Aplicada (1996). «Anomeric Effect». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Juaristi, E.; Cuevas, G. (1992). «Recent studies of the anomeric effect». Tetrahedron 48: 5019-5087. doi:10.1016/S0040-4020(01)90118-8.
- ↑ Box, V. G. S. (1998). «The anomeric effect of monosaccharides and their derivatives. Insights from the new QVBMM molecular mechanics force field». Heterocycles 48 (11): 2389-2417. doi:10.3987/REV-98-504.
- ↑ Takahashi, O.; Yamasaki, K.; Hohno, Y.; Ohtaki, R.; Ueda, K.; Suezawa, H.; Umezawa, Y.; Nishio, M. (2007). «The anomeric effect revisited. A possible role of the CH/n hydrogen bond». Carbohydr. Res. 342: 1202-1209. doi:10.1016/j.carres.2007.02.032.
- ↑ Box, V. G. S. (2000). «Explorations of the Origins of the Reverse Anomeric Effect of the Monosaccharides using the QVBMM (Molecular Mechanics) Force Field». J. Mol. Struct. 522: 145-164. doi:10.1016/S0022-2860(99)00358-0.
- ↑ Vila, A.; Mosquera, R. A. (2007). «Atoms in molecules interpretation of the anomeric effect in the O—C—O unit». J. Comp. Chem. 28: 1516-1530. doi:10.1002/jcc.20585.
- ↑ Box, V. G. S. (1990). «The role of lone pair interactions in the chemistry of the monosaccharides. The anomeric effect». Heterocycles 31: 1157-1181.
- ↑ Box, V. G. S. (1991). «The role of lone pair interactions in the chemistry of the monosaccharides. Stereo-electronic effects in unsaturated monosaccharides». Heterocycles 32: 795-807. doi:10.3987/REV-91-425.
