B6-vitamiini
| Tätä artikkelia tai sen osaa on pyydetty parannettavaksi, koska se ei täytä Wikipedian laatuvaatimuksia. Voit auttaa Wikipediaa parantamalla artikkelia tai merkitsemällä ongelmat tarkemmin. Lisää tietoa saattaa olla keskustelusivulla. Tarkennus: Artikkeli sisältää hirveästi asiavirheitä. |
B6-vitamiinilla tarkoitetaan erilaisia 5-(hydroksimetyyli)-3-pyridinolin johdannaisia,[1] jotka ovat elämän kannalta välttämättömiä ihmisille ja kaikille muille tunnetuille eliöille. Monet kasvit ja mikrobit tuottavat näitä aineita. Ihmiset tai mitkään muut eläimet taas eivät pysty valmistamaan niitä, joten ne ovat niille vitamiineja ja niiden tulee saada näitä aineita ravinnosta.[2] Märehtijöiden pötsimikrobit tosin usein tuottavat B6-vitamiinia kylliksi eläimen tarpeeseen.[3]
Ihmisillä B6-vitamiinin liian vähäinen saanti on harvinaista, sillä sitä on kylliksi useimmissa ruuissa.[4] B6-vitamiini imeytyy kuitenkin kasvikunnan tuotteista heikommin kuin eläinperäisistä elintarvikkeista. Vegaaniruokavaliota noudattavan saattaa olla tämän vuoksi hyvä käyttää B6-vitamiinilisää. Myös monet lääkeaineet saattavat heikentää B6-vitamiinin imeytymistä.[5]
Suomen valtion ravitsemusneuvottelukunnan saantisuositus on noin 1 milligramma B6-vitamiinia per vuorokausi (mg/vrk).[6] Vitamiinia voi saada liikaa lisäravintoaineista. Lisien useita kuukausia kestävä käyttö noin 500 mg/vrk annoksin[7] voi johtaa muun muassa hermostoperäisiin kipuihin, epätavallisiin tuntemuksiin iholla ja liikkumisvaikeuksiin.[8]
|

|
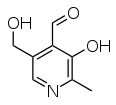
| Pyridoksaali | Pyridoksaali-5'-fosfaatti |

|

|
| Pyridoksiini | Pyridoksamiini |
Luonnosta löytyvät B6-vitamiinina toimivat isomeerit eli vitameerit ovat pyridoksaali (aldehydi), pyridoksiini (alkoholi), pyridoksamiini (amiini) ja näiden 5'-fosfaatit, joissa 5-OH-ryhmään on sitoutunut fosfaatti. Näitä on ruuissa ja syötynä ne muuntuvat ihmiskehossa fosfaatin sitovaksi pyridoksaali-5'-fosfaatiksi eli PLP:ksi. PLP sitoutuu tiettyihin entsyymeihin entsyymitoiminnan kannalta pakollisena osana, joko koentsyyminä tai prosteettisena ryhmänä.[3] Vuonna 2019 eliöissä tunnettiin yli 190 eri entsyymityyppiä, joissa PLP on toiminnallisena osana.[9]
PLP on osallisena ihmisissä esimerkiksi lähes kaikissa aminohappojen hajotuksen ja valmistuksen reaktioreiteissä; glykogeenin vapautumisessa glykogeenifosforylaasilla; serotoniinin tuotossa 5-hydroksitryptofaanista aromaattisten L-aminohappojen dekarboksylaasilla; dopamiinin, ja siten myös norepinefriinin ja epinefriinin esiasteen tuotossa levodopasta aromaattisten L-aminohappojen dekarboksylaasilla; GABA:n tuotossa glutamaattidekarboksylaasilla; hemoglobiinin hemin ja muiden porfyriinien esiasteiden tuotossa 5-aminolevulinaattisyntaasilla;[3] sfingolipidien tuotossa muun muassa sfinganiini-1-fosfaattialdolaasilla.[10]
Suositukset
muokkaaVähimmäissuositus
muokkaa6–65-vuotiaan tulisi joka vuorokausi saada B6-vitamiinia keskimäärin 1 milligramma (mg), jos hänen energiatarpeensa on 2 000 kilokaloria vuorokaudessa. Tämä suositus ja alla olevan taulukon arvot ovat Suomen valtion ravitsemusneuvottelukunnan ravitsemussuosituksia. Neuvottelukunta ei ole määrittänyt sitä, että ovatko B6-suositusten massat (mg) esimerkiksi pyridoksiinina tai jonain muuna B6-vitameerinä.[6]
| Lapset | Miehet | Naiset | Raskaana
olevat | |||
|---|---|---|---|---|---|---|
| Ikä | mg | Ikä | mg | Ikä | mg | 1,4 mg |
| < 6 kk | a | 10–13 v | 1,2 | 10–13 v | 1,1 | |
| 6–11 kk | 0,4 | 14–17 v | 1,6 | 14–17 v | 1,3 | |
| 12–23 kk | 0,5 | 18–30 v | 1,5 | 18–30 v | 1,2 | Imettävät |
| 2–5 v | 0,7 | 31–60 v | 1,5 | 31–60 v | 1,2 | 1,5 mg |
| 6–9 v | 1,0 | 61–74 v | 1,5 | 61–74 v | 1,3 | |
| ≥ 75 v | 1,5 | ≥ 75 v | 1,3 | |||
| a: Äidinmaito tai äidinmaidonkorvike tyydyttää alle 6 kk ikäisten ravinnetarpeet | ||||||
Vuonna 2017 tarkasteltiin 18–74-vuotiaiden suomalaisten ravitsemusta. Tuolloin miehet saivat pyridoksiinia keskimäärin 2,2 milligrammaa vuorokaudessa (mg/vrk) ja 0,25 mg per ruuasta ravintoenergiana saatu megajoule (mg/MJ). Naisilla nämä arvot olivat 1,8 mg/vrk ja 0,25 mg/MJ. Miehistä 84 % sai pyridoksiinia saantisuositusten mukaisesti ja 4 % alle keskimääräisen tarpeen (eli alle 1,3 mg/vrk). Naisilla nämä osuudet olivat vastaavasti 92 % ja 2 % (eli alle 1 mg/vrk). "Keskimääräinen tarve" tyydyttää ravinnetarpeen puolella väestöstä, mutta sitä hieman alhaisempi saanti ei silti välttämättä johda oireilevaan puutostilaan.[11]
Enimmäissuositus
muokkaaB6-vitamiinin turvallisena enimmäismääränä aikuisille pidettiin aiemmin 25:tä milligrammaa per vuorokausi. Nykyisin ylärajana pidetään kuitenkin 12:ta milligrammaa. Tämän rajan ylittäminen saattaa aiheuttaa pitkäaikaisessa käytössä perifeeristä neuropatiaa eli ääreishermostossa havaittavia toimintahäiriöitä tai patologisia muutoksia. Ylärajan ylittäviä ravintolisiä saa myydä edelleen, mutta ne on varustettava merkinnällä, jonka mukaan valmiste ei sovellu pitkäaikaiskäyttöön.[12]
Alla oleva taulukko perustuu vanhentuneeseen riskiarvioon.
| Ikä tai
ihmisryhmä |
1–3 v | 4–6 v | 7–10 v | 11–14 v | 15–17 v | Aikuiset | Raskaana
olevat |
Imettävät |
|---|---|---|---|---|---|---|---|---|
| mg/vrk | 5 | 7 | 10 | 15 | 20 | 25 | 25 | 25 |
Puutos
muokkaaIhmisillä
muokkaaMonet lääkeaineet saattavat aiheuttaa B6-vitamiinin puutetta[5].
B6-vitamiinia on verrattain paljon monissa ruuissa, jonka vuoksi sen puutos on harvinainen tila. Selkeitä puutosoireita ilmenee vasta vakavassa puutoksessa, ja ne loppuvat usein nopeasti saataessa jälleen B6-vitamiinia. Ihmisillä oireita ovat muun muassa heikkous, unettomuus, suupielten halkeilu, kielitulehdus, suutulehdus ja heikentynyt immuunipuolustus.[3] Hermosto-oireita voivat olla ainakin ataksia, ääniherkkyys, kosketusherkkyys, keskittymishäiriöt ja kouristelukohtaukset.[10] Kouristelua ilmenee lähinnä vain vauvoilla.[14]
B6-puutos aiheuttaa myös mikrosyyttistä sideroblastista anemiaa, jossa siis veren punasolujen tilavuus on pienentynyt ja niissä on liikaa hemoglobiinin hemiin sitoutumatonta rautaa. Tämä johtuu siitä, että puutoksessa hemin tuotto vähenee B6-riippuvaisella 5-aminolevulinaattisyntaasilla. Puutos aiheuttaa myös homokysteiinin kertymistä vereen eli homokysteinemiaa, koska B6 on osa kystationi-
B6-puutosta voi ilmetä maksasairauksissa kuten kirroosissa.[14] Tietyt primäärisiä amiiniryhmiä (–NH2) sisältävät lääkkeet, kuten isoniatsidi, sykloseriini ja penisillamiini, liittyvät kovalenttisesti B6:n aktiivisen PLP-muodon karbonyyliin muuntaen PLP:n ei-aktiiviseksi Schiffin emäkseksi. Esimerkiksi isoniatsidin sivuvaikutuksiin kuuluvat siksi ääreishermoston toimintahäiriöt.[10] Maitokorvikkeen voimakas lämpökäsittely sen teollisessa valmistuksessa voi johtaa B6 tuhoutumiseen korvikkeesta. Tämä on aiheuttanut puutosepidemioita vauvoilla esimerkiksi 1950-luvulla USA:ssa.[16][15]
Muilla eläimillä
muokkaaMuilla eläimillä hermosto-oireet ovat hyvin samanlaiset kuin ihmisillä.[10] Jyrsijöillä ilmenee symmetristä hilseilevää ihottumaa (hännässä, käpälissä, kasvoissa ja kurkussa), rasvamaksan kehittymistä, lihasheikkoutta, anemiaa, virtsan oksaattipitoisuuden kasvua, insuliinin erityksen vähentymistä. Muilla eläimillä vaikutukset ovat samantapaisia.[10]
Täysikasvuisilla märehtijöillä pötsin mikrobit tuottavat usein tarpeeksi B6-vitamiinia, joten niillä ei ilmene sen puutosta. Vasikoilla ja muilla vastasyntyneillä märehtijöillä puutos on mahdollinen, sillä niille ei vielä ole kehittynyt sopivaa vitamiinia tuottavaa mikrobikantaa pötsiin. Ne saavat B6-vitamiinia emän maidosta tai sen korvikkeesta.[3]
Liikasaanti
muokkaaYliannostus B6-vitamiinia aiheuttaa hermostollisia ongelmia, jotka ovat osin samanlaisia kuin B6-puutoksessa.[17] Yliannostuksia ei ole ilmennyt ruuasta, vaan tunnetut tapaukset johtuvat B6-lisäravintoaineiden liikakäytöstä.[4] Ihmisillä yliannostuksen oireita voivat olla muun muassa
- parestesia, jota on kuvailtu esimerkiksi polttavaksi, kutisevaksi tai pisteleväksi – voi ilmetä myös tunnottomuutta, joka ilmenee pääosin raajoissa, mutta joskus myös kasvoissa[8]
- "luukivut", jotka ilmenevät pääosin jaloissa, ja joita on kuvailtu pistäviksi tai sähköiskun kaltaisiksi[8]
- lihasheikkous ja kömpelyys[8]
- lihasten nykiminen[8]
- ihorakkulat[7]
- oksentelu[7]
Edeltävät oireet yleensä lakkaavat lopetettaessa lisien liikakäyttö. Myrkytysoireita ilmenee jatkuvassa B6-lisien käytössä kerta-annoksesta johtuvien myrkytysten sijaan.[17] Ihmisillä esimerkiksi yli 2 000 mg/vrk annoksin ensimmäisten oireiden ilmenemisessä saattaa kestää yli vuosi. Vakavien oireiden ilmenemiseen vaaditaan usein vähintään 500 mg/vrk annostelu. Lieviä haittoja on havaittu yksittäistapauksissa myös 50 mg/vrk annoksin, muttei kaikissa tutkimuksissa.[7]
Ei tiedetä varmuudella, miksi suuret annokset B6-vitamiinia ovat myrkyllisiä. Useimmissa lisäravinteissa B6 on pyridoksiinin suoloina ja vitameereistä ainakin se saattaa yliannostuksessa estää kilpailevasti PLP:n toimintaa siitä riippuvaisissa entsyymeissä. Tämä selittäisi miksi B6-puutoksen ja yliannostuksen oireet ovat osin samankaltaiset. Myrkyllisyys taas ilmenisi siten molemmissa tilanteissa osin samoin mekanismein. Erääksi myrkyllisyyden aiheuttajaksi on ehdotettu 3-hydroksikynureniinia (3HK, CAS-numero 484-78-6). 3HK:ta muodostuu hermostossa kun tryptofaani muuntuu nikotiiniamidiksi ns. kynureniini-reitillä (eng. kynurenine pathway). 3HK muuntuu ksanturenaatiksi ja 3-hydroksiantraniliinihapoksi PLP-entsyymeillä. Runsas ylimäärä pyridoksiinia saattaisi estää näiden entsyymien toimintaa. Tällöin hermomyrkyllistä 3HK:ta kertyy hermostoon.[17]
Pyridoksiinin hydrokloridin LD50 on 5,5 g/kg rotille nieltynä ja ihonalaispistoksena 3,7 g/kg. Rotat kuolevat kouristelukohtausten aikana.[18]
Imeytyminen
muokkaaB6-vitamiini esiintyy eläimissä lähinnä pyridoksaalina ja pyridoksamiinina ja kasveissa pyridoksiinina. Valtaosa näistä on fosforyloitunut tai sitoutunut proteiineihin niiden lysiinien
B6-vitamiinia esiintyy myös glykosyloituneissa muodoissa, lähinnä kasveissa. Arviolta vain noin 60 % ihmisen nauttimista glykosideistä imeytyy ruoansulatuksen yhteydessä. Esimerkiksi porkkanoiden B6-vitamiinista jopa 86 % voi olla glykosyloidussa muodossa. Muita runsaasti B6-glykosylaatteja sisältäviä ruokia ovat esimerkiksi parsakaali, keräkaali, kukkakaali, pinaatti, tomaatti, appelsiini,[3] maissi, riisilese, soijapapu, vehnälese ja täysjyvävehnä.[19]
Varastoinnin ja käsittelyn aiheuttama vitamiinihukka
muokkaaJos ruoka kypsennetään keittämällä, osa sen B6-vitamiinista liukenee keitinveteen. Esimerkiksi riisi kannattaa kypsentää tämän vuoksi siten, että keitinvesi imeytyy siihen.[20]
B6-vitamiini on vakaa happamassa, mutta saattaa olla epävakaa emäksisissä ja neutraaleissa oloissa, erityisesti kuumassa tai valoisassa. Kasvien kuumentamisen aiheuttama häviö vaihtelee välillä 0–70 %. Kasviperäinen pyridoksiini on muita vitameerejä vakaampi eri olosuhteissa, joten kuumentaminen johtaa eläinperäisissä ruuissa usein isompaan B6-vitamiinin häviöön. Esimerkiksi maitojauheen valmistus kuumentamalla) voi johtaa 30–70 % häviöön.[3]
Myös ruuan varastoiminen saattaa johtaa häviöihin. Eri ruuissa on havaittu 19–60 % häviö, kun niitä on pidetty 5 kk pakkasessa –18 °C:n lämpötilassa.[21]
Ruokapitoisuudet
muokkaaSiipikarja, naudan- ja sianliha sekä kala sisältävät runsaasti B6-vitamiinia. Sitä esiintyy melko paljon myös täysjyväviljoissa, etenkin rukiissa.[22] Viljojen B6-vitamiini on pääosin niiden alkioissa ja kuoriosissa kuten leseissä, joten raffinointi vähentää jonkin verran viljan B6-vitamiinipitoisuutta[3]. Esimerkiksi valkeassa vehnäjauhossa on 10 prosenttia vähemmän B6-vitamiinia kuin täysjyväjauhoissa[22]. Riisin valkaisu ei kuitenkaan vähennä sen B6-vitamiinipitoisuutta[23][24].
Vegaaniruokavaliota noudattavan saattaa olla hyvä käyttää B6-vitamiinilisäystä, koska kasviperäinen B6-vitamiini imeytyy eläinperäistä huonommin.[5]
| Pavut ja pähkinät | Lihat | ||||
|---|---|---|---|---|---|
| Kaurahiutale | 0,119 | Cashewpähkinä, kuivapaahdettu | 0,256 | Ankka, paahdettu | 0,25 |
| Maissijauho, täysjyvä | 0,37 | Härkäpapu, keitetty | 0,072 | Kalkkuna, iholla, paahdettu | 0,41 |
| Ohraryyni | 0,115 | Kidneypapu, keitetty | 0,12 | Kana, iholla, paahdettu | 0,52 |
| Pasta, täysjyvä, keitetty | 0,079 | Kikherne, keitetty | 0,139 | Kirjolohi (viljelemätön), paistettu | 0,346 |
| Riisi, tumma, keitetty | 0,145 | Linssi, keitetty | 0,178 | Makrilli, kuivattu, (paistettu ennen kuivaamista) | 0,46 |
| Riisi, valkoinen, keitetty | 0,026 | Maapähkinä, kuivapaahdettu | 0,256 | Vasikanmaksa, paistettu[26] | 0,73 |
| Ruisjauho, puolikarkea | 0,268 | Manteli, kuivapaahdettu | 0,074 | Nauta, rasvainen kylki, (25 % rasvaa), pariloitu | 0,27 |
| Soijajauho, rasvainen | 0,351 | Parapähkinä, kuivapaahdettu | 0,251 | Naudanmunuainen, pariloitu[26] | 0,30 |
| Vehnäjauho, täysjyvä | 0,341 | Pekaanipähkinä, kuivapaahdettu | 0,195 | Sika, kinkku, (vähärasvainen), paahdettu | 0,45 |
| Vehnälese | 1,303 | Pistaasi, kuivapaahdettu | 0,255 | Silli, säilyke | 0,17 |
| Vehnänalkio | 1,3 | Voipapu, keitetty | 0,193 | Turska, paistettu | 0,283 |
| Kasvikset ja ruokasienet | Hedelmät ja marjat | Lehmänmaitotuotteet | |||
| Bataatti, kuorimaton, uunipaistettu | 0,241 | Aitoviikuna | 0,113 | Briejuusto | 0,235 |
| Herne | 0,169 | Ananas | 0,087 | Camembertjuusto | 0,227 |
| Jääsalaatti | 0,04 | Appelsiini | 0,06 | Cheddarjuusto | 0,074 |
| Keltasipuli | 0,116 | Aprikoosi | 0,054 | Edamjuusto | 0,076 |
| Keräkaali, keitetty | 0,113 | Avokado | 0,28 | Maito, rasvaton | 0,04 |
| Kukkakaali, keitetty | 0,173 | Banaani | 0,578 | Raejuusto, 1 % rasvaa | 0,068 |
| Kurkku | 0,042 | Hunajameloni | 0,115 | Sinihomejuusto | 0,166 |
| Lanttu | 0,102 | Karviainen | 0,08 | Voi | 0,003 |
| Maissi, keltainen | 0,055 | Luumu | 0,081 | Kerma, 31,3 % rasvaa[26] | 0,03 |
| Parsa, keitetty | 0,01 | Mango | 0,134 | Herajauhe, makea[26] | 0,58 |
| Parsakaali, keitetty | 0,143 | Mansikka | 0,059 | Jugurtti, 3,3 % rasvaa[26] | 0,05 |
| Peruna, kuorimaton, uunipaistettu | 0,301 | Mustaherukka | 0,066 | Muut | |
| Pinaatti | 0,195 | Mustikka | 0,036 | Kananmuna, keitetty | 0,121 |
| Porkkana | 0,147 | Omena | 0,048 | Rintamaito (ihmisen) | 0,011 |
| Punajuuri, keitetty | 0,067 | Persikka | 0,018 | Rypsiöljy | 0 |
| Selleri | 0,087 | Päärynä | 0,018 | Oliiviöljy | 0 |
| Siitake, kuivattu | 0,965 | Vadelma | 0,057 | Olut, lager | 0,05 |
| Tomaatti | 0,08 | Viinirypäle | 0,042 | Leivinhiiva, tuore (puristehiiva)[26] | 0,60 |
| a: ruuat ovat raakoja eli valmistamattomia ellei toisin mainita. Pitoisuudet ovat keskimääräisiä ja annettu pyridoksiinina (ruuissa on useita erimassaisia B6-vitameerejä). | |||||
Teollinen valmistus
muokkaaB6-vitamiinia ei tuoteta teollisesti mikrobeissa, vaan kemiallisella synteesillä.[27] Yleensä teollisesti tuotettu ja lisäravinteissa käytetty B6-vitamiini on pyridoksiinin hydrokloridi (suola). Tämä kestää lämmitystä ja muita olosuhteita paremmin kuin ei-suolamuotoiset B6-vitameerit.[3]
Pyridoksiinia tuotetaan teollisesti lähinnä erilaisin Diels-Alder-reaktioin. Dieeninä on jokin sopiva oksatsoli. Dienofiilinä on esimerkiksi maleiinihappo tai fumaarihappo. DA-reaktion jälkeen tuotetta muokataan eri tavoin, jotta saadaan pyridoksiinia[28]
Toiminta eliöissä
muokkaaB6-vitameerit muuntuvat eliöissä pyridoksaali-5'-fosfaatiksi eli PLP:ksi, joka sitoutuu tiettyihin entsyymeihin näiden toiminnan kannalta välttämättömänä koentsyyminä tai prosteettisena ryhmänä Schiffin emässidoksella. Sidos on PLP:n karbonyylin ja jonkin entsyymin aminohapon primäärisen amiinin välinen.[10] PLP on eliöissä osana esimerkiksi lähes kaikissa aminohappojen hajotuksen ja valmistuksen reaktioreiteissä.[3] Näissä aminohappo-aineenvaihdunnan entsyymeissä emässidoksen amiini on tietyn lysiinin sivuketjun
Yleistäen PLP:n pyridiini on entsyymillä reagoivan aineen eli substraatin elektroneja delokalisoiva rakenne. Se siis madaltaa entsyymin reaktioiden siirtymätilaenergioita tehden reaktioista mahdollisia ja elämälle kyllin nopeita. Substraatti kiinnittyy PLP:hen
PLP on koentsyyminä neljän tyyppisissä reaktioissa:
α -hiilen reaktiot. Nämä voidaan jakaa edelleenα -aminohappojenα -dekarboksylaatioihin.[10] Näissä aminohaposta jää jäljelle primäärinen amiini kun siitä irtoaa karboksyylihappo CO2:na. Eräs esimerkki on ornitiinidekarboksylaasi.[3]- transaminaatioihin.[10] Näissä reaktioissa PLP:n karbonyylin happi ja aminohapon amiini vaihtuvat keskenään. PLP:stä muodostuu pyridoksamiinifosfaatti ja aminohaposta oksohappo. Sitten jonkin toisen oksohapon karbonyylin happi ja pyridoksamiinifosfaatin amiini vaihtuvat keskenään. Muodostuu PLP ja aminohappo.[15] Esim. aspartaattiaminotransferaasi.[3]
α -aminohappojen rasemaatioihin.[10] Näissä aminohaponα -hiili deprotonoituu (H+ irtoaa) kun PLP muodostaa siihen yksöissidoksen sijaan kaksoissidoksen. Aromaattinen PLP muuntuu samalla väliaikaisesti kinoniksi.α -hiili protonoituu jommaltakummalta puolelta, jolloin muodostuu joko L- tai D-aminohappo. Esim. alaniinirasemaasi (EC-numero 5.1.1.1).[15]
α ,β -eliminaatiot. Esim. 5-aminolevulinaattisyntaasi, glysiinihydroksimetyylitransferaasi (EC 2.1.2.1), sfinganiini-1-fosfaattialdolaasi (EC 4.1.2.27).[10]β -hiilen reaktiot. Esim. L-seriiniammonialyaasi (EC 4.3.1.17), kystationi-β -syntaasi (EC 4.2.1.22), tryptofanaasi (EC 4.1.99.1), kynureninaasi.[10]γ -hiilen reaktiot. Esim. homoseriinidehydrogenaasi (EC EC 1.1.1.3) ja kystationi-γ -lyaasi (EC 4.4.1.1).[10]
PLP on myös osana glykogeenifosforylaasia, jossa katalyysiin osallistuva PLP:n ryhmä ei ole karbonyyli edeltävistä entsyymeistä poiketen, vaan 5'-fosfaatti. Poikkeuksellista on myös se, että PLP on prosteettinen ryhmä. Entsyymin ja PLP:n välinen Schiffin emässidos ei siis katkea missään vaiheessa.[15]
Muu biokemia
muokkaaVitameerien muunnos
muokkaaVitameerit voivat muuntua useimmissa eliöissä PLP:ksi. Muuntumiseen osallistuvat usein vähintään pyridoksaalikinaasi (EC-numero 2.7.1.35), pyridoksaali-5'-fosfaattisyntaasi (EC 1.4.3.5) ja pyridoksiini-4-dehydrogenaasi (EC 1.1.1.65).[2]
Kinaasin reaktiot ovat:[29][2]
- pyridoksiini + ATP → pyridoksiini-5'-fosfaatti + ADP
- pyridoksamiini + ATP → pyridoksamiini-5'-fosfaatti + ADP
- pyridoksaali + ATP → PLP + ADP
Syntaasin reaktiot ovat:[30][2]
- pyridoksiini-5'-fosfaatti + O2 → PLP + H2O
- pyridoksamiini-5'-fosfaatti + H2O + O2 → PLP + NH3 + H2O2
Dehydrogenaasin reaktio on:[31][2]
- pyridoksaali + NADPH → pyridoksiini + NADP+
Pyridoksiinin, pyridoksaalin ja pyridoksamiinin 5'-fosfaatit voivat defosforyloitua fosfataaseilla takaisin fosfaatittomiin muotoihinsa.[10] Edeltävät reitit ovat normaalin toiminnan ja selviytymisen kannalta tärkeitä myös useimmille eliöille, jotka pystyvät valmistamaan PLP:tä (katso kohta biosynteesi).[2]
Imeytyminen
muokkaaB6 imeytyy passiivisella diffuusiolla ohutsuolesta. Ruuan proteiineihin sitoutuneet B6-muodot pilkkoutuvat näistä irti entsymaattisesti ja fosfaatteja sitovat muodot defosforyloituvat ennen kuin ne päätyvät ohutsuolen soluihin ja sieltä vereen.[15] B6-vitamiinin imeytyminen ihmisillä ja muilla eläimillä jopa 2–3-kertaa tehokkaampaa kuin sen todellinen tarve.[3]
Kuljetus
muokkaaIhmisillä B6 päätyy suolistosta porttilaskimon kautta maksaan lähinnä fosfaatittomana pyridoksaalina. Maksassa pyridoksaali, pyridoksiini, pyridoksamiini ja näiden fosfaatit hapettuvat ja/tai fosforyloituvat PLP:ksi pyridoksaali-5'-fosfaattisyntaasilla ja pyridoksaalikinaasilla (katso kohta vitameerien muunnos). Pyridoksamiini-5'-fosfaatin muunnosta PLP:ksi katalysoivat syntaasin lisäksi transaminaasit. Maksasta PLP poistuu vereen albumiiniin sitoutuneena, josta se voi siirtyä edelleen punasoluihin tai kehon kudoksiin.[15] Maksan käsittelyprosessi on sama lähes kaikilla muillakin eläimillä.[2]
Ihmisillä veren B6:sta pääosa on PLP:tä, joka on sitoutunut tiukasti proteiineihin Schiffin emässidosten kautta. Nämä muodostuvat PLP:n karbonyylin ja aminohapon jonkin amiinin välille. PLP:n veriplasmapitoisuus on usein alle 1 mM, mutta punasoluissa sitä on noin 6 kertaa tätä enemmän. Punasolupitoisuudet ovat tätäkin isompia vastasyntyneillä, mutta 5-vuotiaaksi mennessä pitoisuudet ovat tasoittuneet samalle tasolle kuin aikuisilla. Punasoluissa PLP on sitoutunut hemoglobiinin
Kehon B6:n kokonaismäärästä alle 0,1 % on plasmassa, jossa se on kiinni albumiinissa Schiffin emässidoksin. Albumiinin B6:sta noin 90 % on PLP:tä.[3] Albumiini suojaa PLP:tä fosfataasien ennenaikaiselta defosforylaatiolta.[2]
Soluihin siirtyäkseen PLP defosforyloituu ensin pyridoksaaliksi alkalisten fosfataasien toimesta. Siirtyminen soluun tapahtuu kantajaproteiinivälitteisesti, mutta ainakaan ihmisten kohdalla tarkempaa proteiinia tai -proteiineja ei tunneta.[2] Pyridoksaali fosforyloituu jälleen kalvon läpäisemättömäksi PLP:ksi useimmissa soluissa olevalla pyridoksaalikinaasilla jääden siten soluun, ja liittyen sitten proteiineihin. Fosfataasien toiminta on kuitenkin useimmissa soluissa suurempaa kuin kinaasien. Siten proteiineihin sitoutumattomat ylimääräiset PLP:t defosforyloituvat ja poistuvat kehosta.[15]
Varastoituminen
muokkaaIhmiskehossa ei ole mitään tarkoituksenmukaista varastointijärjestelmää B6-vitamiinille, vaan se on toiminnollisena osana proteiineissa. Proteiineihin sitoutumaton B6 ylimäärä poistuu kehosta nopeasti.[15] B6-vitamiinia on aikuisella ihmisellä on kehossaan noin 40–150 mg. Tämä riittää 20–75 vrk tarpeisiin. Tästä määrästä 70–80 % on lihaksissa PLP:n muodossa, joka on sitoutunut glykogeenifosforylaasi-entsyymeihin. B6-pitoisuudet ovat suuret myös maksassa, aivoissa, munuaisissa ja haimassa.[3] Fosforylaasipitoisuudet kuitenkin laskevat esimerkiksi nälkiintymisessä, sillä tällöin kehossa on vähän glykogeeniä, eikä sen hajotukselle ole juuri tarvetta. Tällöin fosforylaasien PLP:t siirtyvät muihin kudoksiin, lähinnä maksaan ja munuaisiin.[2]
Hajotus ja erittyminen
muokkaaIhmisillä maksassa noin 40–60 % syödystä B6-vitamiinista defosforyloituu ja hapettuu pyridoksaalikinaasilla (EC-numero 2.7.1.35) tai aldehydidehydrogenaasilla (EC 1.2.1.3) 4-pyridoksiinihapoksi. Tämä erittyy virtsan mukana pois kehosta. Sen vuorokausittainen eritys on 0,5–1,2 mg miehillä ja 0,4–1,1 mg naisilla. Sen pitoisuudet pienevät syötäessä runsaasti aminohappoja ja päinvastoin. Hyvin alhaiset pitoisuudet voivat tarkoittaa sitä, että henkilöllä on B6-puutos.[3]
Virtsassa on muitakin aineenvaihduntatuotteita, mutta pienempiä määriä. Näitä ovat pyridoksaali ja pyridoksamiini sekä niiden fosfaatit. 4-pyridoksiinihapon pitoisuudet vähenevät syötäessä runsaasti aminohappoja ja päinvastoin.[25]
Biosynteesi
muokkaaB6-vitamiinia muodostuu lähes kaikissa kasveissa, sienissä ja bakteereissa,[32] muttei missään eläimissä. Eliöissä tunnetaan kaksi reittiä, DXP-reitti ja DXP-riippumaton-reitti, joiden kautta PLP:tä muodostuu.[2]
DXP-reitillä PLP:tä tuotetaan deoksiksyluloosi-5'-fosfaatista (DXP) ja 4-fosfohydroksi-L-treoniinista. Nämä lähtöaineet muodostuvat eri tavoin eliöstä riippuen. 4-hydroksitreoniini-4-fosfaattidehydrogenaasin (EC-numero 1.1.1.262) reaktio on:[34][2]
- 4-fosfohydroksi-L-treoniini + NAD+ → 3-amino-3-oksopropyylifosfaatti + CO2 + NADH
Pyridoksiini-5'-fosfaattisyntaasin (EC 2.6.99.2) reaktio on:[35][2]
- deoksiksyluloosi-5'-fosfaatti + 3-amino-3-oksopropyylifosfaatti → pyridoksiini-5'-fosfaatti + Pi + 2 H2O
Pyridoksiini-5'-fosfaatti hapettuu PLP:ksi pyridoksaali-5'-fosfaattisyntaasilla (katso kohta vitameerien muunnos).
DXP-riippumattomalla-reitillä PLP:tä muodostuu PDX1- ja PDX2-entsyymien muodostamalla pyridoksaali-5'-fosfaattisyntaasilla (EC 4.3.3.6). Lähtöaineina on ribuloosi-5-fosfaatti, L-glutamiini ja D-glyseraldehydi-3-fosfaatti.[36][2]
Antagonistit
muokkaaB6-vitamiinilla on antagonisteja, jotka estävät sen toimintaa eri tavoin – esimerkiksi ottaen sen paikan entsyymeissä, mutta suorittamatta sen toimintoja. Nämä aineet voivat kehoon päätyessään aiheuttaa B6-puutosta. Esimerkkejä ovat 4'-deoksipyridiini (CAS-numero 148-51-6), isoniatsidi,[3] ginkgotoksiini (CAS 1464-33-1),[37] toksopyrimidiini (CAS 73-67-6)[38] ja gyromitriini tai pikemminkin sen hajoamistuote, metyylihydratsiini.[39]
-
4'-Deoksipyrimidiini
-
Ginkgotoksiini
-
Toksopyrimidiini
Nimet ja historia
muokkaa1934 Paul György (1893–1976) sai rotilla aikaan pellagran kaltaista ihottumaa, jonka hän osoitti johtuvan tuntemattoman B-vitamiinin puutoksesta. Hän nimesi aineen "B6-vitamiiniksi".[40][41] Tuolloin tunnettiin tiamiini (B1) ja riboflaviini (B2). Vitamiinien B3, B4 ja B5 oli myös esitetty olevan olemassa, vaikkakaan niiden olemassaoloa ei oltu osoitettu varmuudella. B6-vitamiinin nimessä siis käytettiin numeroa 6 jottei se mene sekaisin näiden muiden tunnettujen ja ehdotettujen aineiden kanssa.[41]
Puhtaan B6-vitamiinin eristi ensimmäisenä 1938 Samuel Lepkovsky (1899–1984).[42][43] Pian tämän jälkeen samana vuonna aineen eristivät toisistaan riippumattomasti 4 muuta tutkijaryhmää.[41]
1939 Leslie Julius Harris (synt. 1898) ja Karl Folkers (1906–1997) selvittivät pyridoksiinin rakenteen, jonka he olettivat olevan B6-vitamiinin ainoa vitamiinina toimiva rakenne.[44][43] Samana vuonna P. György ja Robert E. Eckardt esittivät nimen "pyridoksiini" olevan sopiva nimitys aineelle muun muassa sen rakenteessa olevan pyridiinin vuoksi.[45][41]
1942 Esmond Emerson Snell (1914–2003) ja kollegat tekivät kasvatuskokeita Enterococcus faecalis -bakteereilla (entinen Streptococcus) havaiten olevan olemassa toistaiseksi tuntematon "pseudopyridoksiini", joka tehosti tuntemattomalla tapaa bakteerien kasvua jopa tuhatkertaisesti.[46][47] 1944 E. Snell esitti tiedejulkaisussa pyridoksiinin muuntuvan E. faecalis kasvatusliuosten autoklavoinnissa aldehydiksi tai amiiniksi, joilla on bakteereille isompi hyötyosuus kuin pyridoksiinilla.[48][47] Samassa tiedejulkaisun numerossa Karl Folkers ja kollegat esittivät pyridoksaalin (aldehydin) ja pyridoksamiinin (amiinin) rakenteet ja synteesit, jotka he olivat selvittäneet E. Snellin pyynnöstä.[49][47]
Lähteet
muokkaa- J Zempleni et al: Handbook of vitamins. (4. painos) Taylor & Francis, 2007. ISBN 9780849340222
- GF Combs et al: The vitamins: fundamental aspects in nutrition and health. (3. painos) Elsevier Academic Press, 2008. ISBN 9780121834937
Viitteet
muokkaa- ↑ Combs, s. 55
- ↑ a b c d e f g h i j k l m n M Parra, S Stahl, H Hellmann: Vitamin B6 and Its Role in Cell Metabolism and Physiology. Cells, 22.7.2018, 7. vsk, nro 7. PubMed:30037155 doi:10.3390/cells7070084 ISSN 2073-4409 Artikkelin verkkoversio.
- ↑ a b c d e f g h i j k l m n o p q r Combs, s. 313–327
- ↑ a b PJ Stover, MS Field: Vitamin B-6. Advances in Nutrition, 7.1.2015, 6. vsk, nro 1, s. 132–133. PubMed:25593152 doi:10.3945/an.113.005207 ISSN 2161-8313 Artikkelin verkkoversio.
- ↑ a b c B6-vitamiini – tärkeimmät lähteet ja saantisuositus | Terveystalo www.terveystalo.com. Viitattu 18.7.2023.
- ↑ a b c Suomalaiset ravitsemussuositukset 2014, s. 49, 51. (5. painos) Valtion ravitsemusneuvottelukunta, 2018. ISBN 9789524538015 Teoksen verkkoversio.
- ↑ a b c d Opinion of the Scientific Committee on Food on the Tolerable Upper Intake Level of Vitamin B6 2000. Euroopan komissio. Viitattu 21.3.2019.
- ↑ a b c d e K Dalton, MJT Dalton: Characteristics of pyridoxine overdose neuropathy syndrome. Acta Neurologica Scandinavica, 1987, 76. vsk, nro 1, s. 8–11. PubMed:3630649 doi:10.1111/j.1600-0404.1987.tb03536.x ISSN 1600-0404 Artikkelin verkkoversio.
- ↑ B6db home bioinformatics.unipr.it. Arkistoitu 27.3.2006. Viitattu 25.3.2019.
- ↑ a b c d e f g h i j k l m n Zempleni, s. 315–322
- ↑ L Valsta et al: Ravitsemus Suomessa - FinRavinto 2017 -tutkimus, s. 100. Terveyden ja hyvinvoinnin laitos, 2018. ISBN 9789523432383 Teoksen verkkoversio.
- ↑ B6-vitamiinin UL-arvo puolittui – korkeita pitoisuuksia sisältäviin ravintolisiin varoitusmerkintä Ruokavirasto. Viitattu 29.11.2023.
- ↑ Overview on Tolerable Upper Intake Levels as derived by the Scientific Committee on Food (SCF) and the EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA) (pdf) EFSA. 2018. Viitattu 6.3.2019.
- ↑ a b Y Tong: Seizures caused by pyridoxine (vitamin B6) deficiency in adults: A case report and literature review. Intractable & Rare Diseases Research, toukokuu 2014, 3. vsk, nro 2, s. 52–56. PubMed:25343127 doi:10.5582/irdr.2014.01005 ISSN 2186-3644 Artikkelin verkkoversio.
- ↑ a b c d e f g h i j k B Caballero et al: Encyclopedia of human nutrition, s. 340–343. Academic Press, 2013. ISBN 9780123848857 Teoksen verkkoversio.
- ↑ EM Nelson: Association of vitamin B6 deficiency with convulsions in infants. Public Health Reports, toukokuu 1956, 71. vsk, nro 5, s. 445–449. PubMed:13323208 ISSN 0094-6214 Artikkelin verkkoversio.
- ↑ a b c MF Vrolijk et al: The vitamin B6 paradox: Supplementation with high concentrations of pyridoxine leads to decreased vitamin B6 function. Toxicology in vitro, lokakuu 2017, 44. vsk, s. 206–212. PubMed:28716455 doi:10.1016/j.tiv.2017.07.009 ISSN 1879-3177 Artikkelin verkkoversio.
- ↑ J Greslin, K Unna: Studies on the Toxicity and Pharmacology of Vitamin B6 (2-Methyl-3-Hydroxy-4,5-Bis-(hydroxymethyl)-Pyridine). Journal of Pharmacology and Experimental Therapeutics, 1.12.1940, 70. vsk, nro 4, s. 400–407. ISSN 0022-3565 Artikkelin verkkoversio.
- ↑ Combs, s. 448
- ↑ Gholamreza Asadikaram, Saam Norouzi, Tahereh Khalili, Moslem Abolhassani, Masoud Torkzadeh-Mahani, Mohammad Reza Hajizadeh, Zakaria Vahabzadeh: Effect of Cooking Procedure on B1, B2, and B6 Vitamins Content and Some Elements in the Main Rice Brands in the Iranian Market. Current Nutrition & Food Science, 12.6.2023, 20. vsk, nro 2, s. 242–249. doi:10.2174/1573401319666230502103931 Artikkelin verkkoversio. (englanniksi)
- ↑ I Vedrina-Dragojević, B Sebecić: Effect of frozen storage on the degree of vitamin B6 degradation in different foods. Zeitschrift Fur Lebensmittel-Untersuchung Und -Forschung, tammikuu 1994, 198. vsk, nro 1, s. 44–46. PubMed:8171918 ISSN 0044-3026
- ↑ a b https://fineli.fi/fineli/fi/ravintotekijat/2276
- ↑ Eat This Much Inc: Eat This Much, your personal diet assistant Eat This Much. Viitattu 10.5.2024. (englanniksi)
- ↑ Brown Rice Nutrition Facts - Eat This Much www.eatthismuch.com. Viitattu 10.5.2024.
- ↑ a b Combs, s. 528–560
- ↑ a b c d e f ME Ensminger et al: The concise encyclopedia of foods & nutrition, s. Ensminger, "Chapter 6 F". CRC Press, 1995. ISBN 9780849344558
- ↑ CG Acevedo-Rocha et al: Microbial cell factories for the sustainable manufacturing of B vitamins. Current Opinion in Biotechnology, 2019, 56. vsk, s. 18–29. PubMed:30138794 doi:10.1016/j.copbio.2018.07.006 Artikkelin verkkoversio.
- ↑ M Eggersdorfer et al: ”Vitamins”, Ullmann's Encyclopedia of Industrial Chemistry, s. 95–99. American Cancer Society, 2000. ISBN 9783527306732 Teoksen verkkoversio.
- ↑ ENZYME entry 2.7.1.35 enzyme.expasy.org.
- ↑ ENZYME entry 1.4.3.5 enzyme.expasy.org.
- ↑ ENZYME entry 1.1.1.65 enzyme.expasy.org.
- ↑ C Wrenger et al: Analysis of the Vitamin B6 Biosynthesis Pathway in the Human Malaria Parasite Plasmodium falciparum. Journal of Biological Chemistry, 18.2.2005, 280. vsk, nro 7, s. 5242–5248. PubMed:15590634 doi:10.1074/jbc.M412475200 ISSN 0021-9258 Artikkelin verkkoversio.
- ↑ TB Fitzpatrick et al: Two independent routes of de novo vitamin B6 biosynthesis: not that different after all. The Biochemical Journal, 1.10.2007, 407. vsk, nro 1, s. 1–13. PubMed:17822383 doi:10.1042/BJ20070765 ISSN 1470-8728 Artikkelin verkkoversio.
- ↑ ENZYME entry 1.1.1.262 enzyme.expasy.org.
- ↑ EC 2.6.99.2 enzyme.expasy.org.
- ↑ ENZYME entry 4.3.3.6 enzyme.expasy.org.
- ↑ H Jang et al: Ginkgotoxin Induced Seizure Caused by Vitamin B6 Deficiency. Journal of Epilepsy Research, 31.12.2015, 5. vsk, nro 2, s. 104–106. PubMed:26819944 doi:10.14581/jer.15018 ISSN 2233-6249 Artikkelin verkkoversio.
- ↑ BG Haughton, HK King: Toxopyrimidine phosphate as an inhibitor of bacterial enzyme systems that require pyridoxal phosphate. Biochemical Journal, joulukuu 1958, 70. vsk, nro 4, s. 660–665. PubMed:13607425 ISSN 0264-6021 Artikkelin verkkoversio.
- ↑ A Wright et al: Amelioration of Toxic Effects of Ethylidene Gyromitrin (false Morel Poison) with Pyridoxine Chloride. Journal of Food Safety, 1981, 3. vsk, nro 3, s. 199–203. doi:10.1111/j.1745-4565.1981.tb00422.x ISSN 1745-4565 Artikkelin verkkoversio. (Arkistoitu – Internet Archive)
- ↑ P György: Vitamin B2 and the Pellagra-like Dermatitis in Rats. Nature, maaliskuu 1934, nro 3361, s. 498–499. doi:10.1038/133498a0 ISSN 1476-4687 Artikkelin verkkoversio.
- ↑ a b c d P György: The History of Vitamin B6. Introductory Remarks. Vitamins & Hormones, 1964, 22. vsk, s. 361–365. PubMed:14284110 doi:10.1016/S0083-6729(08)60343-X ISSN 0083-6729 Artikkelin verkkoversio.
- ↑ S Lepkovsky: Crystalline Factor I. Science, 18.2.1938, 87. vsk, nro 2251, s. 169–170. PubMed:17740355 doi:10.1126/science.87.2251.169 ISSN 0036-8075 Artikkelin verkkoversio.
- ↑ a b IH Rosenberg: A history of the isolation and identification of vitamin B(6). Annals of Nutrition & Metabolism, 2012, 61. vsk, nro 3, s. 236–238. PubMed:23183295 doi:10.1159/000343113 ISSN 1421-9697 Artikkelin verkkoversio.
- ↑ SA Harris, K Folkers: Synthesis of Vitamin B6. Journal of the American Chemical Society, toukokuu 1939, 61. vsk, nro 5, s. 1245–1247. doi:10.1021/ja01874a069 ISSN 0002-7863 Artikkelin verkkoversio.
- ↑ RE Eckardt, P György: Vitamin B6 and Skin Lesions in Rats. Nature, syyskuu 1939, 144. vsk, nro 3646, s. 512. doi:10.1038/144512a0 ISSN 1476-4687 Artikkelin verkkoversio.
- ↑ RJ Williams, BM Guirard, EE Snell: Occurrence in Natural Products of a Physiologically Active Metabolite of Pyridoxine. Journal of Biological Chemistry, 1.4.1942, 143. vsk, nro 2, s. 519–530. ISSN 0021-9258 Artikkelin verkkoversio.
- ↑ a b c RL Hill, RD Simoni, N Kresge: Esmond E. Snell and the B Vitamins. Journal of Biological Chemistry, 1.4.2005, 280. vsk, nro 13, s. e10–e10. ISSN 0021-9258 Artikkelin verkkoversio.
- ↑ EE Snell: The Vitamin Activities of "Pyridoxal" and "Pyridoxamine". Journal of Biological Chemistry, 1.6.1944, 154. vsk, nro 1, s. 313–314. ISSN 0021-9258 Artikkelin verkkoversio.
- ↑ K Folkers, D Heyl, SA Harris: The Structure and Synthesis of Pyridoxamine and Pyridoxal. Journal of Biological Chemistry, 1.6.1944, 154. vsk, nro 1, s. 315–316. ISSN 0021-9258 Artikkelin verkkoversio.
Aiheesta muualla
muokkaa- Fineli: B6-vitamiinin lähteet ruoka-aineissa
- Linus Pauling Institute: Vitamin B6 (englanniksi)
- The Small Molecule Pathway Database (SMPDB): Vitamin B6 Metabolism, Homo sapiens (englanniksi)
- B6 DataBase: tietokanta tunnetuista PLP-entsyymeistä (Arkistoitu – Internet Archive) (englanniksi)
- KEGG: Pyridoxal 5'-phosphate (englanniksi)
- KEGG: Pyridoxal (englanniksi)
- KEGG: Pyridoxine (englanniksi)
- KEGG: Pyridoxamine (englanniksi)