Akoniittihappo
| Akoniittihappo | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
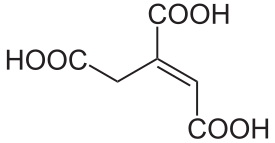
| IUPAC-nimi | Prop-1-eeni-1,2,3-trikarboksyylihappo |
| CAS-numero | |
| PubChem CID | |
| SMILES | C(C(=CC(=O)O)C(=O)O)C(=O)O[1] |
| Ominaisuudet | |
| Molekyylikaava | C6H6O6 |
| Moolimassa | 174,108 g/mol |
| Sulamispiste |
126–129 °C (cis-isomeeri, hajoaa)[2] 198–199 °C (trans-isomeeri)[3] |
| Liukoisuus veteen | 500 g/l (25 °C)[4] |
Akoniittihappo (C6H6O6) on karboksyylihappoihin kuuluva orgaaninen yhdiste, jolla on cis- ja trans-isomeerit. Yhdisteen cis-isomeeria (CAS 585-84-2) esiintyy kaikissa eliöissä osana sitruunahappokiertoa ja trans-akoniittihappoa (CAS 4023-65-8) voidaan käyttää muovien- ja kumien pehmentimien valmistamiseen.
Ominaisuudet ja biologinen rooli
[muokkaa | muokkaa wikitekstiä]Molemmat akoniittihapon isomeerit ovat huoneenlämpötilassa valkoisia kiteisiä aineita, jotka liukenevat hyvin veteen ja etanoliin, mutta eivät juurikaan dietyylieetteriin. Trans-akoniittihappo on hieman cis-isomeeriään stabiilimpi. Kuumennettaessa yhdistettä siitä muodostuu ensin akoniittihapon anhydridi ja edelleen itakonianhydridiä tai sitrakonianhydridiä, jotka voidaan hydrolysoida itakoni- ja sitrakonihapoiksi.[3][5][6][7][8]
Cis-akoniittihappoa esiintyy kaikissa eliöissä sitruunahappokierron osana. Sitä muodostuu välituotteena, kun akonitaasientsyymi isomeroi sitruunahappoa isositruunahapoksi.[7][9][10] Ensimmäisen kerran yhdiste eristettiin vuonna 1820 ukonhatusta (Aconitum napellus). Cis-isomeerin lisäksi trans-isomeeria on eritetty muun muassa ukonhatusta, sokeriruo'osta, juurikkaasta ja kortteista. Niissä se esiintyy magnesium- ja kalsiumsuoloina.[3][7][10]
Valmistus ja käyttö
[muokkaa | muokkaa wikitekstiä]Akoniittihappoa voidaan valmistaa kuumentamalla sitruunahappoa rikkihappo- tai metaanisulfonihappopitoisessa liuoksessa 175 °C:n lämpötilaan. Näin muodostuu pääasiassa trans-akoniittihappoa, mutta myös cis-akoniittihappoa, itakonihappoa, sitrakonihappoa ja asetonidikarboksyylihappoa.[5][6][7]
Akoniittihappoa voidaan käyttää itakonihapon valmistamiseen ja akoniittihaposta saatavia trietyyli- tai tributyyliestereitä käytetään synteettisten muovien ja kumien pehmentiminä.[3][4]
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ cis-Aconitic acid – Substance summary PubChem. NCBI. Viitattu 28.7.2015.
- ↑ W. L. F. Armarego,Christina Chai: Purification of Laboratory Chemicals, s. 95. Butterworth-Heinemann, 2012. ISBN 978-0123821614 Kirja Googlen teoshaussa (viitattu 28.7.2015). (englanniksi)
- ↑ a b c d Susan Budavari (päätoim.): Merck Index, s. 21. (12th Edition) Merck & Co., 1996. ISBN 0911910-12-3 (englanniksi)
- ↑ a b George W. A. Milne: Gardner's commercially important chemicals, s. 11. John Wiley and Sons, 2005. ISBN 978-0-471-73518-2 Kirja Googlen teoshaussa (viitattu 28.7.2015). (englanniksi)
- ↑ a b Rebecca Lopez-Garcia: Citric Acid, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2010. Viitattu 28.7.2015
- ↑ a b Frank H. Verhoff & Hugo Bauweleers: Citric Acid, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2014. Viitattu 28.7.2015
- ↑ a b c d Thomas Scott, Mary Eagleson: Concise encyclopedia chemistry, s. 12. Walter de Gruyter, 1994. ISBN 978-3110114515 Kirja Googlen teoshaussa (viitattu 28.7.2015). (englanniksi)
- ↑ Alexander Apelblat: Citric Acid, s. 222. Springer, 2014. ISBN 978-3-319-11232-9 Kirja Googlen teoshaussa (viitattu 28.7.2015). (englanniksi)
- ↑ Jeremy M. Berg, John L. Tymoczko & Lubert Stryer: Biochemistry, 6th Edition, s. 484. W. H. Freeman and Company, 2006. ISBN 978-0-7167-8724-2 (englanniksi)
- ↑ a b Thomas Scott: Concise encyclopedia biology, s. 12. Walter de Gruyter, 1996. ISBN 978-3110106619 Kirja Googlen teoshaussa (viitattu 28.7.2015). (englanniksi)
Aiheesta muualla
[muokkaa | muokkaa wikitekstiä]- Human Metabolome Database: cis-Aconitic acid (englanniksi)
- Human Metabolome Database: trans-Aconitic acid (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): cis-Aconitic acid (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): trans-Aconitic acid (englanniksi)
- Liber Herbarum II: Luettelo akoniittihappoa sisältävistä kasveista