Fibrinogeeni
| Fibrinogeenin | |
| Tunnisteet | |
| Tietokannat | |
| Entrez | 2243 |
| OMIM | 134820 |
| UniProt | P02671 |
| Fibrinogeenin | |
| Tunnisteet | |
| Tietokannat | |
| Entrez | 2244 |
| OMIM | 134830 |
| UniProt | P02675 |
| Fibrinogeenin | |
| Tunnisteet | |
| Tietokannat | |
| Entrez | 2266 |
| OMIM | 134850 |
| UniProt | P02679 |
Fibrinogeeni on ihmisten ja kaikkien muiden selkärankaisten veressä oleva proteiini. Se on pakollinen osa normaalia veren hyytymistä.[1] Fibrinogeenit pilkkoutuvat trombiinin avulla fibriineiksi, joista verihyytymät pääosin koostuvat. Hyytymissä useat fibriinit ovat yhtyneet suureksi ei-veriliukoiseksi kovalenttiseksi verkostoksi. Hyytymien rakenteeseen osallistuvat tosin myös verihiutaleet.[2]
Ihmisten fibrinogeeni on tankomainen glykoproteiini. Se koostuu kahdesta usein samanlaisesta puolikkaasta, jotka ovat yhtyneet symmetrisesti ja pitkittäin. Kummassakin puolikkaassa on 3 toisiinsa kiertynyttä peptidiketjua:
Geenit
[muokkaa | muokkaa wikitekstiä]Ihmisten fibrinogeenin
FGA-geenin pituus on 7.6 kiloemäsparia (kbp) ja siinä on 6 eksonia. FGB-geenin pituus on 8 kbp ja siinä on 8 eksonia. FGG-geenin pituus on 8.5 kbp ja siinä on 10 eksonia.[4]
Rakenne
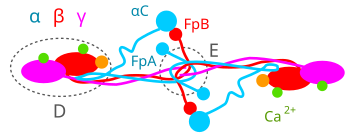
[muokkaa | muokkaa wikitekstiä]Ihmisten fibrinogeeni on noin 45 nanometriä pitkä tankomainen glykoproteiini. Se on heteroheksameeri eli siinä on 6 peptidiketjua, joista osa on keskenään erilaisia. Fibrinogeenissä on 2 puolikasta. Nämä ovat usein keskenään identtisiä ja kukin puolikas koostuu aina 3:sta eri peptidiketjusta:
Vaihtoehtoinen silmukointi tuottaa peptidiketjuille eri muunnelmia. Veren fibrinogeenistä pääosa koostuu A
29 disulfidisidosta pitää fibrinogeeniä koossa. Sen puolikkaat ovat kiinni 5:llä disulfidisidoksella. Puolikkaiden A
Vaihtoehtoinen silmukointi
[muokkaa | muokkaa wikitekstiä]
Silmukointi tuottaa kullekin
1–2 % ihmisveren fibrinogeeneissä molemmat A
Toiminta
[muokkaa | muokkaa wikitekstiä]Tuotto
[muokkaa | muokkaa wikitekstiä]Ihmisillä fibrinogeeni muodostuu pääosin maksassa, joka tuottaa sitä vuorokausittain noin 1.7–5 g. Soluissa fibrinogeenin ketjut päätyvät solulimakalvostoon, jossa ne muun muassa glykosyloidaan ja kootaan fibrinogeeniksi. Soluista ne erittyvät kokonaisina heksameereinä vereen. Suuri osa tosin varastoituu maksasoluihin. Fibrinogeenien puoliintumisaika veriplasmassa on noin 3–5 päivää[7] ja pitoisuus normaalisti 2–4 g/l. Pitoisuus voi vaihdella näistä arvoista merkittävästi ja kohoaa muun muassa tulehduksellisissa sairauksissa.[2]
Hyytymän muodostus
[muokkaa | muokkaa wikitekstiä]
1. Trombiinit (IIa) poistavat FpA:ita, joista jäljelle jääneet A
2. Pian IIa:t poistavat FpB:itä ja
3. Tekijä XIIIa tuottaa verkkosidoksia muun muassa A
Trombiini poistaa nopeimmin A
Hieman pidemmällä aikavälillä trombiini leikkaa B
Edellä muodostuneet fibriinit kasvavat kuiduiksi. Ne alkavat haarautua vapaiden
Hajoaminen
[muokkaa | muokkaa wikitekstiä]Fibriinihyytymän hajoaminen eli fibrinolyysi tapahtuu, jotta verenkierto voi normalisoitua ja vaurioitunut kudos korjautua. Veren plasminogeeni päätyy hyytymään, johon se sitoutuu. Hyytymässä olevat verestä tulleet plasminogeenin kudosaktiaattorit (tPA) pilkkovat plasminogeenin aktiiviseksi plasmiiniksi. tPA:iden toiminta tehostuu eritoten niiden ollessaan kiinni fibriinissä. Ollessaan vapaana veressä tPA:iden entsyymiteho on heikko. Muualla vaurioalueella olevat plasminogeenin urokinaasiaktivaattorit (uPA) pilkkovat plasminogeeniä plasmiiniksi. tPA:n tai uPA:n tuottama plasmiini voi pilkkoa useiden eri lysiinien viereisiä sidoksia fibrinogeenissä.[2]
Sairaudet
[muokkaa | muokkaa wikitekstiä]Jos normaalista poikkeavaa fibrinogeeniä ilmenee veressä, kutsutaan tätä dysfibrinogenemiaksi. Jos veressä ei ole lainkaan fibrinogeeniä, kyse on afibrinogenemiasta. Jos pitoisuudet ovat alhaiset, mutta fibrinogeeniä on veressä, kyse on hypofibrinogemiasta. Edeltävät fibrinogenemiat voivat ilmetä muun muassa maksavaurioiden tai joidenkin syöpien takia. Myös
Afibrinogenemiaa ilmenee
Dysfibrinogenemia periytyy lähinnä autosomaalisesti ja dominantisti. Oireet ja niiden vakavuus riippuu mutaatioista. Noin 10 %:lla sitä potevista ilmenee kohonnut riski saada veritulppa liian tehokkaan hyytymisen takia. Noin 20–25 %:lla ilmenee lisääntynyttä verenvuotoa. Myös keskenmenoriski voi olla kohonnut tautia potevilla naisilla.[4]
Katso myös
[muokkaa | muokkaa wikitekstiä]Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ Y Jiang, RF Doolittle: The evolution of vertebrate blood coagulation as viewed from a comparison of puffer fish and sea squirt genomes. Proceedings of the National Academy of Sciences of the United States of America, 2003, 100. vsk, nro 13, s. 7527–7532. PubMed:12808152. doi:10.1073/pnas.0932632100. ISSN 0027-8424. Artikkelin verkkoversio.
- ↑ a b c d e f g h i j k l On Topaz et al: Cardiovascular Thrombus, s. 31–43. Academic Press, 2018. ISBN 9780128126158.
- ↑ S Spena et al: Congenital afibrinogenaemia caused by uniparental isodisomy of chromosome 4 containing a novel 15-kb deletion involving fibrinogen A
α -chain gene. European Journal of Human Genetics, 2004, 12. vsk, nro 11, s. 891–898. doi:10.1038/sj.ejhg.5201207. ISSN 1476-5438. Artikkelin verkkoversio. - ↑ a b c d GL Tiscia, M Margaglione: Human fibrinogen: molecular and genetic aspects of congenital disorders. International Journal of Molecular Sciences, 2018, 19. vsk, nro 6. PubMed:29844251. doi:10.3390/ijms19061597. ISSN 1422-0067. Artikkelin verkkoversio.
- ↑ MW Mosesson: Fibrinogen and fibrin structure and functions. Journal of Thrombosis and Haemostasis, 2005, 3. vsk, nro 8, s. 1894–1904. doi:10.1111/j.1538-7836.2005.01365.x. ISSN 1538-7836. Artikkelin verkkoversio.
- ↑ AV Cooper, KF Standeven, RA Ariëns: Fibrinogen gamma-chain splice variant gamma' alters fibrin formation and structure. Blood, 2003, 102. vsk, nro 2, s. 535–540. PubMed:12663453. doi:10.1182/blood-2002-10-3150. ISSN 0006-4971. Artikkelin verkkoversio.
- ↑ JW Weisel, RI Litvinov: Fibrin formation, structure and properties. Sub-cellular biochemistry, 2017, 82. vsk, s. 405–456. PubMed:28101869. doi:10.1007/978-3-319-49674-0_13. ISSN 0306-0225. Artikkelin verkkoversio.