« Silicium amorphe » : différence entre les versions
m r2.7.1) (robot Ajoute: nl:Amorf Silicium |
Pld (discuter | contributions) m relecture |
||
| (27 versions intermédiaires par 22 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
{{À sourcer|date=juin 2016}} |
|||
| ⚫ | |||
[[Image:Amorphous Porous Silicon.jpg|vignette|Silicium amorphe poreux vu par [[microscopie électronique en transmission]].|alt=Silicium amorphe poreux vue par [[microscopie électronique en transmission]].]] |
|||
Le '''silicium amorphe''' est |
Le '''silicium amorphe''', généralement abrégé '''a-Si''', est la [[Allotropie|variété allotropique]] non [[cristal]]lisée du [[silicium]], c’est-à-dire dans lequel les [[atome]]s sont désordonnés et ne sont pas rangés de façon régulière définissant une [[structure cristalline]]. |
||
Le silicium amorphe peut être déposé en [[Couche mince|couches minces]] à basse température sur un grand nombre de substrats, permettant d'envisager une grande variété d'applications [[microélectronique]]s. Ce matériau [[semi-conducteur]] est couramment utilisé pour réaliser certains [[Capteur solaire photovoltaïque|panneaux solaires photovoltaïques]]. |
|||
== Description == |
|||
{{Portail|matériaux|Chimie}} |
|||
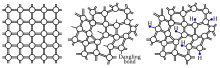
[[Image:A-Si structure-en.svg|vignette|De gauche à droite : structures cristalline, amorphe et amorphe hydrogénée du silicium.|alt=Comparaison entre les structures cristalline, amorphe et amorphe hydrogénée du silicium.]] |
|||
L'atome de silicium est tétravalent, il forme donc quatre [[Liaison covalente|liaisons covalentes]] avec ses voisins. Dans sa forme cristalline, le silicium adopte la [[structure diamant]], comme le carbone et le [[germanium]], formant ainsi un cristal ordonné. |
|||
| ⚫ | |||
| ⚫ | |||
Le silicium amorphe se caractérise par l'absence d'ordre à longue portée : les atomes forment plutôt un réseau aléatoire continu dans lequel certaines liaisons ne sont pas satisfaites ; on parle alors de liaisons "pendantes". Dans un réseau aléatoire continu, la distance interatomique, les angles entre les liaisons covalentes ainsi que les [[Angle dièdre|angles dièdres]] ne sont pas fixes mais suivent plutôt une distribution. Il est possible d'obtenir des informations sur ces distributions en construisant la [[fonction de distribution radiale]] du silicium amorphe à partir des expériences de spectroscopie à [[Rayon X|rayons X]]. |
|||
[[de:Amorphes Silicium]] |
|||
[[en:Amorphous silicon]] |
|||
Les liaisons pendantes sont des [[Défaut cristallin|défauts cristallins]] qui sont notamment responsables de l'altération des propriétés [[électronique (technique)|électronique]]s du matériau. |
|||
[[it:Silicio amorfo]] |
|||
Il est possible de réduire la densité de ces défauts de plusieurs ordres de grandeur en traitant le silicium amorphe à l'[[Dihydrogène|hydrogène]] pour former du silicium amorphe hydrogéné, généralement abrégé '''a-Si:H''', présentant suffisamment peu de défauts résiduels pour pouvoir être utilisé dans des [[Composant électronique|composants électroniques]]. L'hydrogène est cependant une impureté associée à la [[photodégradation]] du silicium par [[effet Staebler–Wronski]]. |
|||
[[ja:アモルファスシリコン]] |
|||
[[nl:Amorf Silicium]] |
|||
== Propriétés == |
|||
[[pl:Krzem amorficzny]] |
|||
La densité du silicium amorphe est de {{unité|4.90 e22|atomes/cm|3}} ({{unité|2.285|g/cm|3}}) à {{unité|300|K}} (calculée à partir de couches minces de {{unité|5| |
|||
[[zh: |
|||
== Silicium amorphe hydrogéné == |
|||
Le silicium amorphe non hydrogéné a une très haute densité de défauts de coordination, ce qui entraîne des propriétés indésirables comme la difficulté de [[Dopage (semi-conducteur)|dopage]], pourtant crucial dans la modulation des propriétés des semi-conducteurs, ou encore une faible [[photoconductivité]]. |
|||
En introduisant de l'hydrogène lors de la fabrication du silicium amorphe, la photoconductivité s'améliore significativement et le dopage devient possible. |
|||
Le silicium amorphe hydrogéné a été fabriqué pour la première fois en 1969 par Chittick, Alexander et Sterling par déposition. Le matériau se caractérisait pas une plus faible densité de défauts et une plus grande conductivité grâce aux impuretés. |
|||
À partir des années 1970, le a-Si:H a été développé en cellules photovoltaïques dont l'efficacité a augmenté jusqu'à 13,6 % en 2015<ref>http://www.nrel.gov/pv/assets/images/efficiency_chart.jpg</ref>. |
|||
== Notes et références == |
|||
{{Références}} |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
Dernière version du 30 mars 2024 à 18:12

Le silicium amorphe, généralement abrégé a-Si, est la variété allotropique non cristallisée du silicium, c’est-à-dire dans lequel les atomes sont désordonnés et ne sont pas rangés de façon régulière définissant une structure cristalline. Le silicium amorphe peut être déposé en couches minces à basse température sur un grand nombre de substrats, permettant d'envisager une grande variété d'applications microélectroniques. Ce matériau semi-conducteur est couramment utilisé pour réaliser certains panneaux solaires photovoltaïques.
Description[modifier | modifier le code]
L'atome de silicium est tétravalent, il forme donc quatre liaisons covalentes avec ses voisins. Dans sa forme cristalline, le silicium adopte la structure diamant, comme le carbone et le germanium, formant ainsi un cristal ordonné.
Le silicium amorphe se caractérise par l'absence d'ordre à longue portée : les atomes forment plutôt un réseau aléatoire continu dans lequel certaines liaisons ne sont pas satisfaites ; on parle alors de liaisons "pendantes". Dans un réseau aléatoire continu, la distance interatomique, les angles entre les liaisons covalentes ainsi que les angles dièdres ne sont pas fixes mais suivent plutôt une distribution. Il est possible d'obtenir des informations sur ces distributions en construisant la fonction de distribution radiale du silicium amorphe à partir des expériences de spectroscopie à rayons X.
Les liaisons pendantes sont des défauts cristallins qui sont notamment responsables de l'altération des propriétés électroniques du matériau. Il est possible de réduire la densité de ces défauts de plusieurs ordres de grandeur en traitant le silicium amorphe à l'hydrogène pour former du silicium amorphe hydrogéné, généralement abrégé a-Si:H, présentant suffisamment peu de défauts résiduels pour pouvoir être utilisé dans des composants électroniques. L'hydrogène est cependant une impureté associée à la photodégradation du silicium par effet Staebler–Wronski.
Propriétés[modifier | modifier le code]
La densité du silicium amorphe est de 4,90 × 1022 atomes/cm3 (2,285 g/cm3) à 300 K (calculée à partir de couches minces de 5
Silicium amorphe hydrogéné[modifier | modifier le code]
Le silicium amorphe non hydrogéné a une très haute densité de défauts de coordination, ce qui entraîne des propriétés indésirables comme la difficulté de dopage, pourtant crucial dans la modulation des propriétés des semi-conducteurs, ou encore une faible photoconductivité. En introduisant de l'hydrogène lors de la fabrication du silicium amorphe, la photoconductivité s'améliore significativement et le dopage devient possible.
Le silicium amorphe hydrogéné a été fabriqué pour la première fois en 1969 par Chittick, Alexander et Sterling par déposition. Le matériau se caractérisait pas une plus faible densité de défauts et une plus grande conductivité grâce aux impuretés. À partir des années 1970, le a-Si:H a été développé en cellules photovoltaïques dont l'efficacité a augmenté jusqu'à 13,6 % en 2015[2].
Notes et références[modifier | modifier le code]
- (en) J. S. Custer, Michael O. Thompson, D. C. Jacobson, J. M. Poate, S. Roorda, W. C. Sinke et F. Spaepen, « Density of amorphous Si », Applied Physics Letters, vol. 64, no 4, , p. 437–439 (ISSN 0003-6951, DOI 10.1063/1.111121, lire en ligne).
- http://www.nrel.gov/pv/assets/images/efficiency_chart.jpg

