Ivabradine
| Ivabradine | |
| |
| Identification | |
|---|---|
| DCI | ivabradine |
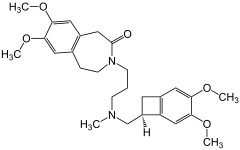
| Nom UICPA | 3-[3-({[(7S)-3,4-diméthoxybicyclo[4.2.0]octa-1,3,5-trièn-7-yl]méthyl}(méthyl)amino)propyl]-7,8-diméthoxy-2,3,4,5-tétrahydro-1H-3-benzazépin-2-one |
| No CAS | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C27H36N2O5 [Isomères] |
| Masse molaire[1] | 468,585 1 ± 0,026 g/mol C 69,21 %, H 7,74 %, N 5,98 %, O 17,07 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | 40 % |
| Liaison protéique | 70 % |
| Métabolisme | premier passage hépatique > 50 %, voie du cytochrome P450 3A4 |
| Demi-vie d’élim. | 2 h |
| Excrétion | |
| Considérations thérapeutiques | |
| Classe thérapeutique | bradycardisant |
| Voie d’administration | per os |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'ivabradine est un médicament bradycardisant indiqué dans l'insuffisance cardiaque ou coronaire.
Pharmacocinétique
[modifier | modifier le code]Sa demi-vie est courte, exigeant une prise deux fois par jour. L'ivabradine est métabolisée par le cytochrome CYP3A4, avec les interactions médicamenteuses en conséquence[2].
Indication
[modifier | modifier le code]L’ivabradine possède deux indications :
- dans la maladie coronaire, l’ivabradine traite les symptômes chez l’adulte coronarien en rythme sinusal. Elle est indiquée chez l’adulte ne pouvant être traité par bêtabloquants (intolérance ou contre-indication) et chez ceux insuffisamment contrôlés par les bêtabloquants, en association avec ces derniers, mais seulement pour ceux dont la fréquence cardiaque au repos est au-dessus de 60 par minute ;
- par ailleurs, l’ivabradine traite l’insuffisance cardiaque chronique chez les patients en rythme sinusal, dont la fréquence cardiaque est supérieure ou égale à 75 battements par minute au repos. Elle peut être prescrite en association avec des traitements conventionnels type bêtabloquants, ou chez les patients contre-indiqués ou intolérants pour ces traitements.
Mode d'action
[modifier | modifier le code]L'ivabradine réduit la fréquence cardiaque en inhibant de manière spécifique le courant If[3] intervenant dans l'automaticité de la dépolarisation au niveau du nœud sinusal, ce dernier étant le responsable du rythme cardiaque[4]. Par ce biais, elle ralentit la fréquence cardiaque en augmentant le temps diastolique que met le canal HCN4 à induire une dépolarisation.
L'ivabradine n’a pas d’effet sur les temps de conduction intra-auriculaires, auriculo-ventriculaires ou intra-ventriculaires, sur la contractilité myocardique, et sur la repolarisation ventriculaire.
Effets cliniques
[modifier | modifier le code]Dans la maladie coronarienne
[modifier | modifier le code]L’efficacité, ainsi que la sécurité d’emploi de l’ivabradine ont été étudiées dans plusieurs études. Sur les symptômes, en cas d'angor stable, la molécule est d'une efficacité comparable à celle de l'aténolol, un bêtabloquant[5] ou à celle de l'amlodipine[6], un inhibiteur calcique. L'ajout de l'ivabradine à un bêtabloquant augmente l'efficacité de ce dernier[7].
Toutefois, en l'absence d'insuffisance cardiaque, ce médicament n'a pas démontré de diminution de la mortalité ou de la morbidité cardiovasculaire[8].
Dans l'insuffisance cardiaque
[modifier | modifier le code]Le , la Société européenne de cardiologie a intégré l'ivabradine dans la prise en charge de l'insuffisance cardiaque chronique, en vue de réduire le risque d'hospitalisation chez les patients ayant une fraction d'éjection inférieure à 35 % et une fréquence cardiaque supérieure à 70 battements par minute[9].
Dans l’étude Shift, (3 241 patients traités par ivabradine), une réduction significative de 18 % de la mortalité cardiovasculaire et des hospitalisations pour insuffisances cardiaques a été démontrée en addition avec les bêtabloquants[10]. Cet effet n’est pas retrouvé dans l’étude Beautiful[11], qui soutient toutefois la sécurité d’emploi sur le plan de la mortalité cardiovasculaire. La qualité de vie semble également améliorée[12].Certains[2] critiquent cependant le résultat de l'étude Shift, soulignant, en particulier, que les patients n'étaient pas traités de manière optimale avant la randomisation (peu de resynchronisation cardiaque, bêtabloquants sous-utilisés...). En 2014, la publication des résultats négatifs de l'étude Signify[13], visant à évaluer l'intérêt de l'ivabradine à plus fortes doses que celles préconisées, chez des patients coronariens avec une fraction d'éjection normale, a montré une augmentation modérée mais significative du risque combiné de décès cardiovasculaire et d’infarctus du myocarde dans le sous-groupe des patients présentant un angor symptomatique. L'ANSM (Agence nationale de sécurité du médicament et des produits de santé) a alors lancé une réévaluation du rapport bénéfices/risques de cette molécule (vendue sous le nom de Procoralan en France)[14].
Le , l'Agence européenne des médicaments publie un communiqué confirmant l’aspect positif du rapport bénéfices/risques de cette molécule[15], tout en précisant les nouvelles conditions de prescription de ce médicament, notamment la dose maximale qui ne doit pas dépasser 7,5 mg deux fois par jour.
Malgré tout, le communiqué de l'Agence européenne des médicaments n'a pas interrompu les critiques[16],[17].
Dans l'insuffisance cardiaque à fonction systolique conservée, les résultats sont mitigés[18].
Effets indésirables
[modifier | modifier le code]L’ensemble des études conduites sur l’ivabradine a permis d’identifier les effets indésirables de cette molécule chez près de 14,000 patients. Les effets décrits les plus fréquemment sont les céphalées, les sensations de vertige, une vision trouble, une bradycardie. Plus souvent (14,5 %), les patients rapportent des phosphènes (d’intensité légère à modérée), généralement provoqués par des brusques variations d’intensité lumineuse. S’ils apparaissent communément au début du traitement, la majorité disparaît en cours de traitement (77,5 %). Ces phosphènes seraient dus à la présence, dans les cellules rétiniennes, de canaux proches des canaux If cardiaques[19]. Ces événements n’impactent que modérément les habitudes de vie des patients dont seulement 1 % d’entre eux déclarent avoir dû adapter leurs habitudes de vie quotidienne.
Controverse
[modifier | modifier le code]La revue Prescrire célèbre pour avoir dénoncé la dangerosité du médiator[20] a publié plusieurs articles dénonçant le rapport risque défavorable du Procoralan[21],[22].
Aspects commerciaux
[modifier | modifier le code]Cette molécule est commercialisée par les laboratoires Servier sous les dénominations commerciales de Procoralan (partout dans le monde), Coralan (à Hong Kong, Singapour, en Australie), Corlentor (en Arménie, Espagne, Italie et en Roumanie) et Coraxan (en Russie et Serbie). Elle est également commercialisée en Inde sous les noms commerciaux d'Ivabid et de Bradia. Au cours de son développement, l'ivabradine a été connue sous le nom de S-16257.
Le , Amgen a acquis les droits d'exploitation commerciale de l'ivabradine aux États-Unis, dans l'insuffisance cardiaque et dans l'angine de poitrine[23]. Le , la FDA a autorisé l'évaluation prioritaire de l'ivabradine dans l'insuffisance cardiaque [24]. En , la FDA identifiait des signaux d'effets indésirables graves pour l'ivabradine : Potential Signals of Serious Risks/New Safety Information Identified by the FDA Adverse Event Reporting System (FAERS) April - June 2016
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Psotka MA, Teerlink JR, Ivabradine: Role in the chronic heart failure armamentarium, Circulation, 2016;133:2066-2075
- (en) P. Bois, J. Bescond, B. Renaudon et J. Lenfant, « Mode of action of bradycardic agent, S 16257, on ionic currents of rabbit sinoatrial node cells », British Journal of Pharmacology, vol. 118, , p. 1051–1057 (ISSN 0007-1188, PMID 8799581, PMCID 1909508, lire en ligne, consulté le )
- (en) DiFrancesco D. « The role of the funny current in pacemaker activity » Circ Res. 2010;106:434-446.
- (en) Jean-Claude Tardif, Ian Ford, Michal Tendera, Martial G. Bourassa, Kim Fox, Efficacy of ivabradine, a new selective If inhibitor, compared with atenolol in patients with chronic stable angina, EHJ, 2005;26;23;2529–2536 (consulté le 20 mars 2018)
- (en) Ruzyllo W, Tendera M, Ford I, Fox KM, Antianginal efficacy and safety of ivabradine compared with amlodipine in patients with stable effort angina pectoris: a 3-month randomised, double-blind, multicentre, noninferiority trial, Drugs, 2007;67:393–405 (consulté le 20 mars 2018)
- (en) Jean-Claude Tardif, Piotr Ponikowski, Thomas Kahan, Efficacy of the If current inhibitor ivabradine in patients with chronic stable angina receiving beta-blocker therapy: a 4-month, randomized, placebo-controlled trial, EHJ, 2009;30;5;540–548 (consulté le 20 mars 2018)
- (en) Fox K, Ford I, Steg PG et al. Ivabradine in stable coronary artery disease without clinical heart failure, N Engl J Med, 2014;371:1091–1099
- (en) « What’s new in the 2012 heart failure guidelines » sur escardio.org/congresses/esc-2012
- (en) Swedberg K, Komajda M, Böhm M. et al. pour le groupe d'investigateurs Shift « Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study » Lancet 2010;376:875-885
- (en) Fox K, Ford I, Steg PG, Tendera M, Ferrari R, pour le groupe d'investigateurs Beautiful « Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a randomised, double-blind, placebo-controlled trial » Lancet 2008;372:807-816
- (en) Ekman I, Chassany O, Komajda M. et al. « Heart rate reduction with ivabradine and health related quality of life in patients with chronic heart failure: results from the SHIFT study » Eur Heart J. 2011;32:2395-2404
- (en) Fox K, Ford I, Steg PG, Tardif JC, Tendera M, Ferrari R, « Ivabradine in stable coronary artery disease without clinical heart failure » N Engl J Med. 2014;371:1091-1099
- « Procoralan (ivabradine) : réévaluation européenne du rapport bénéfice/risque à la suite de nouvelles données de sécurité - Point d'Information » [1]
- (en) « European Medicines Agency recommends measures to reduce risk of heart problems with Corlentor/Procoralan (ivabradine) » [2]
- Revue Prescrire 2014 - Angor : l'ivabradine (Procoralan) augmente le risque d'accidents cardiovasculaires Ivabradine et patients coronariens : accidents cardiovasculaires augmentés Rev Prescrire 2014 ; 34 (373) : 827. (pdf, réservé aux abonnés)
- A propos de l'Ivabradine sur le blog du Dr Jean-Marie Vailloud : Cardiologue titulaire du Diplôme d’université. Interprétation et lecture critique des essais thérapeutiques
- (en) Kosmala W, Holland DJ, Rojek A, Wright L, Przewlocka-Kosmala M, Marwick TH, Effect of If-channel inhibition on hemodynamic status and exercise tolerance in heart failure with preserved ejection fraction: a randomized trial, J Am Coll Cardiol, 2013;62:1330–1338
- (en) Cervetto L, Demontis GC, Gargini C, Cellular mechanisms underlying the pharmacological induction of phosphenes, Br J Pharmacol, 2007;150:383–390
- « "La fille de Brest" : un témoignage exceptionnel », sur prescrire.org, (consulté le )
- « Angor : l'ivabradine (Procoralan°) augmente le risque d'accidents cardiovasculaires », sur www.prescrire.org, (consulté le )
- « Angor et insuffisance cardiaque : l'ivabradine à écarter », sur www.prescrire.org, (consulté le )
- (en) « Amgen buys US rights to Servier’s Procoralan », [3]
- (en) « FDA Grants Amgen Priority Review Designation For Ivabradine For The Treatment Of Chronic Heart Failure » [4]
