beta-Sitosterol
 | |
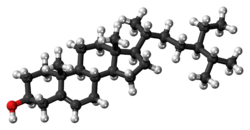 | |
Estigmast-5-en-3 | |
Outros nomes 22,23-Dihidroestigmasterol, | |
| Identificadores | |
| Número CAS | 83-46-5 |
| PubChem | 222284 |
| ChemSpider | 192962 |
| UNII | S347WMO6M4 |
| ChEBI | CHEBI:27693 |
| ChEMBL | CHEMBL221542 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C29H50O |
| Masa molar | 414,71 g mol−1 |
| Punto de fusión | 136–140 °C; 277–284 °F; 409–413 K |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O
Distribución natural e en alimentos
[editar | editar a fonte]O
Investigación en humanos
[editar | editar a fonte]O
Trastorno xenético
[editar | editar a fonte]Aínda que os esterois vexetais son xeralmente beneficiosos, existe un raro trastorno xenetico autosómico, a fitosterolemia, que causa unha sobreabsorción de fitosterois.[5]
Precursor do esteroide anabólico boldenona
[editar | editar a fonte]O
Química
[editar | editar a fonte]Enxeñaría química
[editar | editar a fonte]O uso de sitosterol como intermediario químico estivo durante moitos anos limitado debido á que carecía dun punto químico por onde atacar a súa cadea lateral, o que permitiría eliminar dita cadea. Despois de amplos esforzos realizados por moitos laboratorios conseguiuse finalmente descubrir un microbio do grupo das pseudomonas que podía efectuar eficientemente esta transformación. A fermentación dixire toda a cadea lateral alifática no carbono 17 rendendo unha mestura de produtos 17-ceto incluíndo a deshidroepiandrosterona.[9]
Síntese
[editar | editar a fonte]Non se conseguiu aínda a síntese total de
O primeiro paso da síntese é formar tosilato de estigmasterol (2) a partir de estigmasterol (1) (95% de pureza) usando p-TsCl, DMAP, e piridina (rendemento do 90%). O tosilato (2) sofre despois solvólise ao ser tratado con piridina e MeOH anhidro para dar unha proporción de 5:1 de i-estigmasterol metil éter (3, cun 74% de rendemento) respecto a estigmasterol metil éter (4), que é seguidamente retirado por cromatografía. O paso de hidroxenación dunha síntese previamente proposta comprende o uso do catalizador Pd/C e o solvente etil acetato. Porén, debido á isomerización durante a hidrólise, foron tamén probados outros catalizadores, como o PtO2, e solventes, como o etanol. Observáronse poucos cambios co uso dun catalizador diferente. Porén, o etanol impedía a isomerización e a formación de impurezas non identificadas para dar o composto 5. O último paso da síntese é a desprotección do dobre enlace do anel
Biosíntese
[editar | editar a fonte]
A regulación da biosíntese de esterois e algúns lípidos específicos ocorre durante a bioxénese de membranas.[11] Por medio de padróns de etiquetado 13C, determinouse que na formación de
A biosíntese de cicloartenol empeza cando unha molécula de isopentenil difosfato (IPP) e dúas moléculas de dimetilalil difosfato (DMAPP) forman farnesil difosfato (FPP). Dúas moléculas de FPP únense despois cola con cola rendendo escualeno, un triterpeno. O escualeno, por medio dunha reacción de ciclación co 2,3-oxidoescualeno 6 como intermediario forma cicloartenol.
O dobre enlace do cicloartenol (composto 7 no diagrama) é metilado polo encima SAM para dar lugar a un carbocatión que sofre un cambio de hidruro e perde un protón para render un composto cunha cadea lateral metileno. Ambos os pasos son catalizados pola esterol C-24 metiltransferase (paso E1 do diagrama). O composto 8 é despois catalizado pola esterol C-4 desmetilase (E2) e perde un grupo metilo para producir cicloeucalenol (9). Seguidamente, o anel ciclopropano abre e a cicloeucalenol cicloisomerase (E3) forma o 10. O composto 10 perde un grupo metilo e sofre unha isomerización alílica orixinando gramisterol (11). Este paso é catalizado pola esterol C-14 desmetilase (E4), a esterol
Notas
[editar | editar a fonte]- ↑ "Nutrition data: Foods highest in beta-sitosterol per 200 calorie serving". Conde Nast, USDA National Nutrient Database, version SR-21. 2014. Consultado o 25 de setembro de 2015.
- ↑ Wilt, T; Ishani, A; MacDonald, R; Stark, G; Mulrow, C; Lau, J (2000). "Beta-sitosterols for benign prostatic hyperplasia". The Cochrane Database of Systematic Reviews 2011 (2): CD001043. PMC 8407049. PMID 10796740. doi:10.1002/14651858.CD001043.
- ↑ Kim, T. H.; Lim, H. J.; Kim, M. S.; Lee, M. S. (2012). "Dietary supplements for benign prostatic hyperplasia: An overview of systematic reviews". Maturitas 73 (3): 180–5. PMID 22883375. doi:10.1016/j.maturitas.2012.07.007.
- ↑ Rudkowska I, AbuMweis SS, Nicolle C, Jones PJ (2008). "Cholesterol-lowering efficacy of plant sterols in low-fat yogurt consumed as a snack or with a meal". J Am Coll Nutr 27 (5): 588–95. PMID 18845709. doi:10.1080/07315724.2008.10719742.
- ↑ Patel Manoj D.; Thompson Paul D. (2006). "Phytosterols and Vascular Disease". Atherosclerosis 186 (1): 12–19. PMID 16325823. doi:10.1016/j.atherosclerosis.2005.10.026.
- ↑ G. Gallina; G. Ferretti; R. Merlanti; C. Civitareale; F. Capolongo; R. Draisci; C. Montesissa (2007). "Boldenone, Boldione, and Milk Replacers in the Diet of Veal Calves: The Effects of Phytosterol Content on the Urinary Excretion of Boldenone Metabolites". J. Agric. Food Chem. 55 (20): 8275–8283. PMID 17844992. doi:10.1021/jf071097c.
- ↑ Ros MM, Sterk SS, Verhagen H, Stalenhoef AF, de Jong N (2007). "Phytosterol consumption and the anabolic steroid boldenone in humans: a hypothesis piloted" (PDF). Food Addit. Contam. 24 (7): 679–84. PMID 17613052. doi:10.1080/02652030701216727.
- ↑ R. Draisci; R. Merlanti; G. Ferretti; L. Fantozzi; C. Ferranti; F. Capolongo; S. Segato; C. Montesissa (2007). "Excretion profile of boldenone in urine of veal calves fed two different milk replacers". Analytica Chimica Acta 586 (1–2): 171–176. PMID 17386709. doi:10.1016/j.aca.2007.01.026.
- ↑ Lenz, G. R.; Kirk-Othmer Encyclopedia of Chemical Technology, 3rd ed., Wiley Interscience, Londres, 1983, Vol. 21, 645.
- ↑ McCarthy, FO; Chopra, J; Ford, A; Hogan, SA; Kerry, JP; O'Brien, NM; Ryan, E; Maguire, AR (2005). "Synthesis, isolation and characterisation of beta-sitosterol and beta-sitosterol oxide derivatives". Organic & Biomolecular Chemistry 3 (16): 3059–65. PMID 16186940. doi:10.1039/b505069c.
- ↑ Hartmann, Marie-Andrée (2003). "5 Sterol metabolism and functions in higher plants". Lipid Metabolism and Membrane Biogenesis. Topics in Current Genetics 6. pp. 183–211. ISBN 978-3-540-20752-8. doi:10.1007/978-3-540-40999-1_6.
- ↑ De-Eknamkul W.; Potduang B. (2003). "Biosynthesis of
β -Sitosterol and Stigmasterol in Croton sublyratus Proceeds Via a Mixed Origin of Isoprene Units". Phytochemistry 62 (3): 389–398. PMID 12620352. doi:10.1016/S0031-9422(02)00555-1. - ↑ Dewick, P. M. Medicinal Natural Products: A Biosynthetic Approach. 3 ed.; John Wiley & Sons Ltd.: United Kingdom cyclization, 2009; p 539.

