Timah(II) oksida
| |

| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Timah(II) oksida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| SnO | |
| Massa molar | 134.709 g/mol |
| Penampilan | bubuk hitam atau merah jika sebagai anhidrat, putih jika dihidratkan |
| Densitas | 6.45 g/cm3 |
| Titik lebur | 1.080 °C (1.980 °F; 1.350 K)[1] |
| Tidak dapat larut | |
| −19.0·10−6 cm3/mol | |
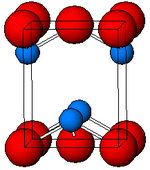
| Struktur | |
| tetragonal | |
| Termokimia | |
| Entropi molar standar (S |
56 J·mol−1·K−1[2] |
| Entalpi pembentukan standar ( |
−285 kJ·mol−1[2] |
| Bahaya | |
| Lembar data keselamatan | ICSC 0956 |
| Titik nyala | Tidak mudah terbakar |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
Tidak ada[3] |
REL (yang direkomendasikan)
|
TWA 2 mg/m3[3] |
IDLH (langsung berbahaya)
|
N.D.[3] |
| Senyawa terkait | |
Anion lain
|
Timah sulfida Timah selenida Timah telurida |
Kation lainnya
|
Karbon monoksida Silikon monoksida Germanium(II) oksida Timbal(II) oksida |
Related
|
Timah dioksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Timah(II) oksida adalah suatu senyawa dengan rumus kimia SnO. Senyawa ini terdiri dari timah dan oksigen dan dalam senyawa ini timah memiliki bilangan oksidasi +2. Terdapat dua bentuk timah(II) oksida, yaitu bentuk yang berwarna biru-hitam dan stsabil, dan bentuk yang berwarna merah dan metastabil.
Persiapan dan reaksi
[sunting | sunting sumber]SnO biru-hitam dapat dihasilkan dengan memanaskan hidrat timah(II) oksida, SnO·xH2O (x<1) yang mengalami pengendapan ketika garam timah(II) direaksikan dengan alkali hidroksida seperti NaOH.[4]
SnO merah yang metastabil dapat disiapkan dengan memanaskan endapan yang dihasilkan dari efek amonia cair pada garam timah(II).[4]
SnO dapat disiapkan sebagai substansi murni di laboratorium dengan memanaskan timah(II) oksalat tanpa adanya udara atau di atmosfer CO2. Metode ini juga diaplikasikan untuk memproduksi besi oksida dan mangan oksida.[5][6]
- SnC2O4·2H2O → SnO + CO2 + CO + 2 H2O
Timah(II) oksida terbakar di udara dengan api hijau yang redup dan membentuk SnO2.[4]
- 2 SnO + O2 → 2 SnO2
Saat dipanaskan di atmosfer yang lembam, awalnya disproporsionasi terjadi dan menghasilkan logam Sn dan Sn3O4 yang kemudian bereaksi menjadi SnO2 dan logam Sn.[4]
- 4SnO → Sn3O4 + Sn
- Sn3O4 → 2SnO2 + Sn
SnO bersifat amfoterik: senyawa ini larut di asam kuat dan menghasilkan garam timah(II), sementara di dalam basa kuat dapat menghasilkan stanit yang mengandung Sn(OH)3−.[4] Senyawa ini dapat dilarutkan di dalam asam kuat untuk menghasilkan kompleks ion Sn(OH2)32+ dan Sn(OH)(OH2)2+, dan di dalam larutan yang kurang asam untuk menghasilkan Sn3(OH)42+.[4] Perlu diingat bahwa stanit anhidrat (seperti K2Sn2O3, K2SnO2) juga diketahui keberadaannya.[7][8][9]
Referensi
[sunting | sunting sumber]- ^ Tin and Inorganic Tin Compounds: Concise International Chemical Assessment Document 65, (2005), World Health Organization
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. hlm. A23. ISBN 0-618-94690-X.
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0615". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c d e f Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0-12-352651-5
- ^ Satya Prakash (2000),Advanced Inorganic Chemistry: V. 1, S. Chand, ISBN 81-219-0263-0
- ^ Arthur Sutcliffe (1930) Practical Chemistry for Advanced Students (1949 Ed.), John Murray - London.
- ^ The First Oxostannate(II): K2Sn2O3, M Braun, R. Hoppe, Angewandte Chemie International Edition in English, 17, 6, 449 - 450, DOI:10.1002/anie.197804491
- ^ Über Oxostannate(II). III. K2Sn2O3, Rb2Sn2O3 und Cs2Sn2O3 - ein Vergleich, R. M. Braun, R. Hoppe, Zeitschrift für anorganische und allgemeine Chemie, 485, 1, 15 - 22, DOI:10.1002/zaac.19824850103
- ^ R M Braun R Hoppe Z. Naturforsch. (1982), 37B, 688-694
