Elettroforesi delle sieroproteine
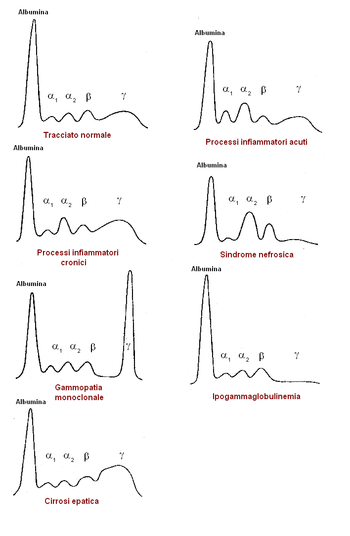
In chimica e in medicina, l'elettroforesi proteica è un metodo d'analisi delle proteine presenti nel sangue e nel siero. È un metodo di separazione di particelle cariche elettricamente, che avviene attraverso elettroforesi, cioè tramite il passaggio continuo di corrente elettrica in una soluzione.
Strumentazione
[modifica | modifica wikitesto]L'attrezzatura necessaria per eseguire una separazione elettroforetica è costituita da:
- una camera umida per ETF: vaschetta di alluminio di plastica divisa da un setto in due scompartimenti in ognuno dei quali viene posto il tampone. In ogni compartimento pesca un elettrodo costituito da un filo di platino e i due elettrodi sono collegati ai rispettivi poli di un alimentatore.
- delle strisce elettroforetiche: rappresentano il supporto solido e poroso per la migrazione. Possono essere di varia natura (amido, agar, carta) a seconda del grado di risoluzione che si deve ottenere. Il gel di acetato di cellulosa è il supporto di più largo impiego per la sua capacità multifrazionativa, per la sua economicità e conservabilità (in metanolo al 30% si conserva per un tempo indeterminato).
- dei ponti: sono supporti in plastica su cui vengono stese e fissate le strisce in modo tale che le estremità siano immerse nel tampone, che salendo per capillarità, potrà distribuirsi su tutta la striscia.
- un applicatore: ha la funzione di depositare una piccolissima quantità di siero sotto forma di sottile striscia rettilinea e perpendicolare alla striscia elettroforetica. Sono disponibili in commercio diversi tipi di applicatori, singoli o multipli, in grado di depositare quantità costanti e consentire una buona standardizzazione del metodo.
- un alimentatore: converte le corrente di rete (alternata) in corrente continua stabilizzata. Esso fornisce una differenza di potenziale costante e consente all'operatore di scegliere la tensione di corrente desiderata.
- un densitometro: spettrofotometro in grado di misurare la trasmissione della luce attraverso una striscia colorata anziché attraverso una soluzione contenuta in una cuvetta. La striscia viene posta su un apposito carrello trasportatore ad avanzamento micrometrico, che avanza a velocità costante di fronte al fototubo in modo che lo spettrofotometro possa leggere le diverse strisce. Il densitometro dà le percentuali delle diverse frazioni proteiche su un display digitale; se è collegato a un registratore si ottiene un grafico avente in ordinata i valori dell'assorbanza e in ascissa la posizione delle bande. Il densitometro è stato oramai sostituito dal computer, che mediante un programma specifico effettua la lettura della striscia elettroforetica e ne elabora poi il grafico.
Questo tipo di analisi viene svolta utilizzando vari tipi di supporto, in particolare con acetato gelatinizzato e il gel d'agarosio. Ultimamente viene sempre più usata l'elettroforesi su capillari direttamente da provetta primaria, a vantaggio della preparazione del campione e della velocità di analisi.
Procedimento
[modifica | modifica wikitesto]Le particelle cariche migrano verso l'elettrodo di carica opposta con una velocità di migrazione o mobilità elettroforetica legata a numerosi fattori dipendenti dalla natura del mezzo e dal campo elettrico applicato e soprattutto dalla massa, dalle dimensioni, dalla carica e dalla forma delle varie particelle. Nell'elettroforesi le proteine reagiscono come molecole elettricamente cariche in soluzione acida o alcalina: esse sono infatti polimeri di amminoacidi, e quindi presentano dei gruppi carbossilici e gruppi amminici. In base al pH della soluzione tampone, dove scorre la corrente, possono essere indotte cariche negative o positive. In particolare in una soluzione alcalina il gruppo carbossilico della molecola viene neutralizzato secondo la reazione:
-COOH + OH- → -COO- + H2O
formando ioni negativi che lasceranno nella proteina una netta carica negativa. In una soluzione leggermente acida, invece, il gruppo amminico associa un protone come si nota nella reazione:
-NH2 + H+ → -NH3+
formando così ioni -NH3+ e quindi lasciando sulla molecola una carica nettamente positiva.
Volendo effettuare una siero-elettroforesi si impiega un tampone a pH alcalino il quale conferisce alle molecole proteiche una carica negativa rendendole solubili senza sottoporle a denaturazione.
Interpretazione
[modifica | modifica wikitesto]Esistono due classi principali nelle sieroproteine: albumina e globuline.
Albumina
[modifica | modifica wikitesto]Solitamente albumina e globuline sono in proporzioni simili, ma l'albumina è molto più corta, e carica negativamente mostrando una concentrazione visiva maggiore. Esiste inoltre una piccola banda superiore all'albumina chiamata pre-albumina.
Globuline
[modifica | modifica wikitesto]Le globuline sono classificate a seconda delle bande relative:
- zona alfa (
α ) o delle alfaglobuline è suddivisa in due bande:- alfa1 - alfa1-antitripsina, alfa1- glicoproteina acida, alfa1-antichimotripsina, alfa1-lipoproteina (HDL), alfa-fetoproteina.
- alfa2 - aptoglobina, alfa2-macroglobulina, alfa2-antiplasmina, ceruloplasmina, colinesterasi, globulina GC (legante Vit.D).
- zona beta (
β ) o delle betaglobuline è suddivisa in due bande:- beta1 - transferrina, lipoproteine a bassa densità (LDL)
- beta2 - complemento C3, beta2-microglobulina, emopessina, fibrinogeno (talvolta in zona gamma, ma in elettroforesi di solito si usa il siero, quindi senza fibrinogeno)
- zona gamma (
γ ) o delle gammaglobuline: immunoglobuline IgA (porzione sx della curva gamma), IgD, IgE, IgG (porzione a dx della curva gamma e IgM (porzione centrale della curva gamma); paraproteine. Le bande monoclonali appaiono solitamente in questa zona.
Valori normali
[modifica | modifica wikitesto]Nella donna
[modifica | modifica wikitesto]| Albumina | 55,0 - 68,0 % |
| alfa1-antitripsina | 1,5 - 5,0 % |
| alfa-acroglobulina | 6,0 - 12,5 % |
| Aptoglobina | 0,34 - 2,00 % |
| Transferrina | 2,0 - 3,8 % |
| Complemento C3 | 0,75 - 1,40 % |
| Immunoglobulina G | 6,9 - 14,0 % |
| Immunoglobulina A | 0,88 - 4,10 % |
| Immunoglobulina M | 0,34 - 2,10 % |
Nell'uomo
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Elettroforesi delle sieroproteine
Wikimedia Commons contiene immagini o altri file su Elettroforesi delle sieroproteine
Collegamenti esterni
[modifica | modifica wikitesto]- Elettroforesi delle proteine del siero, su biessea.com. URL consultato il 27 febbraio 2011 (archiviato dall'url originale il 17 marzo 2011).
