Nitrone

In chimica organica i nitroni[1] sono una classe di derivati azotati del carbonile come le immine e le ossime. In particolare, i nitroni sono N-ossidi di immine.[2] Sono caratterizzati dalla presenza del gruppo funzionale >C=N(R)+–O– (dove R ≠ H)[3][4] e sono quindi composti schematizzabili come R1R2C=N(R3)+–O– oppure anche, evidenziando alternativamente il legame dativo, R1R2C=N(R3)→O.[5] In ogni caso sono composti organici di azoto formalmente pentavalente,[6] come accade per i nitroderivati, i sali di ammonio quaternario, di nitronio e di ossoammonio, i nitrilossidi[7] (RC≡N+−O−) e per gli ammino ossidi.
Come per il caso dei composti carbonilici, che possono essere aldeidi e chetoni, i nitroni possono essere distinti in «aldonitroni» (se almeno uno tra R1 e R2 è un H) e «chetonitroni» (se R1 e R2 sono entrambi alchili o arili).[8]
I nitroni, che nel gruppo funzionale hanno l'atomo di azoto con carica formale positiva e ibridato sp2, sono una classe intermedia tra gli ossidi di ammine terziarie (N+ sp3) e i nitrilossidi (N+ sp).
I nitroni non vanno confusi con i nitreni (R–:N:), che sono specie analoghe ai carbeni e ad essi isoelettronici.[9]
Etimologia
[modifica | modifica wikitesto]Il nome «nitrone» naque dalla contrazione di nitrogen ketone ("chetone all'azoto"), dal suggerimento del chimico tedesco Paul Pfeiffer nel 1916,[10] motivato dalla somiglianza del gruppo >C=N+<, con quello dei chetoni >C=O, somiglianza che attualmente viene riconosciuta, dato che l'atomo di azoto positivo e disostituito è isoelettronico all'ossigeno ed anche per avere questi due gruppi lo stesso tipo di risonanza: la coppia elettronica del legame pi greco che si sposta sull'atomo più elettronegativo, lasciando un carbonio elettrofilo.[11]
Proprietà
[modifica | modifica wikitesto]I nitroni sono composti notevolmente polari e in condizioni ambiente generalmente si presentano come liquidi o solidi, per lo più solubili in acqua a meno che i sostituenti siano a catena lunga o ingombranti. Pertanto, l'estrazione con solventi organici da soluzioni acquose di nitroni a corta catena è in genere possibile solo con previa saturazione con sale della soluzione stessa.[12]
Stereoisomeria
[modifica | modifica wikitesto]Le reciproche posizioni dei gruppi R1 e R2 rispetto a all'atomo di ossigeno e a R3 non sono equivalenti se R1 ≠ R2. Questo comporta in generale la possibilità di avere diastereoisomeri (E) e (Z); gli aldonitroni, ad esempio, hanno isomeri geometrici cis e trans, anche se le barriere energetiche per l'interconversione tra le due forme sono modeste rispetto a quelle degli alcheni: a temperatura ambiente, salvo per la presenza di sostituenti particolarmente ingombranti, le due forme sono in equilibrio:[13]
- (E) ⇄ (Z)
dove una forma è di norma prevalente sull'altra. Per gli aldonitroni in molti casi la forma prevalente è quella Z.[14]
Struttura molecolare
[modifica | modifica wikitesto]La molecola dei nitroni è un ibrido di risonanza per il quale sono prevedibili 3 forme limite:[15]
- >C+−N(R)–O– ←→ >C=N+(R)–O– ←→ >C––N+(R)=O
La prima forma limite è analoga a quella che è sempre presente nella risonanza eterovalente nei composti carbonilici:[11][16]
- >C=O ←→ >C+–O–
qui ha però un peso leggermente maggiore che nel carbonile perché non comporta la creazione di una nuova separazione di carica nel frammento;[17] la seconda è quella che più da vicino rappresenta la molecola reale, visto che il legame tra C e N ha sostanzialmente lunghezza vicina a quella del legame doppio (poco maggiore); la terza ha un peso limitato nell'ibrido di risonanza per la sfavorevole dislocazione delle cariche rispetto alle elettronegatività di C e O, ma contribuisce ad alleviare la carica positiva su C, che tuttavia è sostanziale, e ad aumentare l'ordine di legame tra N e O e quindi ad accorciarlo;[17] tuttavia, pur avendo scarso peso per lo stato fondamentale della molecola, può averne di più allo stato eccitato che è coinvolto negli atti reattivi della molecola stessa.[15]
In ogni caso, gli estremi (C e O) vengono ad avere cariche parziali opposte, positive su C e negative su O; il fatto che le corrispondenti cariche formali siano collegate tramite risonanza qualifica i nitroni come composti 1,3-dipolari e si comportano, in effetti, da tipici reagenti che danno le cicloaddizioni 1,3-dipolari.[18] In accordo con questo, i nitroni sono composti molto polari: in molti casi i loro momenti dipolari cadono nell'intervallo 3,37÷3,47 D.[19]
Da strutture allo stato solido ricavate tramite diffrazione ai raggi X per il nitrone p-Cl−C6H4−CH=N+(CH3)−O−, considerato rappresentativo,[19] si riscontra che il legame C=N (doppio in una sola forma limite) è più lungo che nella corrispondente O-metilossima isomera[20] (130,9 pm contro 126,0 pm) e che il legame +N−O− (doppio in una forma limite) è considerevolmente più corto che nella corrispondente sin-ossima (128,4 pm contro 140,8 pm), dove esso è singolo.[19] Questo legame N−O, qui con N ibridato sp2 e quindi con maggior carattere s, è anche più corto di quello presente nell'N-ossido di trimetilammina (137,8 pm), dove N è ibridato sp3.[21]
Sintesi
[modifica | modifica wikitesto]Un approccio alla sintesi dei nitroni consiste nella condensazione di un'idrossilammina N-alchilata (o arilata) con un carbonile (aldeide o chetone), con eliminazione di una molecola di acqua e formazione del doppio legame C=N.[4] La reazione con aldeidi è spesso piuttosto facile, tanto che in molti casi basta poco più che il semplice mescolamento, mentre quella con i chetoni di struttura paragonabile un po' meno, come generalmente ci si può attendere dalla diversa reattività di aldeidi e chetoni.[22]

Il meccanismo è una variante di quello che porta alle ossime nel caso di idrossilammine non alchilate. La reazione avviene essenzialmente in due stadi: 1) attacco nucleofilo del doppietto libero dell'azoto sull'atomo di carbonio del carbonile, con formazione dell'intermedio tetraedrico e 2) eliminazione acido-catalizzata di acqua con formazione del doppio legame C=N:[23]
- R1R2C=O + :NH(R3)−OH → [ R1R2C(OH)−N(R3)+–OH ] → R1R2C=N(R3)+–O– + H2O
Un ambiente molto acido tende a inibire il primo stadio, dato che in tal caso aumenta la proporzione di atomi di azoto dell'idrossilammina si protonano; d'altro canto, un ambiente poco acido non riesce a catalizzare sufficientemente l'eliminazione di acqua nel secondo stadio. Risulta quindi preferibile condurre queste reazioni a un pH acido intermedio, approssimativamente nell'intervallo 3 - 5.[23]
Un'altra via per l'ottenimento di nitroni consiste nella ossidazione di idrossilammine acicliche o cicliche aventi l'azoto disostituito (R, Ar), purché abbiano almeno un atomo H presente sul C unito a N. Si tratta di una deidrogenazione (un H tolto al carbonio e un altro all'ossigeno) con conseguente formazione del doppio legame C=N, il che costituisce anche un'ossidazione del carbonio (il suo numero di ossidazione aumenta di due unità, quello dell'ossigeno resta invariato):[24]
- >CH–N(R3)−OH (-H2) → >C=N(R3)+–O–
Si possono usare diversi agenti ossidanti: in alcuni casi è sufficiente l'ossigeno dell'aria gorgogliata nella soluzione dell'idrossilammina in presenza del complesso cupro-ammoniacale come catalizzatore; altri agenti ossidanti, a volte più efficienti, sono l'ossido di mercurio (HgO),[25] l'acqua ossigenata, il permanganato di potassio (KMnO4), il ferricianuro di potassio (K3Fe(CN)6) e l'idroperossido di t-butile.[24] I metodi basati sulla condensazione del carbonile evitano i problemi di selettività posizionale associati con l'ossidazione delle idrossilammine contenenti due serie di idrogeni alfa.[26]

I nitroni possono essere anche sintetizzati per ossidazione, in particolari condizioni, di immine sostituite sull'azoto (N-alchil- o N-arilimmine) con permanganato di potassio, acido m-cloroperbenzoico, o dimetildiossirano:[27][28]
R1R2C=NR3 + [O] → R1R2C=N(R3)+–O–
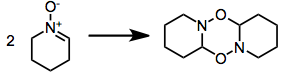
Un problema che affligge molti nitroni reattivi è la dimerizzazione per mutua cicloaddizione 1,3-dipolare.[29] Sperimentalmente si può alleviare questo problema impiegando un eccesso di nitrone oppure aumentando la temperatura di reazione per accentuare il peso del termine entropico (T
Reazioni
[modifica | modifica wikitesto]Cicloaddizioni 1,3-dipolari
[modifica | modifica wikitesto]I nitroni sono 1,3-dipoli e come tali reagiscono con vari dipolarofili,[30] in particolare alcheni e alchini, dando cicloaddizioni 1,3-dipolari e formando in ogni caso un eterociclo a cinque termini: isossazolidine o isossazoline, rispettivamente.[31]
Con gli alcheni la cicloaddizione 1,3-dipolare per formare isossazolidine è strettamente cis-selettiva verso l'olefina.[32] L'anello dell'isossazolidina così formata può poi essere scisso mediante idrogenazione catalitica (idrogenolisi del legame N−O) per dare
Con gli alchini la stessa reazione fornisce isossazoline. Queste, per bromurazione con N-bromosuccinimmide e successivo trattamento con una base, eliminano facilmente acido bromidrico aromatizzandosi a isossazoli.[34]
Nella reazione dei nitroni con gli alchini terminali (R−C≡C-H) , ma in presenza di ioduro di rame(I), la formazione dell'intermedio isossazolinico prosegue con una trasposizione (migrazione di O da N a C) per formare

Sono note anche altre reazioni dei nitroni,[38] ad esempio le cicloaddizioni [3+3] per formare cicli a sei termini, e le cicloaddizioni [2+2+3] per formare cicli a sette termini.[32]
Addizioni nucleofile di reattivi di Grignard e affini
[modifica | modifica wikitesto]I nitroni, analogamente a chetoni e aldeidi, subiscono facilmente l'attacco di nucleofili organometallici (Grignard, alchillitio, etc.) per dare alchilazione sul carbonio alfa all'atomo di azoto; si opera a basse temperature (-40 ° ÷ -60°C) in solventi eterei; la successiva idrolisi in ambiente acido porta ad idrossilammine. La reazione generale è schematizzabile come segue:[39][40]
R−MgBr + RaRbC=N(Rc)+−O– → RRaRbC−N(Rc)−O−MgBr
RRaRbC−N(Rc)−O−MgBr + HX → RRaRbC−N(Rc)–OH + XMgBr
Con reattivi organolitio si opera a temperature più basse, tipicamente a -78 °C, ma lo schema è analogo.
Deossigenazione riduttiva
[modifica | modifica wikitesto]I nitroni possono essere deossigenati alle corrispondenti immine per trattamento con zinco metallico in polvere in etanolo a caldo, in presenza di ioduro rameoso:[41]
RaRbC=N(Rc)+−O– (+ Zn, CuI in EtOH) → RaRbC=N(Rc)
Note
[modifica | modifica wikitesto]- ^ (EN) Jan Hamer e Anthony Macaluso, Nitrones, in Chemical Reviews, vol. 64, n. 4, 1º agosto 1964, pp. 473–495, DOI:10.1021/cr60230a006. URL consultato il 6 settembre 2023.
- ^ McNaught e Wilkinson 2006
- ^ Se su N ci fosse H, esso migrerebbe facilmente come H+ su O–, dando la corrispondente ossima, tautomero parecchio più stabile del nitrone. Pertanto, si formano per lo più come intermedi di reazione.
- ^ a b F. Carey, R. Sundberg, N. Warren e S. Wothers, Organic Chemistry, Oxford University Press, 2001, pp. 932-933, ISBN 0-19-850346-6.
- ^ Michael B. Smith e Jerry March, March's advanced organic chemistry: reactions, mechanisms, and structure, Eighth edition, Wiley, 2020, p. 1030, ISBN 978-1-119-37180-9.
- ^ (EN) B. V. Nekrasov, Pentavalent nitrogen, in Bulletin of the Academy of Sciences of the USSR, Division of chemical science, vol. 28, n. 9, 1º settembre 1979, pp. 1789–1790, DOI:10.1007/BF00952448. URL consultato l'11 settembre 2023.
- ^ R. Fusco, G. Bianchetti e V. Rosnati, 5.5. Fattori che influenzano le cicloaddizioni 1,3-dipolari, in CHIMICA ORGANICA, volume secondo, L. G. Guadagni, 1975, pp. 477-479.
- ^ R. Fusco, G. Bianchetti e V. Rosnati, CHIMICA ORGANICA, volume primo, L. G. Guadagni, 1974, pp. 151-152.
- ^ Internet Archive, Nitrenes, New York, Interscience Publishers, 1970, ISBN 978-0-471-55710-4. URL consultato il 6 settembre 2023.
- ^ Paul Pfeiffer, Lichtchemische Synthese von Indolderivaten (PDF), in Justus Liebigs Annalen der Chemie, vol. 411, n. 1, 1916, pp. 72-158.
- ^ a b (EN) G. R. Delpierre e M. Lamchen, Nitrones, in Quarterly Reviews, Chemical Society, vol. 19, n. 4, 1º gennaio 1965, pp. 329–348, DOI:10.1039/QR9651900329. URL consultato l'8 settembre 2023.
- ^ (EN) G. R. Delpierre e M. Lamchen, Nitrones, in Quarterly Reviews, Chemical Society, vol. 19, n. 4, 1º gennaio 1965, pp. 335-336, DOI:10.1039/QR9651900329. URL consultato l'11 settembre 2023.
- ^ Eli Breuer, Hans Günter Aurich e Arnold Nielsen, The chemistry of functional groups: a series of advanced treatises. 2: Nitrones, nitronates and nitroxides / by Eli Breuer; Hans Günter Aurich; Arnold Nielsen, collana An Interscience publication, Wiley, 1989, pp. 149-151, ISBN 978-0-471-91709-0.
- ^ Mary Eagleson, Concise encyclopedia chemistry, W. de Gruyter, 1994, p. 151, ISBN 978-3-11-011451-5.
- ^ a b Eli Breuer, Hans Günter Aurich e Arnold Nielsen, The chemistry of functional groups: a series of advanced treatises. 2: Nitrones, nitronates and nitroxides / by Eli Breuer; Hans Günter Aurich; Arnold Nielsen, collana An Interscience publication, Wiley, 1989, p. 141, ISBN 978-0-471-91709-0.
- ^ J. B. Hendrickson, D. J. Cram e G. S. Hammond, CHIMICA ORGANICA, traduzione di A. Fava, 2ª ed., Piccin, 1973, p. 441.
- ^ a b J. B. Hendrickson, D. J. Cram e G. S. Hammond, CHIMICA ORGANICA, traduzione di A. Fava, 2ª ed., Piccin, 1973, pp. 156-159.
- ^ Eric V. Anslyn e Dennis A. Dougherty, Modern physical organic chemistry, University science, 2006, p. 902, ISBN 978-1-891389-31-3.
- ^ a b c Eli Breuer, Hans Günter Aurich e Arnold Nielsen, The chemistry of functional groups: a series of advanced treatises. 2: Nitrones, nitronates and nitroxides / by Eli Breuer; Hans Günter Aurich; Arnold Nielsen, collana An Interscience publication, Wiley, 1989, p. 142, ISBN 978-0-471-91709-0.
- ^ p-Cl−C6H4−CH=N−O−CH3
- ^ Arne Haaland, Hanne Thomassen e Yngve Stenstr∅m, Trimethylamine N-oxide, structure and bonding investigated by gas electron diffraction and ab initio MO calculations, in Journal of Molecular Structure, vol. 263, 2 dicembre 1991, pp. 299–310, DOI:10.1016/0022-2860(91)80072-C. URL consultato il 6 settembre 2023.
- ^ (EN) Jennifer Y. Pfeiffer e André M. Beauchemin, Simple Reaction Conditions for the Formation of Ketonitrones from Ketones and Hydroxylamines, in The Journal of Organic Chemistry, vol. 74, n. 21, 6 novembre 2009, pp. 8381–8383, DOI:10.1021/jo901653d. URL consultato l'11 settembre 2023.
- ^ a b (EN) Jessica E. Reimann e William P. Jencks, The Mechanism of Nitrone Formation. A Defense of Anthropomorphic Electrons 1, in Journal of the American Chemical Society, vol. 88, n. 17, 1966-09, pp. 3973–3982, DOI:10.1021/ja00969a016. URL consultato l'11 settembre 2023.
- ^ a b (EN) G. R. Delpierre e M. Lamchen, Nitrones, in Quarterly Reviews, Chemical Society, vol. 19, n. 4, 1º gennaio 1965, p. 333, DOI:10.1039/QR9651900329. URL consultato l'11 settembre 2023.
- ^ Thesing e Mayer 1957
- ^ Exner 1951
- ^ (EN) Dorthe Christensen e Karl Anker Joergensen, Oxidation of imines to nitrones by the permanganate ion, in The Journal of Organic Chemistry, vol. 54, n. 1, 1989-01, pp. 126–131, DOI:10.1021/jo00262a029. URL consultato il 2 aprile 2024.
- ^ (EN) Derek R. Boyd, Peter B. Coulter e M. Rosaleen McGuckin, Imines and derivatives. Part 24. Nitrone synthesis by imine oxidation using either a peroxyacid or dimethyldioxirane, in Journal of the Chemical Society, Perkin Transactions 1, n. 2, 1º gennaio 1990, pp. 301–306, DOI:10.1039/P19900000301. URL consultato il 2 aprile 2024.
- ^ Thesing e Mayer 1956
- ^ Jonathan Clayden, Nick Greeves e Stuart Warren, Organic chemistry, 2nd ed, Oxford university press, 2012, pp. 901-902, ISBN 978-0-19-927029-3.
- ^ (EN) Pat N. Confalone e Edward M. Huie (a cura di), Organic Reactions, 1ª ed., Wiley, 30 aprile 2004, DOI:10.1002/0471264180.or036.01, ISBN 978-0-471-26418-7. URL consultato il 6 settembre 2023.
- ^ a b Yang 2012
- ^ Döpp e Döpp 1990
- ^ G. Bianchi e P. Grünanger, Conversion of 2-isoxazolines to isoxazoles, in Tetrahedron, vol. 21, n. 4, 1º gennaio 1965, pp. 817–822, DOI:10.1016/0040-4020(65)80014-X. URL consultato il 6 settembre 2023.
- ^ Kinugasa e Hashimoto 1972
- ^ Shintani e Fu 2003
- ^ Pal e Basak 2006
- ^ Murahashi e Imada 2019
- ^ Marco Lombardo e Claudio Trombini, Nucleophilic Additions to Nitrones, in Synthesis, vol. 2000, n. 06, 2000, pp. 759–774, DOI:10.1055/s-2000-6269. URL consultato il 13 gennaio 2024.
- ^ (EN) Shun-Ichi Murahashi e Yasushi Imada, Synthesis and Transformations of Nitrones for Organic Synthesis, in Chemical Reviews, vol. 119, n. 7, 10 aprile 2019, pp. 4684–4716, DOI:10.1021/acs.chemrev.8b00476. URL consultato il 13 gennaio 2024.
- ^ Sunil Kumar Singh, M. Srinivasa Reddy e Mangesh Mangle, Cu(I)-mediated deoxygenation of N-oxides to amines, in Tetrahedron, vol. 63, n. 1, 1º gennaio 2007, pp. 126–130, DOI:10.1016/j.tet.2006.10.031. URL consultato il 13 gennaio 2024.
Bibliografia
[modifica | modifica wikitesto]- (DE) D. Döpp e H. Döpp, Methoden der Organischen Chemie, a cura di D. Klamann, E14b, Stuttgart, Thieme Verlag, 1990, pp. 1372–1544, ISBN 3-13-220004-2.
- (EN) O. Exner, A New Synthesis of N-methylketoximes, in Collect. Czech. Chem. Commun., vol. 16, 1951, pp. 258-267, DOI:10.1135/cccc19510258.
- (EN) M. Kinugasa e S. Hashimoto, The reactions of copper(I) phenylacetylide with nitrones, in J. Chem. Soc., Chem. Commun., 1972, pp. 466–467, DOI:10.1039/C39720000466.
- A. D. McNaught e A. Wilkinson, nitrones, su IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"), Blackwell Scientific Publications, 2006. URL consultato l'8 ottobre 2021.
- (EN) S.-I. Murahashi e Y. Imada, Synthesis and Transformations of Nitrones for Organic Synthesis, in Chemical Reviews, vol. 119, n. 7, 2019, pp. 4684–4716, DOI:10.1021/acs.chemrev.8b00476.
- (EN) R. Pal e A. Basak, A novel synthesis of
β -lactam fused cyclic enediynes by intramolecular Kinugasa reaction, in Chem. Commun., 2006, pp. 2992–2994, DOI:10.1039/b605743h. - (EN) R. Shintani e G. C. Fu, Catalytic Enantioselective Synthesis of
β -Lactams: Intramolecular Kinugasa Reactions and Interception of an Intermediate in the Reaction Cascade, in Angew. Chem. Int. Ed., vol. 42, n. 34, 2003, pp. 4082–4085, DOI:10.1002/anie.200352103. - (DE) J. Thesing e H. Mayer, Cyclische Nitrone I: Dimeres 2.3.4.5-Tetrahydro-pyridin-N-oxyd, in Chem. Ber., vol. 89, n. 9, 1956, pp. 2159-2167, DOI:10.1002/cber.19560890919.
- (DE) J. Thesing e H. Mayer, Cyclische Nitrone, II. Über die Polymeren des 2.3.4.5-Tetrahydro-pyridin-N-oxyds und verwandte Verbindungen, in Justus Liebigs Ann. Chem., vol. 609, n. 1, 1957, pp. 46-57, DOI:10.1002/jlac.19576090105.
- (EN) J. Yang, Recent Developments in Nitrone Chemistry, in Synlett, vol. 23, n. 16, 2012, pp. 2293-2297, DOI:10.1055/s-0032-131709.
Voci correlate
[modifica | modifica wikitesto]- Ammino ossido
- Trimetilammina N-ossido
- Nitronio
- Ammonio quaternario
- Sali di N-ossoammonio
- Immine
- Isossazolo
- Idrossilammina
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su nitrone
Wikimedia Commons contiene immagini o altri file su nitrone