퓨린
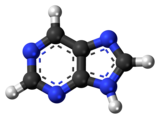
퓨린(영어: purine)은 피리미딘 고리와 이미다졸 고리가 융합된 두 개의 고리 구조를 특징으로 하는 분자식이 C5H4N4인 방향족 헤테로고리 유기 화합물이다. 퓨린은 수용성이다. 퓨린이란 용어는 또한 치환된 퓨린 및 퓨린의 호변이성질체를 포함하는 보다 넓은 의미로도 사용된다. 퓨린은 자연에서 가장 널리 생성되는 질소를 함유하고 있는 헤테로고리 화합물이다.[1]

| |
| |

| |
| 이름 | |
|---|---|
| IUPAC 이름
9H-purine
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.004.020 |
| KEGG | |
| MeSH | Purine |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C5H4N4 | |
| 몰 질량 | 120.115 g·mol−1 |
| 녹는점 | 214 °C (417 °F; 487 K) |
| 500 g/L (RT) | |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
퓨린은 육류 및 육류 제품 특히 간, 콩팥과 같은 내부 장기에서 고농도로 발견된다. 일반적으로 식물성 식단에는 퓨린의 함량이 낮다.[2] 퓨린의 함량이 높은 공급원의 예로는 스위트브레드, 멸치, 정어리, 간, 소의 콩팥, 뇌, 고기 추출물(예: 옥소, 보브릴), 청어, 고등어, 가리비, 맥주(효모로부터 유래), 그레이비 등이 있다.
붉은 고기, 쇠고기, 돼지고기, 가금류, 물고기, 해산물, 아스파라거스, 콜리플라워, 시금치, 식용 버섯, 완두, 렌즈콩, 콩, 오트밀, 속겨, 밀배아 등에도 적당한 양의 퓨린이 함유되어 있다.[3]
핵염기는 퓨린 계열 염기와 피리미딘 계열의 염기로 구성된다. DNA의 빌딩 블록인 4가지 디옥시리보뉴클레오타이드들 중 2가지(디옥시아데노신 일인산, 디옥시구아노신 일인산) 및 RNA의 빌딩 블록인 4가지 리보뉴클레오타이드들 중 2가지(아데노신 일인산, 구아노신 일인산)는 퓨린 뉴클레오타이드이다. DNA와 RNA를 생성하기 위해, 세포에서 퓨린 및 피리미딘 둘 다 대략 동일한 양으로 필요하다. 퓨린과 피리미딘은 둘 다 자가억제 및 활성화된다. 퓨린이 생성되면 더 많은 퓨린을 생성하기 위해 필요한 효소들을 저해한다. 이러한 자가억제는 또한 피리미딘을 생성하기 위해 필요한 효소들을 활성화시키기 때문에 일어난다. 피리미딘도 동시에 유사한 방식으로 자가억제하고 퓨린 생성을 활성화시킨다. 이 때문에 세포 내에 항상 거의 같은 양의 퓨린과 피리미딘이 존재한다.[4]
특성
편집퓨린은 매우 약한 산(pKa 2.39)이며, 약한 염기(pKa 8.93)이다.[5] 물에 용해되면 pH는 이 두 pKa 값 사이의 중간값이 된다.
주목할만한 퓨린
편집자연적으로 생성되는 많은 퓨린들이 있다. 이들은 핵염기인 아데닌과 구아닌을 포함한다. DNA에서 아데닌은 상보적인 피리미딘인 티민과, 구아닌은 사이토신과 수소 결합을 형성한다. 이들은 상보적인 염기쌍이라고 불린다. RNA에서 아데닌은 티민 대신에 유라실과 상보적인 염기쌍을 형성한다.
다른 주목할만한 퓨린으로는 하이포잔틴, 잔틴, 테오브로민, 카페인, 요산, 아이소구아닌이 있다.
N9 치환 유도체
편집퓨린 고리의 9번 질소 원자(N9)에 결합된 수소 원자가 다른 원자 혹은 원자단으로 치환된 많은 화합물들은 생물체 내에서, 혹은 약물로써 다양한 기능을 한다. 아데노신 삼인산(ATP)과 구아노신 삼인산(GTP)은 생물체의 에너지 전달에 필수적인 분자이며,[6] 이 분자들에서 인산기 2개를 떼어낸 아데노신 일인산(AMP)과 구아노신 일인산(GMP) 및 리보스가 아닌 디옥시리보스 치환기를 갖는 dAMP와 dGMP는 각각 유전 정보를 저장하는 RNA와 DNA의 구성요소인 뉴클레오타이드의 일종이다.[7] NADH, NADPH, FADH2는 생물체 내 산화환원 반응에서 전자공여체로 쓰인다.[8]
-
ATP
-
GTP
-
dAMP
-
NADH의 산화된 형태인 NAD+
-
FADH2의 산화된 형태인 FAD
N9에 아릴기가 치환된 많은 화합물은 체내에 들어갔을 때 항바이러스 및 항암 효과를 갖고 있다는 사실이 알려져 있다.[9]
기능
편집DNA 및 RNA에서 퓨린(아데닌 및 구아닌)의 중요한 역할 외에도, 퓨린은 ATP, GTP, cAMP, NADH, 조효소 A와 같은 여러 다른 중요한 생체분자에서 주요 구성 성분이다. (1) 퓨린 그 자체는 자연에서 발견되지 않았지만, 유기 합성에 의해 만들어질 수 있다.
이들은 또한 퓨린작동성 수용체에 작용하여 신경전달물질로 직접 작용할 수 있다. 아데노신은 아데노신 수용체를 활성화시킨다.
역사
편집퓨린(purine) ("순수한 오줌(pure urine)"에서 유래)[10]이라는 단어는 1884년에 독일의 화학자 에밀 피셔가 만들었다.[11][12] 에밀 피셔는 1898년에 처음으로 퓨린을 합성했다.[12] 반응의 출발 물질은 (8) 요산이었다. 요산은 1776년에 칼 빌헬름 셸레에 의해 신장 결석에서 분리되었다.[13] (8) 요산을 오염화 인(PCl5)과 반응시켜 (10) 2,6,8-트라이클로로퓨린을 얻었고, 이를 아이오딘화 수소(HI)와 PH4I로 전환시켜, (11) 2,6-다이아이오도퓨린을 얻었다. 아연 분말을 사용하여 생성물을 (1) 퓨린으로 환원시켰다.
물질대사
편집많은 생물들이 퓨린을 합성하고 분해하기 위한 대사 경로를 가지고 있다.
퓨린은 뉴클레오사이드(핵염기와 리보스가 결합됨)로 생물학적으로 합성된다.
다양한 세포 내 대사 과정, 특히 DNA 및 RNA와 관련된 대사 과정에 결함이 있으면 변형된 퓨린 뉴클레오타이드가 축적된다. 생존하기 위해, 생물은 다수의 (디옥시)퓨린 포스포하이드롤레이스를 가지고 있으며, 이 효소는 이들 퓨린 유도체들을 가수분해하여 활성 NTP 및 dNTP 풀에서 이들을 제거한다. 퓨린 염기의 탈아미노화는 ITP, dITP, XTP, dXTP와 같은 뉴클레오사이드의 축적을 초래할 수 있다.[14]
퓨린의 생성 및 분해를 조절하는 효소의 결함은 세포의 DNA 서열을 심하게 변화시킬 수 있으며, 이는 퓨린 대사 효소의 특정 유전자 변이체를 가지고 있는 사람들이 일부 유형의 암에 대한 발병 위험이 더 높은 이유를 말해준다.
통풍과의 관계
편집육류 및 해산물의 섭취량이 많을수록 통풍의 위험이 증가하는 반면, 유제품의 섭취량이 많을수록 통풍의 위험이 감소하는 것과 관련이 있다. 퓨린이 풍부한 채소나 단백질의 적당한 섭취는 통풍의 위험이 증가하는 것과 관련이 없다.[15][16] 고요산혈증의 위험이 있는 유사한 결과가 발견되었다.
실험실에서의 합성
편집퓨린 대사에서 퓨린의 생체 내 합성 외에도, 퓨린은 인위적으로 합성될 수도 있다.
1972년 도쿄 대학의 야마데 히로시와 오카모토 토시히코는 개방된 용기에서 폼아마이드를 170-190℃의 온도로 28시간 동안 가열하여 (1) 퓨린을 양호한 수율로 얻어냈다.[17]
이 반응과 다른 반응들은 생명의 기원과 관련하여 논의되었다.[18]
오로(Oro), 오겔(Orgel) 및 동료들은 4개의 사이안화 수소(HCN) 분자가 사량체화되어 (12) 다이아미노말레오다이나이트릴을 형성하며, 이는 거의 모든 자연적으로 생성되는 퓨린으로 전환될 수 있음을 보여주었다.[19][20][21][22][23] 예를 들어, 5개의 HCN 분자 발열 반응에서 응축되어 특히 암모니아의 존재 하에서 아데닌을 생성한다.
트라우베 퓨린 합성(1900)은 아민-치환된 피리미딘과 폼산 사이의 고전적인 반응으로 빌헬름 트라우베(Wilhelm Traube)의 이름을 따서 명명되었다.[24]
반응
편집항암제 등의 약물 합성을 위한 반응물로 퓨린 유도체가 사용되는데, 아릴기가 N9 원자에 치환된 퓨린 유도체를 합성하는 방법으로 피리미딘 유도체에서 시작하여 고리화 반응을 통해 아릴기가 치환된 이미다졸 부분(7,8,9번 원자)을 합성하는 방법이 알려져 있다. 하지만 이 방법은 여러 단계를 필요로 한다.[25] 2003년, 노르웨이 오슬로 대학의 Anne Kristin Bakkestuen과 Lise-Lotte Gundersen이 아세트산구리(copper(II) acetate) 존재 하에서 N9 원자에 아무것도 치환되지 않은 퓨린 유도체에 아릴기를 직접 치환하는 데 성공하였다.[26]
같이 보기
편집각주
편집- ↑ Rosemeyer, Helmut (March 2004). “The Chemodiversity of Purine as a Constituent of Natural Products”. 《Chemistry & Biodiversity》 1 (3): 361–401. doi:10.1002/cbdv.200490033. PMID 17191854.
- ↑ “Gout: List of Foods High and Low in Purine Content”. 《Dietaryfiberfood.com》. 2016년 4월 8일. 2011년 11월 12일에 원본 문서에서 보존된 문서. 2016년 7월 16일에 확인함.
- ↑ “Gout Diet: What Foods To Avoid”. 《Healthcastle.com》. 2016년 7월 16일에 확인함.
- ↑ Guyton, Arthur C. (2006). 《Textbook of Medical Physiology》. Philadelphia, PA: Elsevier. 37쪽. ISBN 978-0-7216-0240-0.
- ↑ F. Seela; 외. (2014). Ernst Schaumann, 편집. 《Houben-Weyl Methods of Organic Chemistry Vol. E 9b/2, 4th Edition Supplement: Hetarenes III (Six-Membered Rings and Larger Hetero-Rings with Maximum Unsaturation) - Part 2b》. 310쪽. ISBN 9783131815040.
- ↑ Jeremy M. Berg, John L. Tymoczko, Lubert Stryer, 앞의 책, pp.412-413.
- ↑ John McMurry, 앞의 책, p.981.
- ↑ 위의 책, pp.802-803.
- ↑ Hong-Ying Niu, Chao Xia 외 6명, "CuBr Catalyzed C–N cross coupling reaction of purines and diaryliodonium salts to 9-arylpurines", Organic & Biomolecular Chemistry Issue 14, 2011, pp.5039-5042에서 재인용.
- ↑ McGuigan, Hugh (1921). 《An Introduction To Chemical Pharmacology》. P. Blakiston's Sons & Co. 283쪽. 2020년 4월 16일에 원본 문서에서 보존된 문서. 2012년 7월 18일에 확인함.
- ↑ Fischer, Emil (1884). “Ueber die Harnsäure. I.” [On uric acid. I.]. 《Berichte der Deutschen Chemischen Gesellschaft》 17: 328–338. doi:10.1002/cber.18840170196.
From p. 329: "Um eine rationelle Nomenklatur der so entstehenden zahlreichen Substanzen zu ermöglichen, betrachte ich dieselben als Abkömmlinge der noch unbekannten Wasserstoffverbindung CH3.C5N4H3 and nenne die letztere Methylpurin." (In order to make possible a rational nomenclature for the numerous existing substances, I regarded them as derivatives of a still unknown hydrogen compound, CH3.C5N4H3, and call the latter "methylpurine".) - ↑ 가 나 Fischer, Emil (1898). “Ueber das Purin und seine Methylderivate” [On purine and its methyl derivatives]. 《Berichte der Deutschen Chemischen Gesellschaft》 31 (3): 2550–2574. doi:10.1002/cber.18980310304.
From p. 2550: "…hielt ich es für zweckmäßig, alle diese Produkte ebenso wie die Harnsäure als Derivate der sauerstofffreien Verbindung C5H4N4 zu betrachten, und wählte für diese den Namen Purin, welcher aus den Wörtern purum und uricum kombiniert war." (…I regarded it as expedient to consider all of these products, just like uric acid, as derivatives of the oxygen-free compound C5H4N4, and chose for them the name "purine", which was formed from the [Latin] words purum and uricum.) - ↑ Scheele, C. W. (1776). “Examen chemicum calculi urinari” [A chemical examination of kidney stones]. 《Opuscula》 2: 73.
- ↑ Davies, O.; Mendes, P.; Smallbone, K.; Malys, N. (2012). “Characterisation of multiple substrate-specific (d)ITP/(d)XTPase and modelling of deaminated purine nucleotide metabolism”. 《BMB Reports》 45 (4): 259–264. doi:10.5483/BMBRep.2012.45.4.259. PMID 22531138.
- ↑ Choi, Hyon K.; Atkinson, Karen; Karlson, Elizabeth W.; Willett, Walter; Curhan, Gary (2004). “Purine-Rich Foods, Dairy and Protein Intake, and the Risk of Gout in Men”. 《New England Journal of Medicine》 350 (11): 1093–1103. doi:10.1056/NEJMoa035700. PMID 15014182.
- ↑ “Bone Health”. USDA. 2016년 7월 17일에 확인함.
- ↑ Yamada, H.; Okamoto, T. (1972). “A One-step Synthesis of Purine Ring from Formamide”. 《Chemical & Pharmaceutical Bulletin》 20 (3): 623. doi:10.1248/cpb.20.623. 2016년 5월 16일에 원본 문서에서 보존된 문서.
- ↑ Saladino, Raffaele; Crestini, Claudia; Ciciriello, Fabiana; Costanzo, Giovanna; Mauro, Ernesto; 외. (2006). “About a Formamide-Based Origin of Informational Polymers: Syntheses of Nucleobases and Favourable Thermodynamic Niches for Early Polymers”. 《Origins of Life and Evolution of Biospheres》 36 (5–6): 523–531. Bibcode:2006OLEB...36..523S. doi:10.1007/s11084-006-9053-2. PMID 17136429.
- ↑ Sanchez, R. A.; Ferris, J. P.; Orgel, L. E. (1967). “Studies in prebiotic synthesis. II. Synthesis of purine precursors and amino acids from aqueous hydrogen cyanide”. 《Journal of Molecular Biology》 30 (2): 223–253. doi:10.1016/S0022-2836(67)80037-8. PMID 4297187.
- ↑ Ferris, James P.; Orgel, L. E. (March 1966). “An Unusual Photochemical Rearrangement in the Synthesis of Adenine from Hydrogen Cyanide”. 《Journal of the American Chemical Society》 88 (5): 1074. doi:10.1021/ja00957a050.
- ↑ Ferris, J. P.; Kuder, J. E.; Catalano, O. W. (1969). “Photochemical Reactions and the Chemical Evolution of Purines and Nicotinamide Derivatives”. 《Science》 166 (3906): 765–766. Bibcode:1969Sci...166..765F. doi:10.1126/science.166.3906.765. PMID 4241847.
- ↑ Oro, J.; Kamat, J. S. (1961). “Amino-acid Synthesis from Hydrogen Cyanide under Possible Primitive Earth Conditions”. 《Nature》 190 (4774): 442–443. Bibcode:1961Natur.190..442O. doi:10.1038/190442a0. PMID 13731262.
- ↑ Bauer, Wolfgang (1985). 《Houben-Weyl Methods of Organic Chemistry Vol. E 5, 4th Edition Supplement》. Thieme Georg Verlag. 1547쪽. ISBN 9783131811547.
- ↑ Hassner, Alfred; Stumer, C. (2002). 《Organic Syntheses Based on Name Reactions》 2판. Elsevier. ISBN 0-08-043259-X.
- ↑ Hong-Ying Niu, Chao Xia 외 6명, 앞의 논문에서 재인용.
- ↑ Anne Kristin Bakkestuen, Lise-Lotte Gundersen, "Regioselective N-9 arylation of purines employing arylboronic acids in the presence of Cu(II)", Tetrahedron Letters Volume 44, Issue 16, 2003, pp.3359–3362.
외부 링크
편집위키미디어 공용에 퓨린 관련 미디어 분류가 있습니다.
- Purine Content in Food Archived 2011년 11월 12일 - 웨이백 머신