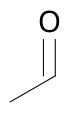
Etanal
Etanal ou Acetaldeído é o aldeído de fórmula química C2H4O. Ele é um líquido incolor, acre, que ferve aproximadamente à temperatura ambiente, é o produto metabólico primário do etanol na sua rota de conversão a ácido acético. É produzido pela enzima álcool desidrogenase, que ocorre principalmente no fígado, mas também, em pequena quantidade, na retina.
Ocorrência natural
[editar | editar código-fonte]Também contribui para o odor das frutas maduras.
Produção
[editar | editar código-fonte]Em 2003, a produção global foi de aproximadamente 106 toneladas/ano.[1] O principal método de produção é a oxidação de etileno via o processo Wacker:
- 2 CH2=CH2 + O2 → 2 CH3CHO
Alternativamente, hidratação de acetileno, catalisado por sais de mercúrio resulta em etenol, o qual tautomeriza-se a acetaldeído. Esta rota industrial foi dominante anteriormente ao processo Wacker[2] Ele também é preparado em pequenas escalas tanto pela desidrogenação quanto pela oxidação catalíticas (por contato com cobre, prata ou platina aquecidos) de etanol. Respectivamente:
- C2H5OH → C2H4O + H2
- C2H5OH + [O] → C2H4O + H2O
Questões no metabolismo humano
[editar | editar código-fonte]O acetaldeído é um dos agentes responsáveis pela ressaca, embora existam também numerosas e complexas contribuições interrelacionadas provenientes das alterações fisiológicas que ocorrem quando o corpo responde a níveis anormalmente altos de etanol e à narcose suave, ao desequilíbrio ácido e à desidratação que ele induz.
O Acetaldeído é metabolizado no organismo pela enzima Aldeído-Desidrogenase-2 , que o converte em acetato. Quando a quantidade de álcool ingerida é maior do que a capacidade de metabolização do aldéido ocorre uma acumulação desta substância no organismo o que pode gerar vermelhidão facial, cefaléia, taquicardia, tontura e náuseas. Grande parte da população oriental possui deficiência desta enzima o que faz com que, nestes indivíduos, os efeitos do acúmulo de acetaldeído no organismo seja sentido precocemente. Existem estudos que indicam que devido a esta deficiência, as populações orientais tem uma menor probabilidade de desenvolver alcoolismo.
O álcool desidrogenase está presente no nosso corpo porque necessitamos metabolizar o álcool produzido em pequenas quantidades pela digestão e quebra dos carboidratos e, em grandes quantidades pelas bactérias em nosso intestino.
Referências
- ↑ Marc Eckert, Gerald Fleischmann, Reinhard Jira, Hermann M. Bolt, Klaus Golka “Acetaldehyde” in Ullmann's Encyclopedia of Industrial Chemistry, 2006, Wiley-VCH, Weinheim. doi:10.1002/14356007.a01_031.pub2.
- ↑ Dmitry A. Ponomarev and Sergey M. Shevchenko (2007). «Hydration of Acetylene: A 125th Anniversary» (PDF). J. Chem. Ed. 84 (10). 1725 páginas. doi:10.1021/ed084p1725