Растворимость
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры. Все вещества в той или иной степени растворимы в растворителях. В случае, когда растворимость слишком мала для измерения, говорят, что вещество нерастворимо.
Зависимость растворимости веществ от температуры выражается с помощью кривых растворимости. По кривым растворимости производят различные расчёты. Например, можно определить массу вещества, которое выпадет в осадок из насыщенного раствора при его охлаждении.
Процесс выделения твёрдого вещества из насыщенного раствора при понижении температуры называется кристаллизацией. Кристаллизация играет огромную роль в природе — приводит к образованию некоторых минералов, участвует в процессах, протекающих в горных породах.
Способы выражения характеристик растворимости
[править | править код]Характеристики растворимости подразделяются на качественные и количественные.
Качественные характеристики определяют мнение исследователя в отношении растворимости данного вещества — хорошо растворимо, плохо растворимо, мало растворимо, нерастворимо и т. п., и являются субъективными. Попытка сделать их более объективными была сделана в Государственной фармакопее СССР для обозначения растворимости лекарственных средств, но она не получила распространения.
Количественные характеристики определяют количество вещества, растворённого в данном количестве растворителя при данных условиях и обычно имеют размерности концентрации (моль/л, г/100 г растворителя, г/100 г раствора, г/кг растворителя, мольная доля и т. д.).
Качественная и количественная растворимость приводится в справочной литературе.
Влияние условий на растворимость
[править | править код]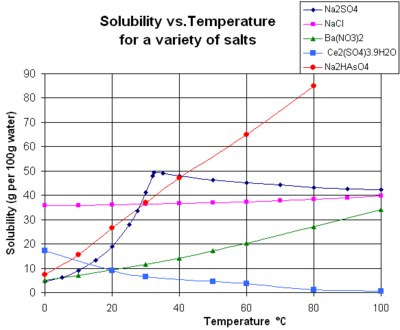
Для определения качественной растворимости часто используется эмпирическое правило «подобное растворяется в подобном». Это правило разные источники объясняют немного по-разному: полярные вещества растворяются в полярных растворителях, вещества, имеющие гидроксильные группы, хорошо растворяются в растворителях с гидроксильными группами и т. п.
Растворимость зависит от
- растворяемого вещества,
- растворителя,
- температуры,
- давления,
- наличия в растворителе других веществ.
Растворимость большинства газов растет с ростом давления и уменьшается с ростом температуры. Для твёрдых и жидких веществ влияние давления на растворимость менее значимо, чем для газов. Температура имеет различное влияние на различные системы «растворяемое вещество — растворитель», но в большинстве случаев при увеличении температуры растёт растворимость (обратной зависимостью обладают, например, многие соли кальция). Так как растворяемое вещество часто увеличивает температуру кипения растворителя, растворимость при атмосферном давлении может быть измерена и выше температуры кипения растворителя. При повышенном давлении и температуре растворимость может сильно увеличиваться (например, в воде при высоком давлении и температуре относительно хорошо растворяются углеводороды и кварц, которые почти нерастворимы при обычных условиях).
Наличие в растворителе других веществ может сильно влиять на растворимость. Примеры:
- добавление солей в водный раствор неполярных веществ может привести к выделению неполярного вещества в осадок, за счет эффекта высаливания,
- наличие растворённого кислорода сильно влияет на растворимость ртути в воде за счет эффектов поверхностного окисления,
- наличие небольшого количества влаги в абсолютном этаноле может сильно изменить растворимость неполярных веществ.
Энергетические эффекты при растворении
[править | править код]Растворение веществ часто происходит с разогреванием или охлаждением раствора.
Способы измерения растворимости
[править | править код]Самым старым способом измерения растворимости является растворение вещества до его выпадения в осадок, выдерживание такой смеси при определенной температуре, отделение осадка и вычисление растворившегося вещества.
В современных условиях для измерения очень малых значений растворимости часто пользуются хроматографическими системами.
При измерениях растворимости важно учесть все факторы, которые могут повлиять на растворимость.
Литература
[править | править код]- Химическая энциклопедия. — Т. 4. — М.: Большая российская энциклопедия, 1995