EDTA
| |

| |
| Imena | |
|---|---|
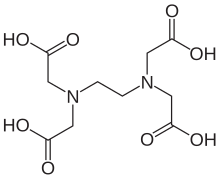
| Priporočeno IUPAC ime
2,2',2'',2'''-(etan-1,2-diildinitrilo)tetraocetna kislina | |
| Sistematično ime
2-({2-[bis(karboksimetil)amino]etil}(karboksimetil)amino)ocetna kislina | |
| Druga imena
diaminoetan-tetraocetna kislina
edetična kislina etilendinitrilo-tetraocetna kislina versen | |
| Identifikatorji | |
| |
3D model (JSmol)
|
|
| Kratice | EDTA H4EDTA |
| 1716295 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.409 |
| EC število |
|
| KEGG | |
| MeSH | Edetic+acid |
PubChem CID
|
|
| RTECS število |
|
| UNII | |
| UN število | 3077 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| C10H16N2O8 | |
| Molska masa | 292,24 g·mol−1 |
| Gostota | 0,86 g cm−3 |
| Kislost (pKa) | pKa1 = 0,0 (CO2H) (µ = 1,0) pKa2 = 1,5 (CO2H) (µ = 0,1) pKa3 = 2,00 (CO2H) (µ = 0,1) pKa4 = 2,69 (CO2H) (µ = 0,1) pKa5 = 6,13 (NH+) (µ = 0,1) pKa6 = 10,37 (NH+) (µ = 0,1)[1] |
| Nevarnosti | |
| Glavne nevarnosti | dražljiva snov |
| R-stavki (zastarelo) | R36 |
| S-stavki (zastarelo) | S26 |
| NFPA 704 (diamant ognja) | |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Etilendiamintetraocetna kislina ali EDTA je najpomembnejši predstavnik poliaminokarboksilatov oz. poliaminokarboksilnih kislin. Je brezbarvna spojina, na sobni temperaturi je v trdnem agregatnem stanju in v vodi se dobro topi. Je kelatni ligand, ki veže kovinske ione v stehiometričnem razmerju 1:1, ne glede na valenco iona.

EDTA se veže na centralni kovinski ion preko dveh dušikov in štirih karboksilatov, v oktaedrični geometriji.
V kislih raztopinah prevladuje dvakrat protonirana oblika H6EDTA2+. Splošni zapis EDTA se nanaša na H4EDTA, ki prevladuje v nevtralnem mediju. V bazičnih medijih pa prevladuje oblika EDTA4-, v kateri so vse štiri karboksilne skupine deprotonirane.
Prednost EDTA je njen širok pH interval efektivne vezave kovinskih ionov (2 < pH < 11), slabost pa je njena slaba biorazgradljivost in nespecifičnost za nekatere ione. Zato obstajajo strukturno različni poliaminokarboksilati z drugačnimi fizikalno-kemijskimi lastnostmi (EDDS, EGTA, BAPTA, DTPA ...).
Sinteza
[uredi | uredi kodo]Letna svetovna proizvodnja EDTA je okrog 80.000 ton. Pripravi se jo iz etilendiamina, formaldehida in natrijevega cianida.
Viri
[uredi | uredi kodo]- ↑ Harris, D.C. "Quantitative Chemical Analysis", 7th ed., W. H. Freeman and Compagny, New York, 2007


