Patiromer
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Veltassa |
| Đồng nghĩa | RLY5016 |
| AHFS/Drugs.com | entry |
| Dược đồ sử dụng | Oral suspension |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | Not absorbed |
| Chuyển hóa dược phẩm | None |
| Bắt đầu tác dụng | 7 hrs |
| Thời gian hoạt động | 24 hrs |
| Bài tiết | Feces |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS |
|
| PubChem SID | |
| DrugBank | |
| ChemSpider |
|
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| Dữ liệu hóa lý | |
| Công thức hóa học | [(C3H3FO2)182·(C10H10)8·(C8H14)10]n [Ca91(C3H2FO2)182·(C10H10)8·(C8H14)10]n (calcium salt) |
Patirome (USAN, tên thương mại Veltassa) là một loại thuốc được sử dụng để điều trị tăng kali máu (nồng độ kali trong máu tăng), một tình trạng có thể dẫn đến đánh trống ngực và rối loạn nhịp tim (nhịp tim không đều). Nó hoạt động bằng cách liên kết kali trong ruột.[1][2]
Sử dụng trong y tế
[sửa | sửa mã nguồn]Patirome được sử dụng để điều trị tăng kali máu, nhưng không phải là một điều trị khẩn cấp cho tăng kali máu đe dọa tính mạng, bởi vì nó hoạt động tương đối chậm.[2] Một tình trạng như vậy cần các loại điều trị khác, ví dụ như truyền calci, insulin cộng với truyền glucose, hít salbutamol và chạy thận nhân tạo.[3]
Những lý do điển hình cho tăng kali máu là bệnh thận mãn tính và áp dụng các loại thuốc ức chế hệ thống aldosterone angiotensinTHER (RAAS) - ví dụ Thuốc ức chế men chuyển, thuốc đối kháng thụ thể angiotensin II hoặc thuốc lợi tiểu tiết kiệm kali - hoặc gây cản trở chức năng thận nói chung, như thuốc chống viêm không steroid (NSAID).[4][5]
Tác dụng phụ
[sửa | sửa mã nguồn]Patirome thường được dung nạp tốt trong các nghiên cứu. Các tác dụng phụ xảy ra ở hơn 2% bệnh nhân trong các thử nghiệm lâm sàng chủ yếu là các vấn đề về dạ dày-ruột như táo bón, tiêu chảy, buồn nôn và đầy hơi, và cả hạ calci máu (nồng độ magiê trong máu thấp) ở 5% bệnh nhân, bởi vì patirome liên kết magnesi trong ruột là tốt.[2][6]
Tương tác
[sửa | sửa mã nguồn]Patirome đã được thử nghiệm về tương tác thuốc với 28 loại thuốc và cho thấy sự ràng buộc hoặc tương tác với 14 loại thuốc này. Điều này có thể làm giảm tính khả dụng của chúng và do đó hiệu quả,[2] đó, người bảo trợ đã nhận được cảnh báo đóng hộp của Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA), nói với bệnh nhân nên chờ ít nhất sáu giờ giữa khi dùng patirome và bất kỳ loại thuốc uống nào khác.[7]
Trong số 14 loại thuốc cho thấy sự tương tác trong ống nghiệm, 12 loại đã được chọn để thử nghiệm thêm trong các nghiên cứu pha 1 ở những người tình nguyện khỏe mạnh để đánh giá xem kết quả nhìn thấy trong ống nghiệm có ảnh hưởng đến con người hay không. Những nghiên cứu này cho thấy patirome không làm thay đổi sự hấp thu của chín trong số 12 loại thuốc khi dùng chung. Patirome làm giảm sự hấp thu của ba loại thuốc khi dùng chung, tuy nhiên, không có tương tác khi patirome và ba loại thuốc này được dùng cách nhau 3 giờ.[8]
Thông tin này đã được đệ trình lên FDA dưới dạng Đơn đăng ký thuốc mới bổ sung (sNDA) và kết quả là vào tháng 11 năm 2016, FDA đã phê chuẩn loại bỏ cảnh báo đóng hộp liên quan đến việc tách patirome và các loại thuốc uống khác. Nhãn cập nhật khuyến cáo bệnh nhân dùng patirome ít nhất 3 giờ trước hoặc 3 giờ sau khi uống thuốc khác.[9]
Dược lý
[sửa | sửa mã nguồn]Cơ chế hoạt động
[sửa | sửa mã nguồn]Patirome hoạt động bằng cách liên kết các ion kali tự do trong đường tiêu hóa và giải phóng các ion calci để trao đổi, do đó làm giảm lượng kali có sẵn để hấp thụ vào máu và tăng lượng bài tiết qua phân. Tác dụng ròng là giảm nồng độ kali trong huyết thanh.[2][4]
Giảm mức kali có thể phát hiện 7 giờ sau khi dùng. Mức độ tiếp tục giảm trong ít nhất 48 giờ nếu tiếp tục điều trị và duy trì ổn định trong 24 giờ sau khi dùng liều cuối cùng. Sau đó, nồng độ kali bắt đầu tăng trở lại trong khoảng thời gian ít nhất bốn ngày.[2]
Dược động học
[sửa | sửa mã nguồn]Patirome không được hấp thụ từ ruột, không được chuyển hóa và được bài tiết ở dạng không đổi với phân.[2]
Hóa học
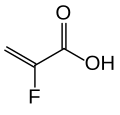
[sửa | sửa mã nguồn]Chất này là một polymer liên kết ngang của axit acrylic 2-fluoro với divinylbenzenes và 1,7-octadiene. Nó được sử dụng dưới dạng muối calci của nó (tỷ lệ 2: 1) và với sorbitol (một phân tử trên hai ion calci hoặc bốn đơn vị axit fluoroacrylic), một sự kết hợp được gọi là calci patirome sorbitex.[10]
-
2-fluoroacrylic acid
-
o-divinylbenzene
-
p-divinylbenzene
-
1,7-octadiene
Patirome sorbitex calci là một loại bột không màu trắng đến nâu nhạt, vô định hình, chảy tự do. Nó không hòa tan trong nước, 0,1 M axit clohydric, heptan và metanol.[2][10]
Lịch sử
[sửa | sửa mã nguồn]Nghiên cứu
[sửa | sửa mã nguồn]Trong một thử nghiệm lâm sàng đa trung tâm giai đoạn III bao gồm 237 bệnh nhân bị tăng kali máu trong điều trị bằng thuốc ức chế RAAS, 76% người tham gia đạt mức kali huyết thanh bình thường trong vòng bốn tuần. Sau khi ngẫu nhiên tiếp theo 107 người trả lời vào một nhóm được tiếp tục điều trị bằng patirome và nhóm giả dược, sự tái xuất hiện của tăng kali máu lần lượt là 15% so với 60%.[11]
Sự chấp thuận
[sửa | sửa mã nguồn]FDA Hoa Kỳ đã phê duyệt patirome vào tháng 10 năm 2015.[7] Thuốc này cũng đã được phê duyệt ở châu Âu tính đến tháng 7 năm 2017[cập nhật].
Xem thêm
[sửa | sửa mã nguồn]- ZS-9, một chất kết dính kali khác
Tham khảo
[sửa | sửa mã nguồn]- ^ Henneman, A; Guirguis, E; Grace, Y; Patel, D; Shah, B (2016). "Emerging therapies for the management of chronic hyperkalemia in the ambulatory care setting". American Journal of Health-System Pharmacy. 73 (2): 33–44. doi:10.2146/ajhp150457. PMID 26721532. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Henneman” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ a b c d e f g h FDA Professional Drug Information for Veltassa. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Drugs.com” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Vanden Hoek TL, Morrison LJ, Shuster M, Donnino M, Sinz E, Lavonas EJ, Jeejeebhoy FM, Gabrielli A; Morrison; Shuster; Donnino; Sinz; Lavonas; Jeejeebhoy; Gabrielli (2010-11-02). "Part 12: cardiac arrest in special situations: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care". Circulation. 122 (18 Suppl 3): S829–61. doi:10.1161/CIRCULATIONAHA.110.971069. PMID 20956228.CS1 maint: Multiple names: authors list (link) Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “AHA2010” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ a b Esteras, R.; Perez-Gomez, M. V.; Rodriguez-Osorio, L.; Ortiz, A.; Fernandez-Fernandez, B. (2015). "Combination use of medicines from two classes of renin-angiotensin system blocking agents: Risk of hyperkalemia, hypotension, and impaired renal function". Therapeutic Advances in Drug Safety. 6 (4): 166–76. doi:10.1177/2042098615589905. PMC 4530349. PMID 26301070. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Esteras” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Rastegar, A; Soleimani, M (2001). "Hypokalaemia and hyperkalaemia". Postgraduate Medical Journal. 77 (914): 759–64. doi:10.1136/pmj.77.914.759. PMC 1742191. PMID 11723313. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Rastegar” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Tamargo, J; Caballero, R; Delpón, E (2014). "New drugs for the treatment of hyperkalemia in patients treated with renin-angiotensin-aldosterone system inhibitors -- hype or hope?". Discovery medicine. 18 (100): 249–54. PMID 25425465. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Tamargo” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ a b "FDA approves new drug to treat hyperkalemia". FDA. ngày 21 tháng 10 năm 2015. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “FDAPress” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Pharmabiz: US FDA approves removal of boxed warning on Relypsa's hyperkalemia drug, Veltassa Lưu trữ 2016-12-21 tại Wayback Machine.
- ^ FDA Package Insert: VELTASSA (patiromer) for oral suspension. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “FDA Package Insert” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ a b RxList: Veltassa.
- ^ Weir, Matthew R.; Bakris, George L.; Bushinsky, David A.; Mayo, Martha R.; Garza, Dahlia; Stasiv, Yuri; Wittes, Janet; Christ-Schmidt, Heidi; Berman, Lance; Pitt, Bertram (2015). "Patiromer in Patients with Kidney Disease and Hyperkalemia Receiving RAAS Inhibitors". New England Journal of Medicine. 372 (3): 211–21. doi:10.1056/NEJMoa1410853. PMID 25415805. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Weir” được định rõ nhiều lần, mỗi lần có nội dung khác
<ref> được định nghĩa trong <references> có tên “rxlist” không có nội dung.