医薬品 情報
| ベシケア | |
| コハク |
|
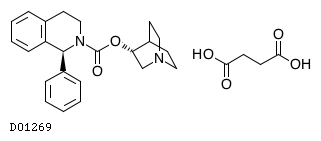
| Solifenacin Succinate | |
| コハク |
|
| 2590 | |
| ATCコード | G04BD08 |
| KEGG DRUG |
D01269
コハク
|
| JAPIC |
|
添付 文書 情報 2019年 8月 改訂 (第 1版 )
商品 情報
3.組成 ・性状
| YJコード | |||||
|---|---|---|---|---|---|
|
ベシケアOD |
Vesicare OD Tablets 2.5mg | アステラス |
2590011F3020 | 54.8 |
|
|
ベシケアOD |
Vesicare OD Tablets 5mg | アステラス |
2590011F4027 | 94.6 |
2. 禁忌
2.1 本 剤 の成分 に対 し過敏 症 の既往 歴 のある患者
2.5 胃 アトニー又 は腸 アトニーのある患者 [抗 コリン作用 により消化 管 運動 が低下 するため症状 が悪化 するおそれがある。]
2.6 重症 筋 無力 症 の患者 [抗 コリン作用 により筋 緊張 の低下 がみられ症状 が悪化 するおそれがある。]
4. 効能 または効果
5. 効能 または効果 に関連 する注意
5.1 本 剤 を適用 する際 、十分 な問診 により臨床 症状 を確認 するとともに、類似 の症状 を呈 する疾患 (尿 路 感染 症 、尿 路 結石 、膀胱 癌 や前立腺 癌 などの下部 尿 路 における新 生物 等 )があることに留意 し、尿 検査 等 により除外 診断 を実施 すること。なお、必要 に応 じて専門 的 な検査 も考慮 すること。
5.2 下部 尿 路 閉塞 疾患 (前立腺 肥大 症 等 )を合併 している患者 では、それに対 する治療 (α 1遮断 薬 等 )を優先 させること。
5.3 過 活動 膀胱 の症状 を明確 に認識 できない認知 症 又 は認知 機能 障害 患者 は本 剤 の投与 対象 とはならない。
6. 用法 及 び用量
なお、
7. 用法 及 び用量 に関連 する注意
7.1 中等 度 の肝 機能 障害 患者 (Child-Pugh分類 B)への投与 は1日 1回 2.5mgから開始 し、慎重 に投与 する。投与 量 の上限 は1日 1回 5mgまでとする。軽度 の肝 機能 障害 患者 (Child-Pugh分類 A)への投与 は1日 1回 5mgから開始 し、増量 に際 しては副作用 発現 に留意 し、患者 の状態 を十分 に観察 しながら慎重 に行 うこと。[9.3.2、9.3.3、9.8参照 ]
8. 重要 な基本 的 注意
8.1 眼 調節 障害 (霧 視 等 )、傾 眠 が起 こることがあるので、高所 作業 、自動車 の運転 等 危険 を伴 う作業 に従事 する場合 には注意 させること。
8.2 本 剤 投与 により効果 が認 められない場合 には、漫然 と投与 せず、適切 な治療 を考慮 すること。
9. 特定 の背景 を有 する患者 に関 する注意
9.1 合併症 ・既往 歴 等 のある患者
9.1.1 排尿 困難 のある患者 (下部 尿 路 閉塞 疾患 (前立腺 肥大 症 等 )又 は排尿 筋 収縮 障害 等 )
9.1.2 下部 尿 路 閉塞 疾患 (前立腺 肥大 症 等 )を合併 している患者
9.1.3 QT延長 症候群 患者
9.1.4 潰瘍 性 大腸 炎 のある患者
9.1.5 甲状腺 機能 亢進 症 の患者
9.1.6 認知 症 又 は認知 機能 障害 のある患者
9.1.7 パーキンソン症状 又 は脳 血管 障害 のある患者
9.2 腎 機能 障害 患者
9.2.1 重度 の腎 機能 障害 患者 (クレアチニンクリアランス30mL/min未満 )
9.2.2 軽度 又 は中等 度 の腎 機能 障害 患者 (クレアチニンクリアランス30mL/min以上 かつ80mL/min以下 )
9.3 肝 機能 障害 患者
9.3.1 重度 の肝 機能 障害 患者 (Child-Pugh分類 C)
9.3.2 中等 度 の肝 機能 障害 患者 (Child-Pugh分類 B)
9.3.3 軽度 の肝 機能 障害 患者 (Child-Pugh分類 A)
9.5 妊 婦
9.6 授乳 婦
9.7 小児 等
9.8 高齢 者
10. 相互 作用
CYP3A4
10.2 併用 注意
フェノチアジン モノアミン | ||
| アゾール イトラコナゾール フルコナゾール ミコナゾール [16.7.1 | これらの | |
| リファンピシン フェニトイン カルバマゼピン | これらの | |
| QT [11.1.4、17.3.1 | QT | これらの |
11. 副作用
11.1 重大 な副作用
11.1.1 ショック、アナフィラキシー(いずれも頻度 不明 )
11.1.2 肝 機能 障害
AST、ALT、γ -GTP、Al-P、総 ビリルビンの上昇 (各 0.1〜5%未満 )等 を伴 う肝 機能 障害 があらわれることがある。
11.1.5 麻痺 性 イレウス(頻度 不明 )
11.1.6 幻覚 ・せん妄 (頻度 不明 )
11.1.7 急性 緑内障 発作 (頻度 不明 )
11.2 その他 の副作用
| 5% | 0.1〜5% | ||
| CK | |||
13. 過 量 投与
13.1 症状
13.2 処置
14. 適用 上 の注意
14.1 薬剤 交付 時 の注意
14.1.1 PTP包装 の薬剤 はPTPシートから取 り出 して服用 するよう指導 すること。PTPシートの誤 飲 により、硬 い鋭角 部 が食道 粘膜 へ刺 入 し、更 には穿孔 をおこして縦 隔 洞 炎 等 の重 篤 な合併症 を併発 することがある。
14.1.2 本 剤 をかみ砕 かないで服用 するよう患者 に指導 すること。本 剤 をかみ砕 いた際 にマスキング粒 が壊 れ、有効 成分 由来 の刺激 性 を感 じる可能 性 がある。
14.1.3 本 剤 は舌 の上 にのせて唾液 を浸潤 させると崩壊 するため、水 なしで服用 可能 である。また、水 で服用 することもできる。
14.1.4 本 剤 は寝 たままの状態 では、水 なしで服用 させないこと。
16. 薬物 動態
16.1 血 中 濃度
16.1.1 単 回 投与
(mg) | Cmax (ng/mL) | Tmax (h) | AUCinf (ng・h/mL) | t1/2 (h) | CL/F (L/h) | |
| 5 | 12 | 6.54±2.41 | 5.50±1.17 | 314.57±110.61 | 38.03±7.48 | 13.68±5.81 |
| 10 | 12 | 14.87±3.41 | 5.67±0.78 | 751.65±255.96 | 40.28±9.21 | 11.04±3.46 |
| 20 | 12 | 25.94±4.01 | 5.67±1.15 | 1,191.59±316.94 | 36.94±8.51 | 13.57±3.74 |
| 40 | 12 | 53.09±9.18 | 5.33±1.23 | 2,535.55±613.92 | 40.55±13.17 | 12.54±2.89 |
| 80 | 12 | 100.31±27.54 | 4.08±1.78 | 4,144.65±1,571.57 | 34.20±4.79 | 16.43±6.17 |
16.1.2 反復 投与
| Cmax (ng/mL) | Tmax (h) | AUC24h (ng・h/mL) | t1/2 (h) | CL/F (L/h) | ||
| 15 | 34.47±11.12 | 3.9±1.1 | 624.71±226.48 | 44.0±10.1 | 13.76±5.20 | |
| 14 | 37.57±18.31 | 5.2±1.4 | 732.82±375.83 | 39.2±9.1 | 12.83±5.71 | |
| 16 | 52.89±23.47 | 4.6±1.6 | 1,091.27±493.88 | 71.1±28.3 | 8.60±4.68 | |
| 16 | 53.82±10.27 | 5.6±1.8 | 1,095.61±213.19 | 61.3±13.1 | 7.18±1.69 |
16.1.3 過 活動 膀胱 患者
16.1.4 生物 学 的 同等 性 試験
| Cmax (ng/mL) | Tmax (h) | AUCinf (ng・h/mL) | t1/2 (h) | CL/F (L/h) | |
| ベシケアOD | 7.35±2.19 | 3.8±1.2 | 380.43±170.68 | 48.3±18.2 | 12.68±10.22 |
| ベシケア | 7.46±2.73 | 4.1±1.2 | 358.23±133.57 | 47.7±11.6 | 14.88±18.50 |
16.2 吸収
16.3 分布
16.4 代謝
16.5 排泄
14C標識 体 10mgを単 回 経口 投与 した後 、投与 量 の69.2%の放射 活性 が尿 中 に、22.5%が糞 中 に回収 された。尿 中 では投与 量 の15%未満 が未 変化 体 として排泄 され、17.8%がN-酸化 体 、8.9%が4R-水酸化 -N-酸化 体 、そして8.3%が4R-水酸化 体 としてそれぞれ排泄 された9)(外国 人 データ)。
16.6 特定 の背景 を有 する患者
16.6.1 腎 機能 障害 患者
16.6.2 肝 機能 障害 患者
16.6.3 高齢 者
16.7 薬物 相互 作用
17. 臨床 成績
17.1 有効 性 及 び安全 性 に関 する試験
17.1.1 国内 第 III相 試験
| プラセボ | 395 | −0.94 | 2.286 | −1.164 | −0.712 |
| ベシケア | 383 | −1.93 | 1.974 | −2.133 | −1.736 |
| ベシケア | 371 | −2.19 | 2.090 | −2.406 | −1.979 |
| プラセボ | 395 | −1.28 | 2.899 | −1.563 | −0.989 |
| ベシケア | 383 | −2.41 | 2.877 | −2.697 | −2.119 |
| ベシケア | 371 | −2.78 | 2.819 | −3.072 | −2.497 |
| プラセボ | 260 | −0.69 | 2.002 | −0.932 | −0.443 |
| ベシケア | 235 | −1.45 | 1.886 | −1.688 | −1.204 |
| ベシケア | 255 | −1.52 | 1.771 | −1.735 | −1.298 |
| プラセボ | 283 | −0.72 | 1.951 | −0.950 | −0.493 |
| ベシケア | 274 | −1.59 | 2.117 | −1.843 | −1.339 |
| ベシケア | 270 | −1.60 | 1.810 | −1.817 | −1.383 |
17.3 その他
17.3.1 QT間隔 に対 する影響
ベシケア錠 反復 投与 時 のQT間隔 に及 ぼす影響 を検討 することを目的 として、健康 成人 女性 86例 を対象 に二 重 盲 検 比較 対照 試験 を実施 した。ベシケア錠 10mg投与 時 の定常 状態 において、QT間隔 の変化 はプラセボと同 程度 であった。一方 、ベシケア錠 30mg投与 時 の定常 状態 、及 びモキシフロキサシン400mgの単 回 投与 時 においてQT間隔 の増加 が認 められた16)(外国 人 データ)。[2.7、9.1.3、10.2、11.1.4参照 ]
| QTc (msec) | 90% | ||
| コハク | 0 | −5 | 5 |
| コハク | 6 | 1 | 11 |
| モキシフロキサシン400mg/ | 10 | 6 | 13 |
18. 薬効 薬理
18.1 作用 機 序
18.2 ムスカリン受容 体 に対 する親和 性
18.3 ムスカリン受容 体 拮抗 作用
18.3.1 ラット及 びモルモット膀胱 平滑 筋 標本 を用 いた摘出 実験 において、カルバコール刺激 による収縮 に対 して濃度 依存 的 かつ競合 的 な拮抗 作用 を示 した。また、ラット及 びカニクイザルの膀胱 平滑 筋 細胞 及 び顎 下 腺 細胞 において、カルバコール刺激 による細胞 内 カルシウム濃度 上昇 に対 して濃度 依存 的 な抑制 作用 を示 したが、顎 下 腺 よりも膀胱 平滑 筋 に対 する抑制 作用 がそれぞれ3.6倍 及 び2.1倍 強 かった18)19)(in vitro)。
18.3.2 麻酔 ラットにおいて、カルバコール刺激 による膀胱 内 圧 上昇 及 び唾液 分泌 に対 して用量 依存 的 な抑制 作用 を示 した。膀胱 内 圧 上昇 及 び唾液 分泌 をそれぞれ30%及 び50%抑制 する用量 で比較 すると、唾液 分泌 よりも膀胱 内 圧 上昇 に対 する抑制 作用 がそれぞれ6.5倍 及 び3.7倍 強 かった18)(in vivo)。
18.4 排尿 機能 に対 する作用
19. 有効 成分 に関 する理化学 的 知見
19.1. コハク酸 ソリフェナシン
20. 取扱 い上 の注意
22. 包装
<ベシケアOD錠 2.5mg>
100錠 (10錠 ×10、乾燥 剤 入 り)、140錠 (14錠 ×10、乾燥 剤 入 り)
<ベシケアOD錠 5mg>
100錠 (10錠 ×10、乾燥 剤 入 り)、140錠 (14錠 ×10、乾燥 剤 入 り)、700錠 (14錠 ×50、乾燥 剤 入 り)
23. 主要 文献
-
田中 孝典 他 ,薬理 と治療 , 34 (Suppl.1), S5-S13, (2006) -
鈴木 真奈 絵 他 ,薬理 と治療 , 34 (Suppl.1), S29-S40, (2006) -
田中 孝典 他 ,薬理 と治療 , 34 (Suppl.1), S15-S27, (2006) -
山口 脩 他 ,薬理 と治療 , 34 (Suppl.1), S47-S68, (2006) -
社内 報告 書 :健康 成人 ・口腔 内 崩壊 錠 水 あり -
社内 報告 書 :健康 成人 ・口腔 内 崩壊 錠 水 なし - Kuipers,M.E.et al., Drugs in R&D., 5 (2), 73-81, (2004)
-
田中 孝典 他 ,薬理 と治療 , 34 (Suppl.1), S41-S45, (2006) -
社内 報告 書 :海外 健康 成人 ・代謝 (ベシケア錠 2006年 4月 20日 承認 CTD 2.7.6.6) - Smulders,R.A.et al., J.Pharmacol.Sci., 103 (1), 67-74, (2007) »PubMed »DOI
- Kuipers,M.et al., J.Pharmacol.Sci., 102 (4), 405-412, (2006) »PubMed »DOI
- Swart,P.J.et al., Basic Clin.Pharmacol.Toxicol., 99 (1), 33-36, (2006) »PubMed »DOI
-
社内 報告 書 :海外 健康 成人 ・相互 作用 (ベシケア錠 2006年 4月 20日 承認 CTD 2.7.6.12) - Yamaguchi,O.et al., BJU Int., 100 (3), 579-587, (2007) »PubMed »DOI
-
社内 報告 書 :国内 二 重 盲 検 群 間 比較 試験 (ベシケア錠 2006年 4月 20日 承認 CTD 2.7.4.7) -
社内 報告 書 :海外 健康 成人 ・二 重 盲 検 比較 対照 試験 (ベシケア錠 2006年 4月 20日 承認 CTD 2.7.6.17) - Ohtake,A.et al., Biol.Pharm.Bull., 30 (1), 54-58, (2007) »PubMed »DOI
- Ohtake,A.et al., Eur.J.Pharmacol., 492 (2-3), 243-250, (2004) »PubMed »DOI
- Kobayashi,S.et al., Life Sci., 74 (7), 843-853, (2004) »PubMed »DOI
- Suzuki,M.et al., Eur.J.Pharmacol., 512 (1), 61-66, (2005) »PubMed »DOI
24. 文献 請求 先 及 び問 い合 わせ先
アステラス製薬 株式会社
メディカルインフォメーションセンター
〒103-8411
東京 都 中央 区 日本橋 本町 2丁目 5番 1号
アステラス製薬 株式会社
メディカルインフォメーションセンター
〒103-8411
東京 都 中央 区 日本橋 本町 2丁目 5番 1号
26. 製造 販売 業者 等
26.1 製造 販売
アステラス製薬 株式会社