Alfa-heliks

Alpha heliks (
Alfa-heliks naziva se i klasično kao Pauling-Corey-Bransonov
Među tipovima lokalne strukture u proteinima,
Otkriće
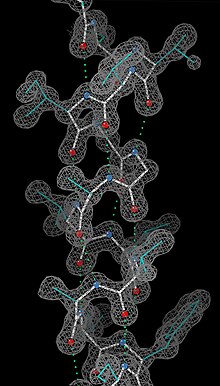
Dvije vodikove veze za istu peptidnu grupu istaknute su u magenta boji; udaljenost H do O je oko 2 Å . Lanac proteina ovdje ide prema gore, odnosno njegov N-kraj nalazi se na dnu, a C-kraj na vrhu.
Bočni lanci (crni stubovi) blago su nagnuti prema dolje, prema N-kraju, dok se peptidni kisici (crveni) usmjeravaju prema gore, a peptidni NH (plavi sa sivim kvržicama) prema dolje.
Ranih 1930-ih, William Astbury pokazao je da je došlo do drastičnih promjena u rendgenskom snimanju difrakcije vlakana vlažne vune ili vlakana kose, nakon značajnog istezanja. Podaci sugeriraju da su nerazvučena vlakna imala smotanu molekulsku strukturu s karakterističnim ponavljanjem ≈ 5,1 Å.
Astbury je za vlakna u početku predložio strukturu previjenog lanca. Kasnije se pridružio drugim istraživačima (posebno američkom hemičaru Mauriceu Hugginsu) predlažući da su:
- nerazvučene molekule proteina tvorile heliks (koju je nazvao
α -oblik) - zbog istezanja spirala se odmotala, formirajući produženo stanje (koje je nazvao
β -oblik).
Iako netačni u svim pojedinostima, Astburyjevi modeli ovih oblika bili su u biti tačni i odgovaraju modernim elementima sekundarne strukture,
Dva ključna razvojma koraka u modeliranju suvremene strukture
Struktura
Zbog svoje strukture, sa izuzetkom biljnog GCR2, svi receptori povezani sa G-proteinima pripadaju nadporodici heptaheliksnim transmembranski proteinima (uobičajeni sinonimi: sedam receptora za transmembranski domen, 7-TM receptori i heptahelskiki receptori). Sastoje se od podjedinice sa sedam (grčki hepta) (transmembranskih) heliksnih struktura, koje obuhvataju ćelijsku membranu i povezane su s tri unutarćelijske i tri vanćelijske petlje. Receptori povezani sa G-proteinima imaju vanćelijski ili transmembranski domen vezanja za ligande. G-protein se veže za ćelijsku unutrašnju (unutarćelijsku) stranu receptora. Kako bi se međusobno upoređivale strukture različitih receptora povezanih sa G-proteinima, razvijen je Ballesteros-Weinsteinov sistem nomenklature.
Dugo vremena, struktura receptora povezanih sa G-proteinima mogla se predvidjeti samo na osnovu analogije sa poznatom strukturom bakterijrskog rodopsina. Trodimenzijsko utvrđivanje strukture receptora vezanog za G-protein kod kičmenjaka, rodopsina domaće stoke postignuto je 2000. Godine, analizom rendgenske strukture.[8] S druge strane, kristalizacija i objašnjenje strukture ostalih receptora povezanih sa G-proteinima teža je, zbog njihovih fizičko-kemijskih svojstava i zbog male gustine receptora u membrani. Stoga je tek 2007. godine mogla biti utvrđena kristalna struktura ligandom aktiviranog receptora vezanog za G-protein (ljudski)
-
β 1–Adrenoceptor -
β 2–Adrenoceptor -
Histamin-H1–receptor
-
M2–acetilholinreceptor
-
A2A–adenozinreceptor
-
S1P1–receptor
-
CXCR1
-
CXCR4
-
PAR1
-
Neurotenzin-NTS1–receptor
U međuvremenu je uspostavljena trodimenzijska struktura, uključujući strukturu transmembranskih domena, za brojne receptore povezane sa G-proteinima, kao što je fiziološki i terapeutski važna klasa A. Struktura je uglavnom određena uz pomoć rentgenske kristalne analize, pomoću fuzijskih proteina ili metoda termičke stabilizacije. Na taj način, između ostalog, rtazjašnjena jwe struktura

Geometrija i vodikova veza
Aminokiseline u
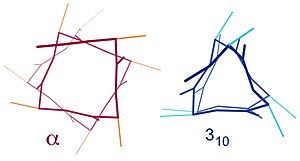
Slične strukture uključuju 310heliks (i 3 → i vodikova veza) i

Ostaci u
- 3 cos
Ω = 1 − 4 cos2φ +ψ /2
Stabilnost
Heliksi u proteinima mogu biti u rasponu od četiri do preko četrdeset ostataka, ali tipska spirala sadrži oko deset aminokiselina (oko tri zavoja). Općenito, kratki polipeptidi ne pokazuju puno
Eksperimentalno određivanje
Budući da je
Postoji nekoliko metoda niže rezolucije za dodjeljivanje opće spiralne strukture. Hemijski pomaci NMR-a (posebno C
Dugi homopolimeri aminokiselina često tvore helikse ako su topljivi. Tako duge, izolirane zavojnice mogu se otkriti i drugim metodima, kao što su dielektrična relaksacija, dvostruko lomljenje protoka i mjerenja konstantas|difuzijske konstante. Strožije rečeno, ovi metodi otkrivaju samo karakteristični prolat (duga cigara) hidrodinamični oblik zavojnice ili njen veliki dipolni moment.
Aminokiselinske sklonosti
Različite sekvence aminokiselina imaju različite sklonosti za formiranje
Standardne aminokiselinske sklonosti α -heliksa
Procijenjene razlike u slobodna energija,
Razlike u slobodnoj energiji, po ostatku[37]
Aminokiselina 3.
slovo1.
slovoHeliksni trošak kcal/mol kJ/mol Alanin Ala A 0.00 0.00 Arginin Arg R 0.21 0.88 Asparagin Asn N 0.65 2.72 Asparaginska kiselina Asp D 0.69 2.89 Cistein Cys C 0.68 2.85 Glutaminska kiselina Glu E 0.40 1.67 Glutamin Gln Q 0.39 1.63 Glicin Gly G 1.00 4.18 Histidin His H 0.61 2.55 Izoleucin Ile I 0.41 1.72 Leucin Leu L 0.21 0.88 Lizin Lys K 0.26 1.09 Metionin Met M 0.24 1.00 Fenilalanin Phe F 0.54 2.26 Prolin Pro P 3.16 13.22 Serin Ser S 0.50 2.09 Treonin Thr T 0.66 2.76 Triptofan Trp W 0.49 2.05 Tirozin Tyr Y 0.53 2.22 Valin Val V 0.61 2.55
Dipolni moment
Sveukupni dipolni moment
Namotane zavojnice
Zavojnice
Raspored lica
Aminokiseline koje čine određeni heliks mogu se ucrtati na spiralni točak, prikaz koji ilustrira orijentaciju sastavnih aminokiselina (takav dijagram potražite u članku za leucinski zatvarač. Često u loptastim proteinima, kao i u specijaliziranim strukturama, kao što su heliksi i leucinski zatvarač,
Promjene u orijentaciji vezanja javljaju se i kod facijski organiziranih oligopeptida. Ovaj obrazac je posebno čest kod antimikrobnih peptida, a napravljeni su mnogi modeli koji opisuju kako to utiče na njihovu funkciju. Zajedničko mnogim od njih je da hidrofobno lice antimikrobnog peptida stvara pore u plazemskoj membrani, nakon povezivanja sa masnim lancima u jezgru membrane.[41][42]
Sklopovi većih razmjera

Mioglobin i hemoglobin, prva dva proteina čije su strukture utvrđene rendgenskim kristalografskim snimkom imaju vrlo slične nabore koji čine oko 70%
Hemoglobin tada ima još veće razmjere kvaternarne strukture, u kojoj se funkcijska molekula koja veže kisik sastoji od četiri podjedinice.
Funkcija


Vezanje DNK
Raspon membrane
Mehanička svojstva
Dinamička svojstva
Alfa-heliksi u proteinima mogu imati niskofrekventno kretanje nalik harmonici, kako je uočeno u Ramanovoj spektroskopiji[46] i analizom putem kvazikontinuiranog modela.[47][48] Heliksi koji nisu stabilizirani tercijarnim interakcijama pokazuju dinamično ponašanje, što se uglavnom može pripisati habanju zavojnica s krajeva.[49]
Tranzicija heliks – namotaj
Homopolimeri aminokiselina (kao što je polilizin) mogu imati
U umjetnosti

Najmanje pet umjetnika u svom radu izričito se poziva na
Umjetnica iz San Francisca Julie Newdoll,[50] koja je diplomirala mikrobiologiju, iz oblasti „malih“ umjetnosti, specijalizirala se za slike inspirisane mikroskopskim snimcima i molekulama od 1990. Na njenoj slici "Uspon alfa-heliksa" (2003) nalaze se ljudske figure poredane u spiralnom aranžmanu. Prema umjetniku, "cvijeće odražava različite tipove bočnih lanaca koje svaka aminokiselina drži u svijetu".[50]
Julian Voss-Andreae je kipar njemačkog porijekla sa diplomom eksperimentalne fizike i skulpture. Od 2001. Voss-Andreae stvara "proteinske skulpture"[51] zasnovane na strukturi proteina, a
Trakasti dijagrami
Mike Tyka je računarski biohemičar na Univerzitetu u Washingtonu, koji radi sa Davidom Bakerom. Tyka izrađuje skulpture molekula proteina od 2010., od bakra i čelika, uključujući ubikvitin i tetramer kalijevog kanala.[54]

Institut za genetičko inženjerstvo i biotehnologiju u Sarajevu, od 2018. godine dodjeljuje stilizirani alfa heliks, kao najveću povremenu nagradu za doprinos razvoju i afirmaciji ove ustanove.
"Ingebov heliks 1988. je stilizirani metalni model strukture DNK na drvenom kvadarskom postolju, na koje se stavlja prigodna pločica sa logom Instituta i odgovarajućim podacima o zaslugama za priznanje i o njegovom dobitniku"[55]
Također pogledajte
Reference
- ^ Kendrew JC, Dickerson RE, Strandberg BE, Hart RG, Davies DR, Phillips DC, Shore VC (februar 1960). "Structure of myoglobin: A three-dimensional Fourier synthesis at 2 Å resolution". Nature. 185 (4711): 422–7. Bibcode:1960Natur.185..422K. doi:10.1038/185422a0. PMID 18990802.
- ^ Neurath H (1940). "Intramolecular folding of polypeptide chains in relation to protein structure". Journal of Physical Chemistry. 44 (3): 296–305. doi:10.1021/j150399a003.
- ^ Taylor HS (1942). "Large molecules through atomic spectacles". Proceedings of the American Philosophical Society. 85 (1): 1–12. JSTOR 985121.
- ^ Huggins M (1943). "The structure of fibrous proteins". Chemical Reviews. 32 (2): 195–218. doi:10.1021/cr60102a002.
- ^ Bragg WL, Kendrew JC, Perutz MF (1950). "Polypeptide chain configurations in crystalline proteins". Proceedings of the Royal Society of London. Series A. Mathematical and Physical Sciences. 203 (1074): 321–?. Bibcode:1950RSPSA.203..321B. doi:10.1098/rspa.1950.0142.
- ^ Pauling L, Corey RB, Branson HR (april 1951). "The structure of proteins; two hydrogen-bonded helical configurations of the polypeptide chain". Proceedings of the National Academy of Sciences of the United States of America. 37 (4): 205–11. Bibcode:1951PNAS...37..205P. doi:10.1073/pnas.37.4.205. PMC 1063337. PMID 14816373.
- ^ "The Nobel Prize in Chemistry 1954".
- ^ K. Palczewski, T. Kumasaka, T. Hori, C. A. Behnke, H. Motoshima, B. A. Fox, I. Le Trong, D. C. Teller, T. Okada, R. E. Stenkamp, M. Yamamoto, M. Miyano: Crystal structure of rhodopsin: A G protein-coupled receptor. In: Science. Band 289, Nummer 5480, August 2000, S. 739–745, PMID 10926528.
- ^ S. G. Rasmussen + (2007). "Crystal structure of the human
β 2 adrenergic G-protein-coupled receptor". Nature. 450 (7168): 383–387. PMID 17952055. - ^ V. Cherezov + (2007). "High-resolution crystal structure of an engineered human beta2-adrenergic G protein-coupled receptor". Science. 318 (5854): 1258–1265. PMID 17962520.
- ^ T. Warne +: Structure of a beta(1)-adrenergic G-protein-coupled receptor. Nature. 2008 Jun 25. Epub ahead of print, PMID 18594507
- ^ V Jaakola et al.: The 2.6Å Crystal Structure of a Human A2A Adenosine Receptor Bound to an Antagonist. In: Science, Epub 2008 Oct 2, PMID 18832607
- ^ PDB: 3PBL Structure Summary
- ^ H. Wu + (2012). "Structure of the human
κ -opioid receptor in complex with JDTic". Nature. 485 (7398): 327–332. doi:10.1038/nature10939. PMID 22437504. - ^ A Manglik et al. (2012) PMID 22437502
- ^ S. Granier et + (2012) PMID 22596164
- ^ A. A. Thompson, W. Liu, E. Chun, V. Katritch, H. Wu, E. Vardy, X. P. Huang, C. Trapella, R. Guerrini, G. Calo, B. L. Roth, V. Cherezov, R. C. Stevens: Structure of the nociceptin/orphanin FQ receptor in complex with a peptide mimetic. In: Nature. Band 485, Nummer 7398, Mai 2012, S. 395–399, doi:10.1038/nature11085, PMID 22596163.
- ^ M. A. Hanson + (2012). "Crystal structure of a lipid G protein-coupled receptor". Science. 335 (6070): 851–855. doi:10.1126/science.1215904. PMID 22344443.
- ^ K. Haga + (2012). "Structure of the human M2 muscarinic acetylcholine receptor bound to an antagonist". Nature. 482 (7386): 547–551. doi:10.1038/nature10753. PMID 22278061.
- ^ A. C. Kruse, J. Hu, A. C. Pan, D. H. Arlow, D. M. Rosenbaum, E. Rosemond, H. F. Green, T. Liu, P. S. Chae, R. O. Dror, D. E. Shaw, W. I. Weis, J. Wess, B. K. Kobilka: Structure and dynamics of the M3 muscarinic acetylcholine receptor. In: Nature. Band 482, Nummer 7386, Februar 2012, S. 552–556, doi:10.1038/nature10867, PMID 22358844.
- ^ T. Shimamura + (2012). "Structure of the human histamine H1 receptor in complex with doxepin". Nature. 475 (7354): 65–70. doi:10.1038/nature10236. PMID 21697825.
- ^ C. Wang, Y. Jiang, J. Ma + (2013). "Structural Basis for Molecular Recognition at Serotonin Receptors". Science. doi:10.1126/science.1232807. PMID 23519210.CS1 održavanje: više imena: authors list (link)
- ^ Dunitz J (2001). "Pauling's Left-Handed
α -Helix". Angewandte Chemie International Edition. 40 (22): 4167–4173. doi:10.1002/1521-3773(20011119)40:22<4167::AID-ANIE4167>3.0.CO;2-Q. PMID 29712120. - ^ IUPAC-IUB Commission on Biochemical Nomenclature (1970). "Abbreviations and symbols for the description of the conformation of polypeptide chains". Journal of Biological Chemistry. 245: 6489–6497.
- ^ "Polypeptide Conformations 1 and 2". www.sbcs.qmul.ac.uk. Pristupljeno 5. 11. 2018.
- ^ Kabsch W, Sander C (decembar 1983). "Dictionary of protein secondary structure: pattern recognition of hydrogen-bonded and geometrical features". Biopolymers. 22 (12): 2577–637. doi:10.1002/bip.360221211. PMID 6667333.
- ^ a b Richardson JS (1981). "The anatomy and taxonomy of protein structure". Advances in Protein Chemistry. 34: 167–339. doi:10.1016/S0065-3233(08)60520-3. ISBN 9780120342341. PMID 7020376.
- ^ Lovell SC, Davis IW, Arendall WB, de Bakker PI, Word JM, Prisant MG, Richardson JS, Richardson DC (februar 2003). "Structure validation by Calpha geometry: phi,psi and Cbeta deviation". Proteins. 50 (3): 437–50. doi:10.1002/prot.10286. PMID 12557186.
- ^ Dickerson RE, Geis I (1969), Structure and Action of Proteins, Harper, New York
- ^ Zorko, Matjaž (2010). "Structural Organization of Proteins". u Langel, Ülo; Cravatt, Benjamin F.; Gräslund, Astrid; von Heijne, Gunnar; Land, Tiit; Niessen, Sherry; Zorko, Matjaž (ured.). Introduction to Peptides and Proteins. Boca Raton: CRC Press. str. 36–57. ISBN 9781439882047.
- ^ Terwilliger TC (mart 2010). "Rapid model building of alpha-helices in electron-density maps". Acta Crystallographica Section D. 66 (Pt 3): 268–75. doi:10.1107/S0907444910000314. PMC 2827347. PMID 20179338.
- ^ Hudgins RR, Jarrold MF (1999). "Helix Formation in Unsolvated Alanine-Based Peptides: Helical Monomers and Helical Dimers". Journal of the American Chemical Society. 121 (14): 3494–3501. doi:10.1021/ja983996a.
- ^ Kutchukian PS, Yang JS, Verdine GL, Shakhnovich EI (april 2009). "All-atom model for stabilization of alpha-helical structure in peptides by hydrocarbon staples". Journal of the American Chemical Society. 131 (13): 4622–7. doi:10.1021/ja805037p. PMC 2735086. PMID 19334772.
- ^ Abrusan G, Marsh JA (2016). "Alpha helices are more robust to mutations than beta strands". PLOS Computational Biology. 12 (12): e1005242. Bibcode:2016PLSCB..12E5242A. doi:10.1371/journal.pcbi.1005242. PMC 5147804. PMID 27935949.
- ^ Rocklin GJ, et al. (2017). "Global analysis of protein folding using massively parallel design, synthesis, and testing". Science. 357 (6347): 168–175. Bibcode:2017Sci...357..168R. doi:10.1126/science.aan0693. PMC 5568797. PMID 28706065.
- ^ Pace CN, Scholtz JM (juli 1998). "A helix propensity scale based on experimental studies of peptides and proteins". Biophysical Journal. 75 (1): 422–7. Bibcode:1998BpJ....75..422N. doi:10.1016/S0006-3495(98)77529-0. PMC 1299714. PMID 9649402.
- ^ Pace, C. Nick; Scholtz, J. Martin (1998). "A Helix Propensity Scale Based on Experimental Studies of Peptides and Proteins". Biophysical Journal. 75. str. 422–427. Bibcode:1998BpJ....75..422N. doi:10.1016/s0006-3495(98)77529-0.
- ^ Hol WG, van Duijnen PT, Berendsen HJ (1978). "The alpha helix dipole and the properties of proteins". Nature. 273 (5662): 443–446. Bibcode:1978Natur.273..443H. doi:10.1038/273443a0. PMID 661956.
- ^ He JJ, Quiocho FA (oktobar 1993). "Dominant role of local dipoles in stabilizing uncompensated charges on a sulfate sequestered in a periplasmic active transport protein". Protein Science. 2 (10): 1643–7. doi:10.1002/pro.5560021010. PMC 2142251. PMID 8251939.
- ^ Milner-White EJ (novembar 1997). "The partial charge of the nitrogen atom in peptide bonds". Protein Science. 6 (11): 2477–82. doi:10.1002/pro.5560061125. PMC 2143592. PMID 9385654.
- ^ Kohn, Eric M.; Shirley, David J.; Arotsky, Lubov; Picciano, Angela M.; Ridgway, Zachary; Urban, Michael W.; Carone, Benjamin R.; Caputo, Gregory A. (4. 2. 2018). "Role of Cationic Side Chains in the Antimicrobial Activity of C18G". Molecules (jezik: engleski). 23 (2): 329. doi:10.3390/molecules23020329. PMC 6017431. PMID 29401708.
- ^ Toke, Orsolya (2005). "Antimicrobial peptides: new candidates in the fight against bacterial infections". Biopolymers. 80 (6): 717–735. doi:10.1002/bip.20286. ISSN 0006-3525. PMID 15880793.
- ^ Branden & Tooze, poglavlje 10
- ^ Branden & Tooze, chapter 12.
- ^ Ackbarow T, Chen X, Keten S, Buehler MJ (oktobar 2007). "Hierarchies, multiple energy barriers, and robustness govern the fracture mechanics of alpha-helical and beta-sheet protein domains". Proceedings of the National Academy of Sciences of the United States of America. 104 (42): 16410–5. Bibcode:2007PNAS..10416410A. doi:10.1073/pnas.0705759104. PMC 2034213. PMID 17925444.
- ^ Painter PC, Mosher LE, Rhoads C (juli 1982). "Low-frequency modes in the Raman spectra of proteins". Biopolymers. 21 (7): 1469–72. doi:10.1002/bip.360210715. PMID 7115900.
- ^ Chou KC (decembar 1983). "Identification of low-frequency modes in protein molecules". The Biochemical Journal. 215 (3): 465–9. doi:10.1042/bj2150465. PMC 1152424. PMID 6362659.
- ^ Chou KC (maj 1984). "Biological functions of low-frequency vibrations (phonons). III. Helical structures and microenvironment". Biophysical Journal. 45 (5): 881–9. Bibcode:1984BpJ....45..881C. doi:10.1016/S0006-3495(84)84234-4. PMC 1434967. PMID 6428481.
- ^ Fierz B, Reiner A, Kiefhaber T (januar 2009). "Local conformational dynamics in alpha-helices measured by fast triplet transfer". Proceedings of the National Academy of Sciences of the United States of America. 106 (4): 1057–62. Bibcode:2009PNAS..106.1057F. doi:10.1073/pnas.0808581106. PMC 2633579. PMID 19131517.
- ^ a b "Julie Newdoll Scientifically Inspired Art, Music, Board Games". www.brushwithscience.com. Pristupljeno 6. 4. 2016.
- ^ Voss-Andreae J (2005). "Protein Sculptures: Life's Building Blocks Inspire Art". Leonardo. 38: 41–45. doi:10.1162/leon.2005.38.1.41.
- ^ Grossman, Bathsheba. "About the Artist". Bathsheba Sculpture. Pristupljeno 6. 4. 2016.
- ^ "About". molecularsculpture.com. Pristupljeno 6. 4. 2016.
- ^ Tyka, Mike. "About". www.miketyka.com. Pristupljeno 6. 4. 2016.
- ^ Pravilnik o priznanjima i nagradama instituta za genetičko inženjerstvo i biotehnologiju, Sarajevo, 2018.
Dopunska literatura
- Tooze, John; Brändén, Carl-Ivar (1999). Introduction to protein structure. New York: Garland Pub. ISBN 0-8153-2304-2..
- Eisenberg D (septembar 2003). "The discovery of the alpha-helix and beta-sheet, the principal structural features of proteins". Proceedings of the National Academy of Sciences of the United States of America. 100 (20): 11207–10. Bibcode:2003PNAS..10011207E. doi:10.1073/pnas.2034522100. PMC 208735. PMID 12966187.
- Astbury, WT; Woods, HJ (1931). "The Molecular Weights of Proteins". Nature. 127 (3209): 663–665. Bibcode:1931Natur.127..663A. doi:10.1038/127663b0.
- Astbury, WT; Street, A (1931). "X-ray studies of the structures of hair, wool and related fibres. I. General". Trans. R. Soc. Lond. A230: 75–101. Bibcode:1932RSPTA.230...75A. doi:10.1098/rsta.1932.0003.
- Astbury, WT (1933). "Some Problems in the X-ray Analysis of the Structure of Animal Hairs and Other Protein Fibers". Trans. Faraday Soc. 29 (140): 193–211. doi:10.1039/tf9332900193.
- Astbury, WT; Woods, HJ (1934). "X-ray studies of the structures of hair, wool and related fibres. II. The molecular structure and elastic properties of hair keratin". Philosophical Transactions of the Royal Society of London Series A. 232 (707–720): 333–394. Bibcode:1934RSPTA.232..333A. doi:10.1098/rsta.1934.0010.
- Astbury, WT; Sisson, WA (1935). "X-ray studies of the structures of hair, wool and related fibres. III. The configuration of the keratin molecule and its orientation in the biological cell". Proceedings of the Royal Society. A150 (871): 533–551. Bibcode:1935RSPSA.150..533A. doi:10.1098/rspa.1935.0121.
- Sugeta, H; Miyazawa, T (1967). "General Method for Calculating Helical Parameters of Polymer Chains from Bond Lengths, Bond Angles, and Internal-Rotation Angles". Biopolymers. 5 (7): 673–679. doi:10.1002/bip.1967.360050708.
- Wada A (1976). "The alpha-helix as an electric macro-dipole". Advances in Biophysics: 1–63. PMID 797240.
- Chothia C, Levitt M, Richardson D (oktobar 1977). "Structure of proteins: packing of alpha-helices and pleated sheets". Proceedings of the National Academy of Sciences of the United States of America. 74 (10): 4130–4. Bibcode:1977PNAS...74.4130C. doi:10.1073/pnas.74.10.4130. PMC 431889. PMID 270659.
- Chothia C, Levitt M, Richardson D (januar 1981). "Helix to helix packing in proteins". Journal of Molecular Biology. 145 (1): 215–50. doi:10.1016/0022-2836(81)90341-7. PMID 7265198.
- Hol WG (1985). "The role of the alpha-helix dipole in protein function and structure". Progress in Biophysics and Molecular Biology. 45 (3): 149–95. doi:10.1016/0079-6107(85)90001-X. PMID 3892583.
- Barlow DJ, Thornton JM (juni 1988). "Helix geometry in proteins". Journal of Molecular Biology. 201 (3): 601–19. doi:10.1016/0022-2836(88)90641-9. PMID 3418712.
- Murzin AG, Finkelstein AV (decembar 1988). "General architecture of the alpha-helical globule". Journal of Molecular Biology. 204 (3): 749–69. doi:10.1016/0022-2836(88)90366-X. PMID 3225849.