Ugljikovodici: razlika između inačica
m Bot: standardizacija |
mNema sažetka uređivanja |
||
| (Nije prikazano 50 međuinačica 38 suradnika) | |||
| Redak 4: | Redak 4: | ||
[[Datoteka:Kalottenmodell Benzol.png|mini|[[Benzen]] - predstavnik [[aren]]a]] |
[[Datoteka:Kalottenmodell Benzol.png|mini|[[Benzen]] - predstavnik [[aren]]a]] |
||
'''Ugljikovodici''' su [[organska kemija|organski kemijski]] spojevi [[ugljik]]a i [[vodik]]a. Sastoje se od "kostura" [[atom]]a ugljika na koje su vezani atomi vodika (i drugih [[kemijski elementi|elemenata]]). |
'''Ugljikovodici''' su najjednostavniji [[organska kemija|organski kemijski]] spojevi koji u svojim molekulama sadrže samo atome [[ugljik]]a i atome [[vodik]]a. Sastoje se od "kostura" [[atom]]a ugljika na koje su vezani atomi vodika (i drugih [[kemijski elementi|elemenata]]). |
||
[[Nafta]] i [[Prirodni plin|zemni plin]] tvari su koje u svojem najvećem dijelu sadržavaju ugljikovodike. |
|||
== Podjela == |
== Podjela == |
||
| Redak 10: | Redak 12: | ||
Ugljikovodici se dijele prema obliku ugljikovog "kostura", dalje uglavnom po zasićenosti. |
Ugljikovodici se dijele prema obliku ugljikovog "kostura", dalje uglavnom po zasićenosti. |
||
* '''aciklički (alifatski)''' - atomi ugljika čine lančaste [[molekule]]. |
* '''aciklički (alifatski)''' - atomi ugljika čine lančaste [[molekule]]. Taj lanac može biti i razgranat. |
||
** '''zasićeni |
** '''zasićeni''' |
||
*** '''[[alkani]]''' (C<sub>n</sub>H<sub>2n+2</sub>) - atomi ugljika su vezani samo jednostrukom [[kovalentna veza|kovalentnom vezom]]. |
|||
** '''nezasićeni''' |
** '''nezasićeni''' |
||
*** ''[[alkeni]]'' - |
*** ''[[alkeni]]'' (C<sub>n</sub>H<sub>2n</sub>) - između barem dva atoma ugljika postoji dvostruka kovalentna veza. |
||
*** ''[[alkini]]'' - |
*** ''[[alkini]]'' (C<sub>n</sub>H<sub>2n-2</sub>) - između barem dva atoma ugljika postoji trostruka kovalentna veza. |
||
* '''ciklički''' - atomi ugljika čine prstenaste molekule. |
* '''ciklički''' - atomi ugljika čine prstenaste molekule. |
||
** '''karbociklički''' - prsten je građen samo od atoma ugljika. |
** '''karbociklički''' - prsten je građen samo od atoma ugljika. |
||
*** ''zasićeni |
*** ''zasićeni'' |
||
**** ''[[cikloalkani]]'' - atomi ugljika su vezani samo jednostrukom kovalentnom vezom. |
|||
*** ''nezasićeni |
*** ''nezasićeni'' |
||
**** ''[[cikloalkeni]]'' - osim jednostruke, između atoma ugljika postoji i dvostruka kovalentna veza. |
|||
*** '' |
**** ''[[cikloalkeni|cikloalkini]]'' - osim jednostruke, između atoma ugljika postoji i trostruka kovalentna veza. |
||
*** ''aromatski'' |
|||
**** ''[[areni]]'' - u prstenu su jednostruka i dvostruka kovalentna veza poredane naizmjenično. |
|||
** '''heterociklički''' - u prstenu postoje i drugi atomi (koji se nazivaju heteroatomima) osim atoma ugljika (npr. atom [[kisik]]a, [[dušik]]a, [[sumpor]]a...). |
** '''heterociklički''' - u prstenu postoje i drugi atomi (koji se nazivaju heteroatomima) osim atoma ugljika (npr. atom [[kisik]]a, [[dušik]]a, [[sumpor]]a...). |
||
| Redak 26: | Redak 33: | ||
'''Aromatski ugljikovodici''' (naziv dolazi od grčkog ''[[aroma]]'' (miris)). |
'''Aromatski ugljikovodici''' (naziv dolazi od grčkog ''[[aroma]]'' (miris)). |
||
U [[19. stoljeće|19.st.]] |
U [[19. stoljeće|19.st.]] [[:en:August_Kekulé|Friedrich August Kekule von Stradonitz]] otkriva strukturu [[benzen]]a. Navodno je njegovu strukturu sanjao. Benzen je kancerogen, ali se nalazi u veoma mnogo spojeva. Čak i poznati lijek Aspirin u sebi sadrži benzensku jezgru. |
||
Molekulska formula benzena je C<sub>6</sub>H<sub>6</sub>, a izvori su [[katran]] kamenog [[ugljen]]a, [[nafta]]. |
Molekulska formula benzena je C<sub>6</sub>H<sub>6</sub>, a izvori su [[katran]] kamenog [[ugljen]]a, [[nafta]]. |
||
H |
|||
| |
| |
||
C |
C |
||
| Redak 39: | Redak 46: | ||
C |
C |
||
| |
| |
||
H |
|||
Poznatiji aromatski ugljikovodici: [[antracen]] i [[naftalen]]. |
Poznatiji aromatski ugljikovodici: [[antracen]] i [[naftalen]]. |
||
== Reakcije ugljikovodika == |
== Reakcije ugljikovodika == |
||
=== Alkani === |
|||
Alkani nisu izrazito reaktivni spojevi jer nemaju izrazito reaktivnih funkcionalnih skupina (u alkana je relativno stabilan vodik). |
|||
Najčešće reakcija alkana je oksidacija odnosno [[gorenje]]. Svrha joj je dobivanje toplinske [[Energija|energije]] koja se oslobađa pri gorenju. |
|||
Druga reakcija koje je moguća u alkana je supstitucija. |
|||
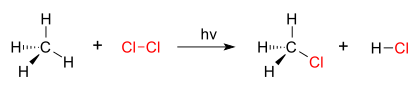
*[[Supstitucija (kemija)|Supstitucija]] - reakcije supstitucije ili zamjene su reakcije zasićenih i aromatskih ugljikovodika pri čemu se atom vodika iz molekule zamjenjuje atomom drugog elementa ili drugom skupinom, pri veoma jakoj svjetlosti. |
*[[Supstitucija (kemija)|Supstitucija]] - reakcije supstitucije ili zamjene su reakcije zasićenih i aromatskih ugljikovodika pri čemu se atom vodika iz molekule zamjenjuje atomom drugog elementa ili drugom skupinom, pri veoma jakoj svjetlosti. |
||
{| class="wikitable" |
|||
|- align="center" |
|||
|| |
|||
[[Slika:SubstitutionReaction.svg|Reakcija supstitucije smjese klora i metana]] |
|||
|- align="center" |
|||
!reakcija supstitucije smjese klora i metana |
|||
|} |
|||
=== Alkeni i alikini === |
|||
Tipične reakcije alkena i alkina su reakcije adicije, ali i oksidacije dok su komercijalno najvažnije reakcije [[Polimerizacija|polimerizacije]]. |
|||
Postoji više vrsta adicije kao što su : adicija vodika - hidrogeniranje, adicija vode - hidratiranje, adicija halogena - [[halogeniranje]], adicija halogenvodika - hidrogenhalogeniranje. |
|||
*[[ Adicija]] ([[latinski|lat.]] ''additio'' - dodavanje, pribrajanje). U organskoj kemiji, vezivanje vodikovih atoma, atoma drugih elemenata ili radikala, te odvajanje na dvostruke ili trostruke veze nezasićenih [[Organski spojevi|organskih spojeva]]. |
|||
{| class="wikitable" |
|||
|- align="center" |
|||
|| |
|||
[[Slika:Chlorine addition to ethene.svg|300px]] |
|||
|- align="center" |
|||
!reakcija adicije klora na eten |
|||
|} |
|||
{{commons|Gallery Hydrocarbons}} |
{{commons|Gallery Hydrocarbons}} |
||
| Redak 50: | Redak 84: | ||
{{Mrva-kem}} |
{{Mrva-kem}} |
||
== Vanjske poveznice == |
|||
| ⚫ | |||
* {{HTE|ugljikovodici|Ugljikovodici}} |
|||
| ⚫ | |||
[[ar:هيدروكربون]] |
|||
[[bg:Въглеводород]] |
|||
[[ca:Hidrocarbur]] |
|||
[[cs:Uhlovodíky]] |
|||
[[cy:Hydrocarbon]] |
|||
[[da:Kulbrinte]] |
|||
[[de:Kohlenwasserstoffe]] |
|||
[[el:Υδρογονάνθρακες]] |
|||
[[en:Hydrocarbon]] |
|||
[[eo:Hidrokarbono]] |
|||
[[es:Hidrocarburo]] |
|||
[[et:Süsivesinikud]] |
|||
[[fa:هیدروکربن]] |
|||
[[fi:Hiilivety]] |
|||
[[fr:Hydrocarbure]] |
|||
[[ga:Hidreacarbón]] |
|||
[[gl:Hidrocarburo]] |
|||
[[he:פחמימן]] |
|||
[[hi:हाइड्रोकार्बन]] |
|||
[[id:Hidrokarbon]] |
|||
[[io:Hidrokarbido]] |
|||
[[is:Kolvetni]] |
|||
[[it:Idrocarburi]] |
|||
[[ja: |
|||
[[kk:Көмірсулар]] |
|||
[[ko:탄화수소]] |
|||
[[lt:Angliavandenilis]] |
|||
[[lv:Ogļūdeņraži]] |
|||
[[mk:Јаглеводород]] |
|||
[[mn:Нүүрсустөрөгч]] |
|||
[[ms:Hidrokarbon]] |
|||
[[nl:Koolwaterstof]] |
|||
[[nn:Hydrokarbon]] |
|||
[[no:Hydrokarbon]] |
|||
[[pl:Węglowodory]] |
|||
[[pt:Hidrocarboneto]] |
|||
[[ro:Hidrocarbură]] |
|||
[[ru:Углеводороды]] |
|||
[[simple:Hydrocarbon]] |
|||
[[sk:Uhľovodík]] |
|||
[[sl:Ogljikovodik]] |
|||
[[sr:Угљоводоник]] |
|||
[[su:Hidrokarbon]] |
|||
[[sv:Kolväte]] |
|||
[[ta:ஹைடிரோகார்பன்]] |
|||
[[th:ไฮโดรคาร์บอน]] |
|||
[[tr:Hidrokarbon]] |
|||
[[uk:Вуглеводні]] |
|||
[[vi:Hyđrocacbon]] |
|||
[[zh:烃]] |
|||
Posljednja izmjena od 23. svibanj 2023. u 23:16



Ugljikovodici su najjednostavniji organski kemijski spojevi koji u svojim molekulama sadrže samo atome ugljika i atome vodika. Sastoje se od "kostura" atoma ugljika na koje su vezani atomi vodika (i drugih elemenata).
Nafta i zemni plin tvari su koje u svojem najvećem dijelu sadržavaju ugljikovodike.
Ugljikovodici se dijele prema obliku ugljikovog "kostura", dalje uglavnom po zasićenosti.
- aciklički (alifatski) - atomi ugljika čine lančaste molekule. Taj lanac može biti i razgranat.
- zasićeni
- alkani (CnH2n+2) - atomi ugljika su vezani samo jednostrukom kovalentnom vezom.
- nezasićeni
- zasićeni
- ciklički - atomi ugljika čine prstenaste molekule.
- karbociklički - prsten je građen samo od atoma ugljika.
- zasićeni
- cikloalkani - atomi ugljika su vezani samo jednostrukom kovalentnom vezom.
- nezasićeni
- cikloalkeni - osim jednostruke, između atoma ugljika postoji i dvostruka kovalentna veza.
- cikloalkini - osim jednostruke, između atoma ugljika postoji i trostruka kovalentna veza.
- aromatski
- areni - u prstenu su jednostruka i dvostruka kovalentna veza poredane naizmjenično.
- zasićeni
- heterociklički - u prstenu postoje i drugi atomi (koji se nazivaju heteroatomima) osim atoma ugljika (npr. atom kisika, dušika, sumpora...).
- karbociklički - prsten je građen samo od atoma ugljika.
Aromatski ugljikovodici (naziv dolazi od grčkog aroma (miris)).
U 19.st. Friedrich August Kekule von Stradonitz otkriva strukturu benzena. Navodno je njegovu strukturu sanjao. Benzen je kancerogen, ali se nalazi u veoma mnogo spojeva. Čak i poznati lijek Aspirin u sebi sadrži benzensku jezgru. Molekulska formula benzena je C6H6, a izvori su katran kamenog ugljena, nafta.
H
|
C
/ \
H-C C-H
| |
H-C C-H
\ /
C
|
H
Poznatiji aromatski ugljikovodici: antracen i naftalen.
Alkani nisu izrazito reaktivni spojevi jer nemaju izrazito reaktivnih funkcionalnih skupina (u alkana je relativno stabilan vodik).
Najčešće reakcija alkana je oksidacija odnosno gorenje. Svrha joj je dobivanje toplinske energije koja se oslobađa pri gorenju.
Druga reakcija koje je moguća u alkana je supstitucija.
- Supstitucija - reakcije supstitucije ili zamjene su reakcije zasićenih i aromatskih ugljikovodika pri čemu se atom vodika iz molekule zamjenjuje atomom drugog elementa ili drugom skupinom, pri veoma jakoj svjetlosti.
| reakcija supstitucije smjese klora i metana |
|---|
Tipične reakcije alkena i alkina su reakcije adicije, ali i oksidacije dok su komercijalno najvažnije reakcije polimerizacije.
Postoji više vrsta adicije kao što su : adicija vodika - hidrogeniranje, adicija vode - hidratiranje, adicija halogena - halogeniranje, adicija halogenvodika - hidrogenhalogeniranje.
- Adicija (lat. additio - dodavanje, pribrajanje). U organskoj kemiji, vezivanje vodikovih atoma, atoma drugih elemenata ili radikala, te odvajanje na dvostruke ili trostruke veze nezasićenih organskih spojeva.
| reakcija adicije klora na eten |
|---|
| U G LJ I K O V O D I C I | |||||
| aciklički | ciklički | ||||
| ZASIĆENI | NEZASIĆENI | KARBOCIKLIČKI | HETEROCIKLIČKI | ||
| alkani | alkeni alkini |
zasićeni | nezasićeni | aromatski | |
| cikloalkani | cikloalkeni | areni | |||
- Ugljikovodici Hrvatska tehnička enciklopedija, portal hrvatske tehničke baštine. LZMK