Lysine
| L-Lysine | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
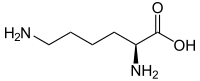
▵ Structuurformule van L-lysine
| ||||

| ||||
▵ Molecuulmodel van L-lysine
| ||||
| Algemeen | ||||
| Molecuulformule | C6H14N2O2 | |||
| IUPAC-naam | Lysine | |||
| Molmassa | 146,18756 g/mol | |||
| CAS-nummer | 56-87-1 | |||
| EG-nummer | 200-294-2 | |||
| PubChem | 5962 | |||
| Wikidata | Q178430 | |||
| Beschrijving | Witachtig poeder | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Smeltpunt | 224 °C | |||
| Oplosbaarheid in water | 300 g/L | |||
| Goed oplosbaar in | water | |||
| Evenwichtsconstante(n) | pKz1 (carboxyl) = 2,20[1] pKz2, ( | |||
| Nutritionele eigenschappen | ||||
| Essentieel? | Ja | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Lysine (afgekort als Lys, K) is een natuurlijk voorkomend aminozuur met een basisch karakter. Het is een van de twintig
Lysine wordt geclassificeerd als een voor mens en dier essentieel aminozuur: het kan enkel uit voeding worden verkregen. Lysine is vooral aanwezig in dierlijke producten (vlees, vis en gevogelte). In mindere mate komt het voor in eieren, peulvruchten en zuivelproducten.[2] Naast eiwitsynthese is lysine van belang bij de versteviging van collageen en de vorming van carnitine voor vetzuursynthese. Lysine is eveneens betrokken bij de modificatie van histonen en daarmee in de regulering van epigenetische processen.
Een tekort aan lysine kan bij de mens leiden tot verschillende ziekten, waaronder defecte bindweefsels, verminderde vetzuurstofwisseling, bloedarmoede en systemische eiwit-energie-deficiëntie.[3][4] Een overvloed aan lysine in het lichaam, bijvoorbeeld door een ineffectieve afbraak, kan daarentegen ook gevaarlijke ziekteprocessen tot gevolg hebben, waaronder neurologische problemen.[5]
Biosynthese[bewerken | brontekst bewerken]
Planten en micro-organismen kunnen lysine de novo synthetiseren uit eenvoudige precursors. Er zijn twee biosyntheseroutes ontdekt die starten uit de verbindingen
Eigenschappen[bewerken | brontekst bewerken]
Lysine is een relatief groot aminozuur met een eenvoudige structuur. Mensen en dieren kunnen het zelf niet maken en moeten het daarom uit hun voeding opnemen. Het behoort daarom tot de essentiële aminozuren. Varkens, kippen en runderen krijgen lysine bijvoorbeeld als voedersupplement.[6]
Lysine vertoont, net als de meeste andere aminozuren (behalve glycine), optische isomerie waardoor twee configuraties van het lysinemolecule mogelijk zijn: D (Dextro) en L (Laevo). Alleen de L-vorm is fysiologisch actief.[2]
De algemene formule R-CH(NH2)-COOH waarbij R=-CH2-CH2-CH2-CH2-NH2.
Toepassingen[bewerken | brontekst bewerken]
Het overgrote deel van het industrieel geproduceerde lysine dient als veevoederadditief, maar daarnaast heeft het ook een aantal andere toepassingen. Zo zit het met andere aminozuren in infuusoplossingen en krachtdrankjes voor bodybuilders. In een hoofdpijntablet helpt het om de bloed-hersenbarrière te slechten en het medicijn dus op de juiste plaats in het lichaam te krijgen. Ook zijn er voedingssupplementen verkrijgbaar die beweren een uitbraak van het herpes simplex-virus te verminderen en voorkomen, maar hier is geen onomstotelijk bewijs voor. Tot slot bevatten een aantal cosmeticaproducten lysine.
Prof. John W. Frost van de Michigan State University heeft een methode ontwikkeld om L-lysine om te zetten in
Poly-L-lysine[bewerken | brontekst bewerken]
Het peptide poly-lysine is een polymeer van verschillende lysines. Omdat de aminogroep een pKa van 10,2 heeft, is deze groep bij (neutrale) pH 7, positief geladen (-NH3+).
Met dit positief geladen polymeer kan DNA gebonden worden (bij de constructie van DNA-microarrays): Een glasoppervlak is bij neutrale (en basische) pH deels negatief geladen door SiO−-groepen. Zij kunnen elektrostatisch met polylysine binden, dat op zijn beurt dan weer de negatief geladen fosfaat-groepen van DNA bindt.
Referenties
|
