Reacție Grignard

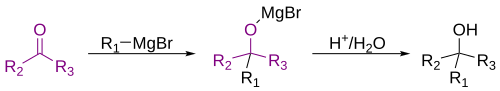
Reacția Grignard este o reacție chimică organometalică în care un reactiv Grignard (adică o halogenură de alchil-, vinil- sau aril-magneziu) se adiționează la o grupă carbonilică dintr-o aldehidă sau o cetonă.[1][2] Reacția este cunoscută pentru faptul că este o metodă importantă de formare de noi legături carbon-carbon.[3][4] Trebuie făcută distincția dintre reacția Grignard și reacția care are loc între un compus halogenat și magneziu metalic, care este reacția de obținere a reactivilor Grignard.[5] Reacția se finalizează cu hidroliza compusului intermediar de adiție, cu obținerea unui alcool primar (plecând de la formaldehidă), a unui alcool secundar (plecând de la aldehide) sau a unui alcool terțiar (plecând de la cetone):
Reacția Grignard și respectivi reactivii Grignard au fost descoperiți de către chimistul francez François Auguste Victor Grignard (Universitatea din Nancy, Franța), care a publicat primele rezultate în anul 1900 și care a primit Premiul Nobel pentru Chimie în anul 1912 pentru lucrările sale.[6]
Mecanism de reacție
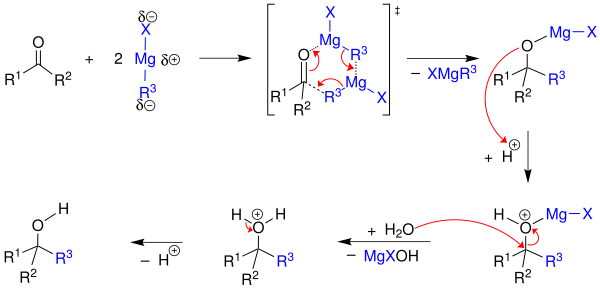
[modificare | modificare sursă]Atomul de carbon legat de magneziu prezintă un caracter nucleofil, producând un atac nucleofil asupra atomului de carbon electrofil prezent în legătura polară a grupei carbonilice. Etapa de adiție a reactivului Grignard la grupa carbonilică are de obicei loc prin intermediul unei stări de tranziție hexaciclice care implică două molecule de reactiv Grignard.[7] După obținerea intermediarului organomagnezian, are loc o reacție de hidroliză în mediu acid, care se finalizează cu obținerea alcoolului corespunzător.
Note
[modificare | modificare sursă]- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (ed. 6), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Chapter 19: Carboxylic Acids. Organic Chemistry 4e Carey. mhhe.com
- ^ Shirley, D. A. (). „The Synthesis of Ketones from Acid Halides and Organometallic Compounds of Magnesium, Zinc, and Cadmium”. Org. React. 8: 28–58.
- ^ Huryn, D. M. (). „Carbanions of Alkali and Alkaline Earth Cations: (ii) Selectivity of Carbonyl Addition Reactions”. În Trost, B. M.; Fleming, I. Comprehensive Organic Synthesis, Volume 1: Additions to C—X
π -Bonds, Part 1. Elsevier Science. pp. 49–75. doi:10.1016/B978-0-08-052349-1.00002-0. ISBN 978-0-08-052349-1. - ^ IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). ISBN: 0-9678550-9-8. doi:10.1351/goldbook.
- ^ Grignard, V. (). „Sur quelques nouvelles combinaisons organométaliques du magnésium et leur application à des synthèses d'alcools et d'hydrocabures”. Compt. Rend. 130: 1322–25.
- ^ Maruyama, K.; Katagiri, T. (). „Mechanism of the Grignard reaction”. J. Phys. Org. Chem. 2 (3): 205–213. doi:10.1002/poc.610020303.