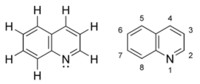
Хинолин
| |

| |
| Називи | |
|---|---|
| IUPAC назив
Quinoline
| |
| Други називи
1-бензазин, 1-азанафтален, бензо[b]пиридин
| |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.001.865 |
| КЕГГ[1] | |
| |
| Својства | |
| C9H7N | |
| Моларна маса | 129,16 g/mol |
| Густина | 1,093 g/ml |
| Тачка топљења | −15 °C |
| Тачка кључања | 108-110°C/11mm Hg |
| Растворан | |
| Базност (пКб) | 4.85[4] |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
Хинолин је хетероциклично ароматично органско једињење. Његова формула је C9H7N. Он је безбојна хигроскопна течност са јаким мирисом. Устајали узорци, ако су изложени светлости, постају жути и касније смеђи. Хинолин је незнатно растворан у хладној води али се брзо раствара у топлој води и већини органских растварача.[5][6]
Хинолин се углавном користи као градивни блок за друге специјализоване хемикалије. Он је прекурзор 8-хидроксихинолина, који је свестрани хелатни агенс и претходник пестицида. Његови 2- и 4-метил деривати су прекурзори цианинских боја. Оксидацијом хинолина настаје хинолинска киселина (пиридин-2,3-дикарбоксилна киселина), која је прекурзор хербицида са тржишним именом Assert.[7]
Изолација и синтеза
[уреди | уреди извор]Фридлиб Фердинанд Рунге је први изоловао хинолин wас из угљене смоле 1834.[8] Смола је још увек главни извор комерцијалног хинолина. Он може да буде синтетисан користећи више метода:
- Комбсова синтеза хинолина користи анилине и
β -дикетоне. - Конрад-Лимпацх синтеза користи анилине и
β -кетоестре. - Доебнер-Милерова реакција користи анилине и
α ,β -незасићена карбонилна једињења. - Фриедландерова синтеза користи 2-аминобензалдехид и ацеталдехид.
- Скраупова синтеза користи феро сулфат, глицерол, анилин, нитробензен, и сумпорну киселину.
Види још
[уреди | уреди извор]- Изохинолин, аналог са атомом азота у позицији 2.
- Пиридин, аналог без кондензованог бензеновог прстена.
- Нафтален, аналог без атома азота.
- Индол, аналог са петочланим азотним прстеном.
- Једноставни ароматични прстени
Референце
[уреди | уреди извор]- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Цлаyден, Јонатхан; Греевес, Ницк; Wаррен, Стуарт; Wотхерс, Петер (2001). Органиц Цхемистрy (I изд.). Оxфорд Университy Пресс. ИСБН 978-0-19-850346-0.
- ^ Катритзкy А.Р.; Позхарскии А.Ф. (2000). Хандбоок оф Хетероцyцлиц Цхемистрy (Сецонд изд.). Ацадемиц Пресс. ИСБН 0080429882.
- ^ Gerd Collin, Hartmut Höke "Quinoline and Isoquinoline" Ullmann's Encyclopedia of Chemical Technology; 2005 Wiley-VCH, Weinheim. . дои:10.1002/14356007.а22_465. Недостаје или је празан параметар
|титле=(помоћ) - ^ „Qуинолине”. Енцyцлопедиа Британница. 1911. Архивирано из оригинала 13. 01. 2008. г. Приступљено 09. 08. 2011.
Литература
[уреди | уреди извор]Спољашње везе
[уреди | уреди извор]- Интернационална карта хемијске безбедности 0071
- Класични методи синтезе хинолина Архивирано на сајту Wayback Machine (26. септембар 2007)
- Novi metodi sinteze hinolinas
