ஐதரசீன்
| |||
| |||
 Hydrazine hydrate
| |||
| பெயர்கள் | |||
|---|---|---|---|
| முறையான ஐயூபிஏசி பெயர்
Hydrazine[2] | |||
| வேறு பெயர்கள் | |||
| இனங்காட்டிகள் | |||
| 302-01-2 | |||
| 3DMet | B00770 | ||
Beilstein Reference
|
878137 | ||
| ChEBI | CHEBI:15571 | ||
| ChEMBL | ChEMBL1237174 | ||
| ChemSpider | 8960 | ||
| EC number | 206-114-9 | ||
Gmelin Reference
|
190 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | C05361 | ||
| ம.பா.த | Hydrazine | ||
| பப்கெம் | 9321 | ||
| வே.ந.வி.ப எண் | MU7175000 | ||
| |||
| UNII | 27RFH0GB4R | ||
| UN number | 2029 | ||
| பண்புகள் | |||
| N 2H 4 | |||
| வாய்ப்பாட்டு எடை | 32.0452 g mol−1 | ||
| தோற்றம் | Colourless liquid | ||
| அடர்த்தி | 1.021 g cm−3 | ||
| உருகுநிலை | 2 °C; 35 °F; 275 K | ||
| கொதிநிலை | 114 °C; 237 °F; 387 K | ||
| மட. P | 0.67 | ||
| ஆவியமுக்கம் | 1 kP (at 30.7 °C) | ||
| காடித்தன்மை எண் (pKa) | 8.10[3] | ||
| காரத்தன்மை எண் (pKb) | 5.90 | ||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.46044 (at 22 °C) | ||
| பிசுக்குமை | 0.876 cP | ||
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 1.85 D[4] | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation |
50.63 kJ mol−1 | ||
| நியம மோலார் எந்திரோப்பி S |
121.52 J K−1 mol−1 | ||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 0281 | ||
| GHS pictograms |     
| ||
| GHS signal word | DANGER | ||
| H226, H301, H311, H314, H317, H331, H350, H410 | |||
| P201, P261, P273, P280, P301+310, P305+351+338 | |||
| ஈயூ வகைப்பாடு | |||
| R-சொற்றொடர்கள் | R45, R10, R23/24/25, R34, R43, R50/53 | ||
| S-சொற்றொடர்கள் | S53, S45, S60, S61 | ||
| தீப்பற்றும் வெப்பநிலை | 52 °C (126 °F; 325 K) | ||
| வெடிபொருள் வரம்புகள் | 1.8–99.99% | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose)
|
59–60 mg/kg (oral in rats, mice)[6] | ||
| தொடர்புடைய சேர்மங்கள் | |||
| தொடர்புடைய சேர்மங்கள் | நவச்சாரியம் | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
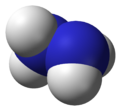
N2H4 எனும் மூலக்கூற்று வாய்ப்பாடுடைய அசேதனச் சேர்மமே ஐதரசீன் ('Hydrazine') ஆகும். இது நிறமற்ற, தீப்பற்றக்கூடிய, அமோனியா போன்ற வாடையுடைய திரவமாகும். இது மிகவும் நச்சுத்தன்மையானது. நிலைப்புத்தன்மை அற்றது. இது பல்வேறு பயன்களைக் கொண்டிருப்பதால் 2002ஆம் ஆண்டளவில் 260000 தொன் ஐதரசீன் உற்பத்தி செய்யப்பட்டது. பல்பகுதிய நுரைத் தயாரிப்பிலும், பல்பகுதியத்தைத் தயாரிக்கப் பயன்படும் வினைவேகமாற்றிகளை உருவக்கவும், மருந்து உற்பத்தியிலும், ரொக்கட்டுகளில் எரிபொருளாகவும் ஹைட்ரஸைன் பயன்படுகின்றது. மின்னுற்பத்தி நிலையங்களில் நீரில் கரைந்துள்ள ஒக்சிசன் அரிப்பை ஏற்படுத்துமென்பதால் ஒக்சிசனை அகற்ற இது பயன்படுகின்றது.
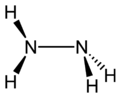
மூலக்கூற்று அமைப்பும் இயல்புகளும்
[தொகு]ஐதரசீனின் அடர்த்தி 1.021 g cm−3 ஆகும். எனினும் இதன் நீரேற்றப்பட்ட வடிவம் இதனை விட சிறிது அடர்த்தி கூடியது (1.032 g cm−3). ஐதரசன் அணு ஒன்றின் வெளியேற்றத்துடன் இரு அமோனிய மூலக்கூறுகள் இணைக்கப்பட்டமையை ஐதரசீனின் மூலக்கூற்றுக் கட்டமைப்பு காட்டுகின்றது. இரண்டு நைதரசன் அணுக்களுக்கு இடையே 1.45 Å (145 pm) இடைவேளி உள்ளது.
நீரில் கரைக்கப்படும் போது அமோனியா போன்ற காரத்தன்மையை ஐதரசீன் காட்டுகின்றது.
- N2H4 + H2O → [N2H5]+ + OH−
ஐதரசீன் தீப்பற்றக்கூடிய திரவமாகும். எரியும் ஒவ்வொரு கிலோகிராம் ஐதரசீனும் 194.1 x 105 J வெப்பத்தை வழங்கும் திறனுடையது.
உற்பத்தி
[தொகு]குளோரமைனையும் (அமோனியம் குளோரைட்டு) அமோனியாவையும் தாக்கத்துக்கு உட்படுத்துவதால் ஐதரசீனை உற்பத்தி செய்ய முடியும்.
- NH2Cl + NH3 → H2N-NH2 + HCl
யூரியாவோடு அல்லது அமோனியாவோடு சோடியம் ஹைபோகுளோரைற்றைத் தாக்கத்துக்கு உட்படுத்துவதாலும் ஐதரசீனை உற்பத்தி செய்ய முடியும்.
- (H2N)2C=O + NaOCl + 2 NaOH → N2H4 + H2O + NaCl + Na2CO3
- 2NH3 + NaClO → N2H4 + NaCl + H2O
அமோனியாவையும் ஐத்ரசன் பர ஒக்சைட்டையும் கொண்டும் இதனை உற்பத்தி செய்யலாம்.
- 2NH3 + H2O2 → H2N-NH2 + 2H2O
ரொக்கெட்டுகளில் ஐதரசீனின் பயன்பாடு
[தொகு]
இரண்டாம் உலகப் போரிலேயே ஐதரசீன் முதன் முதலாக ரொக்கெட் எரிபொருளாகப் பயன்பட்டது. முதல் ரொக்கெட் பூட்டப்பட்ட விமானமான 'Messerschmitt Me 163B' இல் இது B-Stoff (நீரேற்றப்பட்ட ஐதரசீன்) என்ற பெயருடன் எரிபொருளாகப் பயன்படுத்தப்பட்டது.
எரிபொருளாக மட்டுமன்றி தள்ளுகைப் பொருளாகவும் ஐதரசீன் பயன்படுகின்றது. இது இவ்வாறு தள்ளுகை ஆற்றலை வெளிப்படுத்த ஆக்சிசன் தேவைப்படாமையால் விண்வெளி ஓடங்களில் சிறிய தள்ளுகை ரொக்கெட்டுகளாகப் பயன்படுகின்றது. வைகிங், ஃபீனிக்ஸ் மற்றும் கியூரியோசிட்டி ஓடங்களில் இவ்வாறான சிறிய ரொக்கெட்டுகள் பயன்படுத்தப்பட்டன.
எல்லா ஐதரசீனைப் பயன்படுத்தும் தனித்தள்ளுகை இயந்திரங்களிலும் ஊக்க வினைவேகமாற்றிகள் தாக்கத்தைத் தூண்டவும் தொடரவும் பயன்படுத்தப்படுகின்றன. இரீடியம் உலோகத்தோடிணைந்த அலுமினா அல்லது நனோ கார்பன் நார்கள் அல்லது மொசிப்டினம் நைட்ரைட்டோடிணைந்த அலுமினா ஊக்கிகளாகப் பயன்படுகின்றன. இவை ஐதரசீனை ஐதரசன் மற்றும் நைதரசனாகப் பிரிகையுற உதவுகின்றன.
- 3 N2H4 → 4 NH3 + N2
- N2H4 → N2 + 2 H2
- 4 NH3 + N2H4 → 3 N2 + 8 H2
முதலாவது மற்றும் இரண்டாவது தாக்கங்கள் புறவெப்பத்தாக்கங்களாகும். வெப்பநிலையை சடுதியாக 800 °Cக்கு உயர்த்தும் ஆற்றல் இத்தாக்கங்களுக்கு உண்டு. மூன்றாவது தாக்கம் அகவெப்பத் தாக்கமாகும். இது வெப்பநிலையைக் குறைத்தாலும், இத்தாக்கம் அதிகளவு வாயுவை வெளியேற்றும் ஆற்றலுள்ளது. இவ்வனைத்துத் தாக்கங்களும் ஊக்கிகளில் தங்கியுள்ளதால் இத்தாக்கங்களை விரும்பியவாறு கட்டுப்படுத்தி ரொக்கெட்டுகளை இயக்க முடியும்.
மேற்கோள்கள்
[தொகு]- ↑ "NIOSH Guide - Hydrazine". Centers for Disease Control. பார்க்கப்பட்ட நாள் 16 August 2012.
- ↑ 2.0 2.1 "hydrazine - PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information.
- ↑ Hall, H.K., J. Am. Chem. Soc., 1957, 79, 5441.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth–Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0080379419.
- ↑ "Hydrazine safety data sheet". Archived from the original on 2014-01-01. பார்க்கப்பட்ட நாள் 2014-01-02.
{{cite web}}: Unknown parameter|=ignored (help) - ↑ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. p. 361. பன்னாட்டுத் தரப்புத்தக எண் 1-903996-65-1.
{{cite book}}: CS1 maint: multiple names: authors list (link)