Вільна енергія Гельмгольца
| Частина серії статей на тему: |
| Термодинаміка |
|---|
 Теплова машина Карно |
|
|
Ві́льна ене́ргія Гельмго́льца — термодинамічний потенціал, який визначає рівноважні термодинамічні характеристики системи в залежності від об'єму та температури.
Можна показати, що рівноважний стан системи багатьох часток при визначеному об'ємі та сталій температурі визначається мінімумом вільної енергії Гельмгольца[1].
Назва вільна енергія народилася в ті часи, коли створювалася теорія теплових машин. Дослідження показали, що нагрітий газ при охолодженні, що не роби, не віддає всю свою енергію. Ту частку енергії газу, яку можна було відібрати й перетворити в корисну роботу, стали називати вільною енергією.
Як і будь-яка інша енергія, вільна енергія в класичній фізиці визначається з точністю до довільної сталої. Проте, виходячи із квантово-механічних уявлень, можна встановити природну точку відліку. При абсолютному нулі температури, вільна енергія збігається з енергією основного стану квантово-механічної системи.
Вільна енергія F визначається як
- ,
де T — температура, S — ентропія, а E — внутрішня енергія системи.
Зміна вільної енергії дорівнює роботі, виконаній над тілом при ізотермічному процесі
Диференціал вільної енергії дорівнює
- .
У випадку системи із змінним числом частинок, диференціал вільної енергії отримує додатковий член
- ,
де
Термодинамічні характеристики системи визначаються через похідні від вільної енергії. Наприклад, якщо потрібно визначити тиск у газі чи в рідині при певній температурі, можна скористатися формулою:
- .
Аналогічно, якщо об'єм газу фіксований, то його ентропія визначається формулою
- .
Якщо виділити якийсь об'єм у газі при умовах вільного обміну атомами із сусідніми об'ємами, то при сталій температурі його хімічний потенціал визначається як похідна від вільної енергії за кількістю частинок
У статистичній фізиці найчастіше розглядається канонічний ансамбль Гібса, тобто набір однакових за складом систем із визначеним об'ємом і при заданій температурі — саме в тих умовах, для яких використовується вільна енергія.
Ймовірність pn реалізації стану n із енергією En в такому ансамблі визначається формулою
- .
Вільна енергія F знаходиться із умови нормування ймовірності.
- ,
де статистична сума Z дорівнює
Для класичного ідеального одноатомного газу вільна енергія дорівнює
Заряд
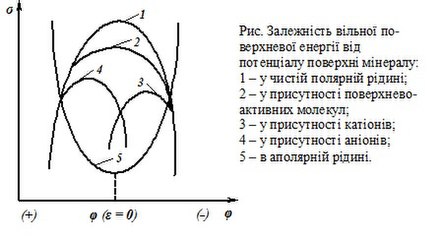
За значенням величини вільної поверхневої енергії та залежно від концентрації йонів і молекул поверхнево-активних речовин у розчині можна розрахувати (за рівнянням Гіббса) їхню абсорбцію на досліджуваній поверхні. За залежністю вільної поверхневої енергії від потенціалу можна визначити поверхневу щільність заряду, а за залежністю адсорбції від потенціалу — орієнтацію молекул в адсорбційному шарі й характер їхньої взаємодії між собою.
Дипольні молекули води можуть закріплюватися (адсорбуватися) на поверхні мінералу в результаті електростатичного притягання їх зарядженими йонами поверхні, міжмолекулярної взаємодії з поверхнею, утворення водневих і координаційних зв'язків з йонами або молекулами поверхневого шару. Структура гідратних шарів на поверхні мінералу при цьому визначатиметься кількісним співвідношенням різнойменних зарядів, на яких можуть закріплюватися та взаємно розташовуватися молекули води.
- ↑ О. С. Гамеева «Физическая и коллоидная химия», — М.:"Высшая школа", 1969, с. 106
- Базаров И. П. Термодинамика. — М. : Высшая школа, 1991. — 376 с.
- Глосарій термінів з хімії / укладачі: Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Донецьк : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.
- Квасников И. А. Теория равновесных систем: Термодинамика // Термодинамика и статистическая физика. — М. : URSS, 2012. — Т. 1. — 328 с.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1 // Теоретическая физика. — М. : Физматлит, 2005. — Т. 5. — 616 с.
- Сивухин Д. В. Термодинамика и молекулярная физика // Общий курс физики. — М. : Физматлит, 2002. — Т. 2. — 576 с.
| Це незавершена стаття з фізики. Ви можете допомогти проєкту, виправивши або дописавши її. |
























