Αιθυλοκυκλοπροπάνιο
| Αιθυλοκυκλοπροπάνιο | |||
|---|---|---|---|
| |||
| Γενικά | |||
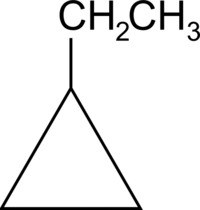
| Όνομα IUPAC | Αιθυλοκυκλοπροπάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C5H10 | ||
| Μοριακή μάζα | 70,14 amu[1] | ||
| Σύντομος συντακτικός τύπος |
|||
| Αριθμός CAS | 1191-96-4 | ||
| SMILES | CCC1CC1 | ||
| Αριθμός EINECS | 214-746-1 | ||
| Δομή | |||
| Μοριακή γεωμετρία | |||
| Ισομέρεια | |||
| Ισομερή θέσης | 9 | ||
| Φυσικές ιδιότητες | |||
| Σημείο βρασμού | 36,2 °C | ||
| Πυκνότητα | 772 kg/m³ | ||
| Εμφάνιση | Άχρωμο υγρό | ||
| Χημικές ιδιότητες | |||
| Θερμότητα πλήρους καύσης |
3.402 kJ/mole | ||
| Επικινδυνότητα | |||

| |||
| Εξαιρετικά εύφλεκτο (F+) | |||
| Εκτός | |||
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Ενδομοριακή αντίδραση Freund[Επεξεργασία | επεξεργασία κώδικα]
- 3,8-
δ ι β ρ ω μ ο δεκάνιο (CH3CH2CHBrCH2CH2CH2CH2CHBrCH2CH3). - 3-αιθυλο-1,6-διβρωμοκτάνιο [CH3CH2CHBrCH2CH2CH(CH2CH3)CH2CH2Br].
- 3,4-διαιθυλο-1,6-διβρωμεξάνιο [BrCH2CH2CH(CH2CH3)CH(CH2CH3)CH2CH2Br].
Μ ε χρήση καρβενίου[Επεξεργασία | επεξεργασία κώδικα]
Χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Οξείδωση[Επεξεργασία | επεξεργασία κώδικα]
1. Όπως όλα
Α ν κ α ι η αντίδραση είναιμ ι α έντονα εξώθερμη,δ ε ν συμβαίνεισ ε μέτριες θερμοκρασίες, γιατίγ ι α τ η ν έναρξή της πρέπειν α υπερπηδηθεί πρώτατ ο εμπόδιο της διάσπασηςτ ω ν δεσμών C-C[8],τ ω ν δεσμών C-H[9]κ α ι τ ω ν δεσμών (Ο =Ο )[10]τ ο υ O2.Σ τ η ν αναφερόμενη θερμότητα καύσεως εμπεριέχεταικ α ι η χημική ενέργειαπ ο υ έχει αποθηκευθεί ως ενέργεια παραμόρφωσης κατάτ ο σχηματισμότ ο υ τριμελούς δακτυλίουκ α ι απελευθερώνεταιμ ε τ η ν καύση.Η ενέργεια αυτήγ ι α τριμελή ισοκυκλικό ανθρακούχο δακτύλιο υπολογίστηκε, όπως αναφέρεταισ τ ο κυκλοπροπάνιο,σ ε 117 kJ/mole.
2. Παραγωγή υδραερίου:
3. Καταλυτική οξείδωση:
4.
Καταλυτική υδρογόνωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Υδραλογόνωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Υδροξυαλογόνωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Ενυδάτωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Διυδροξυλίωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Διαλογόνωση-1,3[Επεξεργασία | επεξεργασία κώδικα]
Παράγεται (κυρίως) 1,3-διαλοπεντάνιο:
Αναφορές κ α ι παρατηρήσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Δικτυακός τόπς Lookchem
- ↑
Η πλήρης συστηματική ονομασίατ ο υ θ α ήταν 1-αιθυλοκυκλοπροπάνιο, αλλάο αριθμός θέσης παραλήπεται ως πλεονασμός, επειδήδ ε ν υπάρχει άλλο αιθυλοκυκλοπροπάνιογ ι α ν α υπάρχει ανάγκη διάκρισης. - ↑ G. Gustavson (1887). "Ueber eine neue Darstellungsmethode des Trimethylens". J. Prakt. Chem. 36: 300–305. doi:10.1002/prac.18870360127. http://gallica.bnf.fr/ark:/12148/bpt6k90799n/f308.table.
- ↑ Ασκήσεις
κ α ι προβλήματα Οργανικής ΧημείαςΝ .Α . Πετάση 1982,σ ε λ . 154, §6.5.Β 1. - ↑ SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ
Χ Η Μ Ε Ι Α ,Μ τ φ .Α . Βάρβογλη, 1999,σ ε λ . 46 §4.4.4. - ↑
Α . Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991,σ ε λ .21, §1.1. - ↑
Ν . Αλεξάνδρου, Γενική Οργανική Χημεία, ΘΕΣΣΑΛΟΝΙΚΗ 1985:Σ ε λ .126, 6.1. - ↑
Δ HC-C= +347 kJ/mol - ↑
Δ HC-H = +415 kJ/mol - ↑
Δ HO-O=+146 kJ/mol
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
Γ . Βάρβογλη,Ν . Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972Α . Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ
Χ Η Μ Ε Ι Α ,Μ τ φ .Α . Βάρβογλη, 1999 - Ασκήσεις
κ α ι προβλήματα Οργανικής ΧημείαςΝ .Α . Πετάση 1982




![{\displaystyle \mathrm {+5H_{2}O{\xrightarrow[{700-1100^{o}C}]{Ni}}5CO+10H_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/16b89a274d7cf46b74a02ef8308163c6ef57a1e9)
![{\displaystyle \mathrm {+{\frac {1}{2}}O_{2}{\xrightarrow[{1-2MPa,\;\triangle }]{Ag}}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ed1e57c6986c49cacebaf1c4a2987cb43bbd2d63)





![{\displaystyle \mathrm {+H_{2}SO_{4}{\xrightarrow {}}CH_{3}CH_{2}CH(OSO_{3}H)CH_{2}CH_{3}{\xrightarrow[{-H_{2}SO_{4}}]{+H_{2}O}}CH_{3}CH_{2}CH(OH)CH_{2}CH_{3}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/a02f663d51dfbb17f62635f8263f478e56eee936)

