Acetilene
| Acetilene | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | |
| etino | |
| Nomi alternativi | |
| acetilene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H2 |
| Massa molecolare (u) | 26,04[1] |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 200-816-9 |
| PubChem | 6326 |
| DrugBank | DBDB15906 |
| SMILES | C#C |
| Proprietà chimico-fisiche | |
| Densità (kg·m−3, in c.s.) | 1,17085 |
| Solubilità in acqua | 0,144 g/l a c.n. |
| Temperatura di fusione | −84 °C (189 K) |
| Temperatura di ebollizione | −83,6 °C (189,6 K) |
| Tensione di vapore (Pa) a 189 K | 1,0252 * 106[2] |
| Proprietà termochimiche | |
| 226,73[1] | |
| 209,20[1] | |
| S0m(J·K−1mol−1) | 200,94[1] |
| C0p,m(J·K−1mol−1) | 43,93[1] |
| −1300[1] | |
| Indicazioni di sicurezza | |
| Limiti di esplosione | 2,5 - 81% vol. |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 220 - 230 - 280 |
| Consigli P | 202 - 210 - 317 - 381 - 403 [3] |
L'acetilene (nome IUPAC: etino) è il più semplice degli alchini, idrocarburi con un triplo legame carbonio-carbonio. Fu scoperto nel 1836 dal chimico britannico Edmund Davy.
Descrizione
[modifica | modifica wikitesto]A temperatura e pressione standard è un gas incolore ed estremamente infiammabile. Ha una temperatura di autoaccensione di circa 305 °C. È un gas estremamente pericoloso perché può esplodere anche con inneschi minimi e per questo è normalmente diluito nell'acetone.
La maggior parte dell'acetilene (~80%) è utilizzata come intermedio di sintesi di altri composti; circa il 20% della produzione annua di acetilene è usato per saldatura e taglio dei metalli (ossiacetilene), dato che la sua combustione con l'ossigeno produce una fiamma la cui temperatura arriva a circa 3300 °C. L'acetilene è anche usato nella lavorazione dell'acciaio.
L'acetilene veniva in passato utilizzato nei dispositivi di illuminazione utilizzati dagli speleologi e dai minatori dove veniva prodotto in situ a partire dal carburo di calcio facendolo reagire con l'acqua.
Viene utilizzato anche in saldatura e in brasatura, sia in bombole sia prodotto in loco da gasogeni, anche se la saldatura elettrica da circa 50 anni sta progressivamente soppiantando l'uso della saldatura a cannello.
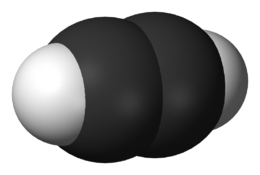
La molecola dell'acetilene ha geometria lineare, ovvero tutti e quattro gli atomi sono allineati lungo l'asse del triplo legame che unisce i due atomi di carbonio che hanno ibridazione sp. Dal punto di vista chimico, la reattività dell'acetilene è simile a quella dell'etene, ovvero si manifesta attraverso reazioni di addizione al triplo legame.
Una particolarità dell'acetilene (e in genere degli alchini terminali, ossia quelli che hanno struttura tipo R-C≡C-H) è l'acidità degli atomi di idrogeno. Per trattamento con basi forti, l'acetilene perde uno o entrambi gli idrogeni formando l'anione HC≡C- (acetiluro) o il dianione C22- (carburo).
Data l'estrema facilità con cui brucia ed esplode, nonché l'elevata energia liberata dalle sue esplosioni, l'acetilene va manipolato con estrema cautela.
Sintesi
[modifica | modifica wikitesto]L'acetilene è un prodotto molto costoso; si tende a sostituirlo con etilene che costa un terzo ed è molto meno pericoloso (infatti l'acetilene ha limiti di esplosività in aria di 2.3-80 e di 2.3-93 in ossigeno).
Il primo metodo di preparazione risale al 1862:
CaO + 3C → CaC2 + COΔ H°=108 kcal/mol
in forno elettrico si carica una miscela di coke (40 %) e di calce (60 %), si scalda a T = 2000 °C. Il consumo di energia elettrica è di 4-4.3 kWh per kg di CaC2. Successivamente si idrolizza il carburo di calcio:
CaC2 + 2H2O → Ca(OH)2 + CH≡CHΔ H°=–32 kcal/mole
Con l'aumento della domanda di acetilene questo processo va in crisi perché non si possono costruire forni di alta capacità. Si è sviluppato quindi un processo di pirolisi di idrocarburi:
2CH4 → CH≡CH + 3H2Δ H°=96 kcal/mole, conΔ G°<0 a T=1450 °C
C4H10 → 2CH≡CH + 3H2Δ H°=72 kcal/mole, conΔ G°<0 a T=1120 °C
A T basse l'acetilene è ancora più instabile, ma la cinetica di decomposizione è più lenta:
2C + H2 → CH≡CHΔ H°=54 kcal/mole, conΔ G°> 0 fino a T=4000 °C
A temperatura ambiente viene assorbito in acetone per essere stabilizzato.
Il problema di questa sintesi è quello di fornire calore ad alte T per tempi bassissimi; le soluzioni trovate sono due:
- calore fornito dall'esterno (arco elettrico o parete riscaldata); i gas di reazione non vengono inquinati o diluiti dai prodotti di combustione;
- calore fornito dall'interno (come nei gasogeni) per combustione parziale dei reagenti, o per miscelazione dei reagenti con i gas di combustione.
Reattore ad arco elettrico rotante
[modifica | modifica wikitesto]È un reattore tubolare raffreddato da una camicia a circolazione di acqua; un'elettrocalamita fa ruotare l'arco che scocca fra l'elettrodo centrale e la parete del reattore, in modo ottenere una d.d.p. uniforme e quindi una T uniforme. Ciò serve a diminuire le quantità di nerofumo e quindi evitare l'abbassamento di resa in acetilene. Ci sono due alimentazioni: a monte dell'arco si alimentano idrocarburi leggeri C1-C3 a T = 2500 °C; a valle si alimentano C4-C11 a T = 1800 °C. Il raffreddamento è ottenuto sia per evaporazione del fluido di quenching sia per assorbimento di calore da parte della reazione paraffina → acetilene. Il tempo di contatto è di circa 1/100 di secondo.
Processo Wulf
[modifica | modifica wikitesto]Prevede due forni che lavorano alternativamente: il primo in fase di riscaldamento, dove si ha la combustione in aria; nel secondo si ha la fase di pirolisi a 1200 °C
Bruciatore Fauser-Montedison
[modifica | modifica wikitesto]In questo caso si hanno due diversi quenching: un primo con benzina, dove avvengono deidrogenazioni con produzione di acetilene ed etilene; in seguito si ha un secondo quenching con acqua.
Processo Hoechst-Uhde
[modifica | modifica wikitesto]Come combustibile si usa il gas che proviene dalla coda dell'impianto (H2 + CO + idrocarburi). Il reagente idrocarburico è successivamente iniettato nella corrente gassosa costituita dai gas combusti caldi, a T = 1500 °C e tempo di contatto pari a 1/1000 di secondo.
Apparecchio Forlanini
[modifica | modifica wikitesto]Forlanini produsse, per l'industria Gazogene e Fabbrica del gas di Forlì, un proprio modello di apparecchio per generare acetilene. I relativi appunti e lo schizzo sono conservati nel Fondo Enrico Forlanini del Museo nazionale della scienza e della tecnologia Leonardo da Vinci di Milano[4].
Note
[modifica | modifica wikitesto]Bibliografia
[modifica | modifica wikitesto]- (EN) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley, Industrial organic chemistry, 4ª ed., Wiley-VCH, 2003, pp. 91-106, ISBN 3-527-30578-5.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «acetilene»
Wikizionario contiene il lemma di dizionario «acetilene» Wikimedia Commons contiene immagini o altri file sull'acetilene
Wikimedia Commons contiene immagini o altri file sull'acetilene
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) acetylene, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 21721 · LCCN (EN) sh85000470 · GND (DE) 4000345-0 · BNF (FR) cb11982014p (data) · J9U (EN, HE) 987007293982305171 · NDL (EN, JA) 00560381 |
|---|