Indene
| Indene | |
|---|---|
 | |
 | |
| Nome IUPAC | |
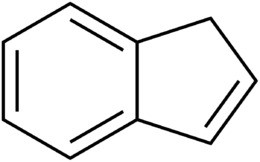
| 1H-indene | |
| Nomi alternativi | |
| Biciclo[4.3.0]nona-1,3,5,7-tetraene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C9H8 |
| Massa molecolare (u) | 116.16 g/mol |
| Numero CAS | |
| Numero EINECS | 202-393-6 |
| PubChem | 7219 |
| SMILES | C1C=CC2=CC=CC=C21 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0.997 g/mL |
| Costante di dissociazione acida a 298 K | ~ 1020.1 (in DMSO) |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | -1.8 °C |
| Temperatura di ebollizione | 181.6 °C |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi H | H226-H304 |
| Consigli P | P301+P310-P331 |
L'indene è un idrocarburo policiclico infiammabile con formula chimica C9H8. Esso è composto da un anello benzenico fuso con l'anello del ciclopentene. È un liquido aromatico incolore, anche se i campioni spesso sono di colore giallo pallido, fenomeno dovuto alla parziale ossidazione della molecola. Il principale uso industriale dell'indene è nella produzione di resine termoplastiche indene/cumarone.
Presenza in natura
[modifica | modifica wikitesto]L'indene si trova in natura in frazioni di catrame di carbone bollente intorno a 175-185 °C. Esso può essere ottenuto riscaldando questa frazione con sodio per precipitare il solido "sodio-indene." Questo passaggio sfrutta l'acidità debole dell'indene dimostrata dalla sua deprotonazione da parte del sodio metallico per dare il derivato indenilico. Il sodio-indene viene riconvertito in indene per distillazione a vapore.[2]
Reattività
[modifica | modifica wikitesto]L'indene polimerizza facilmente. La sua ossidazione con acido dicromato porta all'acido omoftalico (acido o-carbossilfenilacetico). Condensa con ossalato di etile in presenza di etossido di sodio per formare l'estere indene-ossalico, e con aldeidi o chetoni in presenza di alcali per formare benzofulveni. Questi ultimi sono molto colorati. Un indene è anche un precursore dell'anione indenile, un ligando in chimica organometallica con qualche notorietà dovuta all'"effetto indenilico".
Note
[modifica | modifica wikitesto]- ^ Bordwell FG,, Equilibrium acidities in dimethyl sulfoxide solution,, in Accounts of Chemical Research, vol. 21, 1988, pp. 456-463, DOI:10.1021/ar00156a004.
- ^ Gerd Collin, Rolf Mildenberg, Mechthild Zander, Hartmut Höke, William McKillip, Werner Freitag, Wolfgang Imöhl “Resins, Synthetic” Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2000.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su indene
Wikimedia Commons contiene immagini o altri file su indene
Collegamenti esterni
[modifica | modifica wikitesto]- W. v. Miller, Rohde, "Zur Synthese von Indenderivaten", in Berichte der deutschen chemischen gesellschaft, vol. 23, 1890, p. 1881-1886, DOI:10.1002/cber.18900230227.
- W. v. Miller, Rohde, Zur Synthese von Indenderivaten, in Berichte der deutschen chemischen Gesellschaft, vol. 23, 1890, pp. 1887–1902, DOI:10.1002/cber.18900230228.
- I. L. Finar, Organic Chemistry, Longman Scientific & Technical, 1985, ISBN 0-582-44257-5.
| Controllo di autorità | GND (DE) 4161475-6 |
|---|