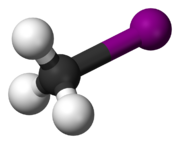
Jódmetán
| Jódmetán | |||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||
| Sumárny vzorec | CH3I | ||||||||||||||||||||||||||||||||||
| Synonymá | Metyljodid Monojódmetán | ||||||||||||||||||||||||||||||||||
| Vzhľad | Bezfarebná až svetložltá kvapalina s charakteristickou éterovou vôňou. Hnedne pri vystavení svetlu a vlhkosti | ||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 142,0 u | ||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 141,93899 g/mol | ||||||||||||||||||||||||||||||||||
| Teplota topenia | -66,5 °C | ||||||||||||||||||||||||||||||||||
| Teplota varu | 41-43 °C | ||||||||||||||||||||||||||||||||||
| Kritická teplota | 254,8 °C | ||||||||||||||||||||||||||||||||||
| Kritický tlak | 7,68 MPa | ||||||||||||||||||||||||||||||||||
| Hustota | 2,27 g/cm3 | ||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 1,4 g/100 ml (20 °C) | ||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | −14,1 až −13,1 kJ/mol | ||||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 82.75 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||
| Číslo CAS | 74-88-4 | ||||||||||||||||||||||||||||||||||
| Číslo UN | 2644 | ||||||||||||||||||||||||||||||||||
| EINECS číslo | 200-819-5 | ||||||||||||||||||||||||||||||||||
| Číslo RTECS | PA9450000 | ||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||
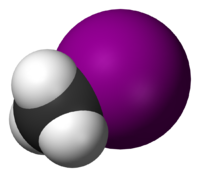
Jódmetán (CH3I), tiež metyljodid alebo monojódmetán, skratka MeI, je organická zlúčenina patriaca medzi halogénderiváty uhľovodíkov, jeho molekula vychádza z molekuly metánu, kde je jeden atóm vodíka nahradený atómom jódu. Za bežných podmienok má jódmetán podobu hustej bezfarebnej prchavej kvapaliny miešateľnej s organickými rozpúšťadlami. V malom množstve vzniká prirodzene v rastlinách ryže.[1] Využíva sa v organickej syntéze k metylácii. Kontroverzným rozhodnutím EPA v roku 2007 bol tiež schválený ako pesticíd.[2]
Vlastnosti
[upraviť | upraviť zdroj]Jódmetán je bezfarebná kvapalina, relatívne prchavá (teplota varu 41-43 °C). Rozpúšťa sa v mnohých organických rozpúšťadlách. Podobne ako mnoho iných organojodidových zlúčenín je potrebné ho uchovávať v tmavých fľašiach, pretože sa na svetle rozkladá; uvoľňovaný jód farbí kvapalinu do hneda. Komerčné produkty môžu byť stabilizované medeným alebo strieborným drôtom.
Referencie
[upraviť | upraviť zdroj]- ↑ K. R. Redeker; N.-Y. Wang; J. C. Low, et al. Emissions of Methyl Halides and Methane from Rice Paddies. Science, 2000, roč. 290, čís. 5493, s. 966–969. DOI: 10.1126/science.290.5493.966. PMID 11062125. (po anglicky)
- ↑ ZITTO, Kelly. Methyl iodide gains state OK for use on crops. San Francisco Chronicle, 2. December 2010. Dostupné online [cit. 2015-05-03]. (po anglicky)
Literatúra
[upraviť | upraviť zdroj]- Sulikowski, G. A .; Sulikowski, M. M. (1999). in Coates, R.M .; Denmark, SE (Eds.) Handbook of Reagents for Organic Synthesis, Volume 1: Reagents, Auxiliaries and Catalysts for CC Bond Formation New York: Wiley, pp.423-26.
- H. M. Bolt; B. Gansewendt. Mechanisms of carcinogenicity of methyl halides.. Critical Reviews in Toxicology, 1993, roč. 23, čís. 3, s. 237–253. DOI: 10.3109/10408449309105011. PMID 8260067. (po anglicky)
Externé odkazy
[upraviť | upraviť zdroj]- IARC Summaries & amp; Evaluations: Vol. 15 (1977), Vol. 41 (1986), Vol. 71 (1999)
- Metabolism of iodomethane in the rat
- Iodomethane NMR spectra Archivované 2007-02-10 na Wayback Machine
- JONES, Nicola. Strawberry pesticide leaves sour taste: Methyl iodide use by Californian farmers up for review.. Nature News, September 24, 2009. Dostupné online [cit. 2009-09-25].
Zdroj
[upraviť | upraviť zdroj]Tento článok je čiastočný alebo úplný preklad článku Jodmethan na českej Wikipédii.




