氯胺
| 氯胺 | |
|---|---|
| |

| |
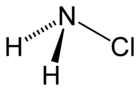
| Chloramine | |
| 别名 | 氯代氨 |
| 识别 | |
| CAS |
10599-90-3 |
| PubChem | 25423 |
| ChemSpider | 23735 |
| SMILES |
|
| InChI |
|
| InChIKey | QDHHCQZDFGDHMP-UHFFFAOYAS |
| NH2Cl | |
| 51.48 g·mol⁻¹ | |
| 熔点 | −66 °C |
氯胺,
一氯代氨的化学式是NH2Cl,为不稳定
水 处理
[编辑]氯胺
饮用水 消毒
[编辑]游泳 池 消毒
[编辑]安全 性
[编辑]制 备
[编辑]氯胺
气态氯胺
- 2 NH3(g) + Cl2(g) ⇌ NH2Cl(g) + NH4Cl(s)
- 2 NH2F + CaCl2 → 2 NH2Cl + CaF2
參考 文獻
[编辑]- ^ Lawrence, Stephen A. Amines: Synthesis, Properties and Applications. Cambridge University Press. 2004: 172 [2018-05-16]. ISBN 9780521782845. (
原始 内容 存 档于2018-04-06) (英 语). - ^
存 档副本 (PDF). [2014-06-02]. (原始 内容 存 档 (PDF)于2008-11-02). - ^ Stuart W. Krasner. The formation and control of emerging disinfection by-products of health concern 367 (1904). Philosophical Transactions of the Royal Society: 4077–95. 2009-10-13. doi:10.1098/rsta.2009.0108. (
原始 内容 存 档于2015-10-27). - ^ Marie Lynn Miranda; et al. Changes in Blood Lead Levels Associated with Use of Chloramines in Water Treatment Systems. Environmental Health Perspectives. February 2007, 115 (2): 221–5. PMC 1817676
 . PMID 17384768. doi:10.1289/ehp.9432.
. PMID 17384768. doi:10.1289/ehp.9432.
- ^ Donegan, Fran J.; David Short. Pools and Spas. Upper Saddle River, New Jersey: Creative Homeowner. 2011. ISBN 978-1-58011-533-9.
- ^ Controlling Chloramines in Indoor Swimming Pools. NSW Government. [2013-02-15]. (
原始 内容 存 档于2011-04-03). - ^ Hale, Chris. Pool Service Information. 2016-04-20 [2016-04-22]. (
原始 内容 存 档于2016-04-05). - ^ Bougault, Valérie; et al. The Respiratory Health of Swimmers. Sports Medicine. 2009, 39 (4): 295–312. doi:10.2165/00007256-200939040-00003. (
原始 内容 存 档于2011-06-05). - ^ The determinants of prevalence of health complaints among young competitive swimmers. International Archives of Occupational and Environmental Health. 2006-10-01, 80 (1): 32–39. doi:10.1007/s00420-006-0100-0.[
永久 失效 連結 ] - ^ Krasner, Stuart W.; Weinberg, Howard S.; Richardson, Susan D.; Pastor, Salvador J.; Chinn, Russell; Sclimenti, Michael J.; Onstad, Gretchen D.; Thruston, Alfred D. Occurrence of a New Generation of Disinfection Byproducts. Environmental Science & Technology. 2006, 40 (23): 7175–7185. doi:10.1021/es060353j.
- ^ 11.0 11.1 Richardson, Susan D.; Plewa, Michael J.; Wagner, Elizabeth D.; Schoeny, Rita; DeMarini, David M. Occurrence, genotoxicity, and carcinogenicity of regulated and emerging disinfection by-products in drinking water: A review and roadmap for research. Mutation Research/Reviews in Mutation Research. 2007, 636 (1–3): 178–242. PMID 17980649. doi:10.1016/j.mrrev.2007.09.001.
- ^ 12.0 12.1 Hakim, Nadey. Artificial Organs. London: Springer-Verlag. 2009: 51 [2014-06-14]. ISBN 9781848822818.
Water that contains chloramine is safe for people to drink, bathe, and cook in because the digestive process neutralizes it. Chloramine can, however, easily harm patients if it enters the blood stream during the dialysis process causing hemolytic anemia.
- ^ 13.0 13.1 Date, S.; Terabayashi, S.; Kobayashi, Y.; Fujime, Y., Effects of chloramines concentration in nutrient solution and exposure time on plant growth in hydroponically cultured lettuce, Scientia Horticulturae, 2005, 103 (3): 257–265, doi:10.1016/j.scienta.2004.06.019
- ^ Fair, G. M., J. C. Morris, S. L. Chang, I. Weil, and R. P. Burden. 1948. The behavior of chlorine as a water disinfectant. J. Am. Water Works Assoc. 40:1051-1061.
