碳酸铍
| 碳酸铍 | |
|---|---|
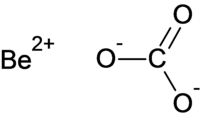
| |
| IUPAC Beryllium Carbonate | |
| 识别 | |
| CAS |
13106-47-3 |
| PubChem | 61577 |
| ChemSpider | 55490 |
| SMILES |
|
| InChI |
|
| InChIKey | ZBUQRSWEONVBES-NUQVWONBAN |
| RTECS | DS2350000 |
| BeCO3 | |
| 69.0202 g·mol⁻¹ | |
| 熔点 | 54 °C |
| 100 °C( | |
| 0.218 g/100 mL (20°C) | |
| 结构 | |
| 热力 | |
| -14.85 kJ/g | |
| 热容 | 0.9417 J/K |
碳酸铍
碱式碳酸铍是
参考 资料
[编辑]- ^ Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0123526515
- ^ David Anthony Everest, 1964, The Chemistry of Beryllium, Elsevier Pub. Co.
- ^ J.E. Macintyre, Dictionary of Inorganic Compounds 1992 CRC Press ISBN 0412301202
| 这是 |
