Χολαγγειοκαρκίνωμα
| Χολαγγειοκαρκίνωμα | |
|---|---|
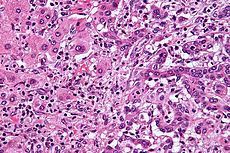 Μικρογραφία ενός χολαγγειοκαρκινώματος (δεξιά | |
| Ειδικότητα | ογκολογία |
| Ταξινόμηση | |
| ICD-10 | C22.1 |
| ICD-9 | 155.1, 156.1 |
| ICD-O | M8160/3 |
| DiseasesDB | 2505 |
| MedlinePlus | 000291 |
| eMedicine | med/343 radio/153 |
| MeSH | D018281 |

Εμφανή συμπτώματα
Σταδιοποίηση[Επεξεργασία | επεξεργασία κώδικα]
Γενικές κατευθυντήριες γραμμές
- Απουσία λεμφαδένων ή ηπατικών μεταστάσεων
- Απουσία εμπλοκής της πυλαίας φλέβας
- Απουσία επέκτασης
τ ο υ όγκουσ ε παρακείμενα όργανα - Απουσία εκτεταμένης μεταστατικής νόσου
Ενδείξεις κ α ι συμπτώματα[Επεξεργασία | επεξεργασία κώδικα]

Παράγοντες κινδύνου[Επεξεργασία | επεξεργασία κώδικα]

Επίσης, ορισμένες παρασιτικές ασθένειες
Παθοφυσιολογία[Επεξεργασία | επεξεργασία κώδικα]
Μολονότι είναι γνωστό ότι
Ιστολογικά,
Διάγνωση[Επεξεργασία | επεξεργασία κώδικα]

Εξετάσεις αίματος[Επεξεργασία | επεξεργασία κώδικα]
Κοιλιακή απεικόνιση[Επεξεργασία | επεξεργασία κώδικα]

Υπέρηχος
Απεικόνιση χοληφόρου δέντρου[Επεξεργασία | επεξεργασία κώδικα]

Ενώ
Χειρουργική επέμβαση[Επεξεργασία | επεξεργασία κώδικα]
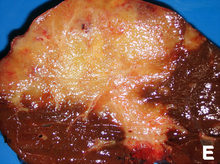
Παθολογία[Επεξεργασία | επεξεργασία κώδικα]
Ιστολογικά,
Θεραπεία[Επεξεργασία | επεξεργασία κώδικα]
Επικουρική θεραπεία κ α ι θεραπεία μ ε ακτινοβολία[Επεξεργασία | επεξεργασία κώδικα]
Εάν
Η θεραπεία της νόσου σ ε προχωρημένο στάδιο[Επεξεργασία | επεξεργασία κώδικα]
Πρόγνωση[Επεξεργασία | επεξεργασία κώδικα]
Επιδημιολογία[Επεξεργασία | επεξεργασία κώδικα]
| Χώρα | ||
|---|---|---|
| 0.60 / 0.43 | 0.70 / 0.87 | |
| Ιαπωνία | 0.23 / 0.10 | 5.87 / 5.20 |
| Αυστραλία | 0.70 / 0.53 | 0.90 / 1.23 |
| Αγγλία/Ουαλία | 0.83 / 0.63 | 0.43 / 0.60 |
| Σκωτία | 1.17 / 1.00 | 0.60 / 0.73 |
| Γαλλία | 0.27 / 0.20 | 1.20 / 1.37 |
| Ιταλία | 0.13 / 0.13 | 2.10 / 2.60 |
Πολλαπλές μελέτες έχουν τεκμηριώσει
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 Landis S, Murray T, Bolden S, Wingo P (1998). «Cancer statistics, 1998». CA Cancer J Clin 48 (1): 6–29. doi:. PMID 9449931.
- ↑ Patel T (2002). «Worldwide trends in mortality from biliary tract malignancies». BMC Cancer 2: 10. doi:. PMID 11991810.
- ↑ Zervos E, Osborne D, Goldin S, Villadolid D, Thometz D, Durkin A, Carey L, Rosemurgy A (2005). «Stage does not predict survival after resection of hilar cholangiocarcinomas promoting an aggressive operative approach». Am J Surg 190 (5): 810–5. doi:. PMID 16226963. https://archive.org/details/sim_american-journal-of-surgery_2005-11_190_5/page/810.
- ↑ 4,0 4,1 4,2 4,3 Mark Feldman, Lawrence S. Friedman, Lawrence J. Brandt, επιμ. (21 Ιουλίου 2006). Sleisenger and Fordtran's Gastrointestinal and Liver Disease (8th έκδοση). Saunders. σελίδες 1493–6. ISBN 978-1-4160-0245-1.
- ↑ Tsao J, Nimura Y, Kamiya J, Hayakawa N, Kondo S, Nagino M, Miyachi M, Kanai M, Uesaka K, Oda K, Rossi R, Braasch J, Dugan J (2000). «Management of Hilar Cholangiocarcinoma: Comparison of an American and a Japanese Experience». Ann Surg 232 (2): 166–74. doi:. PMID 10903592. PMC 1421125. https://archive.org/details/sim_annals-of-surgery_2000-08_232_2/page/166.
- ↑ Rajagopalan V, Daines W, Grossbard M, Kozuch P (2004). «Gallbladder and biliary tract carcinoma: A comprehensive update, Part 1». Oncology (Williston Park) 18 (7): 889–96. PMID 15255172.
- ↑ Nagorney D, Donohue J, Farnell M, Schleck C, Ilstrup D (1993). «Outcomes after curative resections of cholangiocarcinoma». Arch Surg 128 (8): 871–7; discussion 877–9. PMID 8393652.
- ↑ «Bile duct cancer: cause and treatment». Αρχειοθετήθηκε από
τ ο πρωτότυπο στις 23 Απριλίου 2018. Ανακτήθηκε στις 23 Νοεμβρίου 2012. - ↑ 9,0 9,1 Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J (1996). «Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors». Ann Surg 224 (4): 463–73; discussion 473–5. doi:. PMID 8857851. PMC 1235406. https://archive.org/details/sim_annals-of-surgery_1996-10_224_4/page/463.
- ↑ Chapman R (1999). «Risk factors for biliary tract carcinogenesis». Ann Oncol 10 (Suppl 4): 308–11. PMID 10436847.
- ↑ Epidemiologic studies which have addressed the incidence of cholangiocarcinoma in people with primary sclerosing cholangitis include the following:
- Bergquist A, Ekbom A, Olsson R, Kornfeldt D, Lööf L, Danielsson A, Hultcrantz R, Lindgren S, Prytz H, Sandberg-Gertzén H, Almer S, Granath F, Broomé U (2002). «Hepatic and extrahepatic malignancies in primary sclerosing cholangitis». J Hepatol 36 (3): 321–7. doi:. PMID 11867174.
- Bergquist A, Glaumann H, Persson B, Broomé U (1998). «Risk factors and clinical presentation of hepatobiliary carcinoma in patients with primary sclerosing cholangitis: a case-control study». Hepatology 27 (2): 311–6. doi:. PMID 9462625.
- Burak K, Angulo P, Pasha T, Egan K, Petz J, Lindor K (2004). «Incidence and risk factors for cholangiocarcinoma in primary sclerosing cholangitis». Am J Gastroenterol 99 (3): 523–6. doi:. PMID 15056096. https://archive.org/details/sim_american-journal-of-gastroenterology_2004-03_99_3/page/523.
- ↑ 12,0 12,1 12,2 Rosen C, Nagorney D, Wiesner R, Coffey R, LaRusso N (1991). «Cholangiocarcinoma complicating primary sclerosing cholangitis». Ann Surg 213 (1): 21–5. doi:. PMID 1845927. PMC 1358305. https://archive.org/details/sim_annals-of-surgery_1991-01_213_1/page/n30.
- ↑ Watanapa P (1996). «Cholangiocarcinoma in patients with opisthorchiasis». Br J Surg 83 (8): 1062–64. doi:. PMID 8869303. https://archive.org/details/sim_british-journal-of-surgery_1996-08_83_8/page/1062.
- ↑ Watanapa P, Watanapa W (2002). «Liver fluke-associated cholangiocarcinoma». Br J Surg 89 (8): 962–70. doi:. PMID 12153620. https://archive.org/details/sim_british-journal-of-surgery_2002-08_89_8/page/962.
- ↑ Shin H, Lee C, Park H, Seol S, Chung J, Choi H, Ahn Y, Shigemastu T (1996). «Hepatitis B and C virus, Clonorchis sinensis for the risk of liver cancer: a case-control study in Pusan, Korea». Int J Epidemiol 25 (5): 933–40. doi:. PMID 8921477. https://archive.org/details/sim_international-journal-of-epidemiology_1996-10_25_5/page/933.
- ↑ Kobayashi M, Ikeda K, Saitoh S, Suzuki F, Tsubota A, Suzuki Y, Arase Y, Murashima N, Chayama K, Kumada
Η (2000). «Incidence of primary cholangiocellular carcinoma of the liver in Japanese patients with hepatitis C virus-related cirrhosis». Cancer 88 (11): 2471–7. doi:. PMID 10861422. - ↑ Yamamoto S, Kubo S, Hai S, Uenishi T, Yamamoto T, Shuto T, Takemura S, Tanaka H, Yamazaki O, Hirohashi K, Tanaka T (2004). «Hepatitis C virus infection as a likely etiology of intrahepatic cholangiocarcinoma». Cancer Sci 95 (7): 592–5. doi:. PMID 15245596. https://archive.org/details/sim_cancer-science_2004-07_95_7/page/592.
- ↑ Lu H, Ye M, Thung S, Dash S, Gerber M (2000). «Detection of hepatitis C virus RNA sequences in cholangiocarcinomas in Chinese and American patients». Chin Med J (Engl) 113 (12): 1138–41. PMID 11776153.
- ↑ 19,0 19,1 19,2 Shaib Y, El-Serag H, Davila J, Morgan R, McGlynn K (2005). «Risk factors of intrahepatic cholangiocarcinoma in the United States: a case-control study». Gastroenterology 128 (3): 620–6. doi:. PMID 15765398. https://archive.org/details/sim_gastroenterology_2005-03_128_3/page/620.
- ↑ Sorensen H, Friis S, Olsen J, Thulstrup A, Mellemkjaer L, Linet M, Trichopoulos D, Vilstrup H, Olsen J (1998). «Risk of liver and other types of cancer in patients with cirrhosis: a nationwide cohort study in Denmark». Hepatology 28 (4): 921–5. doi:. PMID 9755226. https://archive.org/details/sim_hepatology_1998-10_28_4/page/921.
- ↑ Lipsett P, Pitt H, Colombani P, Boitnott J, Cameron J (1994). «Choledochal cyst disease. A changing pattern of presentation». Ann Surg 220 (5): 644–52. doi:. PMID 7979612. PMC 1234452. https://archive.org/details/sim_annals-of-surgery_1994-11_220_5/page/644.
- ↑ Dayton M, Longmire W, Tompkins R (1983). «Caroli's Disease: a premalignant condition?». Am J Surg 145 (1): 41–8. doi:. PMID 6295196.
- ↑ Mecklin J, Järvinen H, Virolainen M (1992). «The association between cholangiocarcinoma and hereditary nonpolyposis colorectal carcinoma». Cancer 69 (5): 1112–4. doi:. PMID 1310886.
- ↑ Lee S, Kim M, Lee S, Jang S, Song M, Kim K, Kim H, Seo D, Song D, Yu E, Lee S, Min Y (2004). «Clinicopathologic review of 58 patients with biliary papillomatosis». Cancer 100 (4): 783–93. doi:. PMID 14770435.
- ↑ Lee C, Wu C, Chen G (2002). «What is the impact of coexistence of hepatolithiasis on cholangiocarcinoma?». J Gastroenterol Hepatol 17 (9): 1015–20. doi:. PMID 12167124. https://archive.org/details/sim_journal-of-gastroenterology-and-hepatology_2002_17_9/page/1015.
- ↑ Su C, Shyr Y, Lui W, P'Eng F (1997). «Hepatolithiasis associated with cholangiocarcinoma». Br J Surg 84 (7): 969–73. doi:. PMID 9240138. https://archive.org/details/sim_british-journal-of-surgery_1997-07_84_7/page/969.
- ↑ Donato F, Gelatti U, Tagger A, Favret M, Ribero M, Callea F, Martelli C, Savio A, Trevisi P, Nardi G (2001). «Intrahepatic cholangiocarcinoma and hepatitis C and B virus infection, alcohol intake, and hepatolithiasis: a case-control study in Italy». Cancer Causes Control 12 (10): 959–64. doi:. PMID 11808716.
- ↑ Sahani D, Prasad S, Tannabe K, Hahn P, Mueller P, Saini S (2003). «Thorotrast-induced cholangiocarcinoma: case report». Abdom Imaging 28 (1): 72–4. doi:. PMID 12483389.
- ↑ Zhu A, Lauwers G, Tanabe K (2004). «Cholangiocarcinoma in association with Thorotrast exposure». J Hepatobiliary Pancreat Surg 11 (6): 430–3. doi:. PMID 15619021.
- ↑ Klatskin G (1965). «Adenocarcinoma Of The Hepatic Duct At Its Bifurcation Within The Porta Hepatis. An Unusual Tumor With Distinctive Clinical And Pathological Features». Am J Med 38 (2): 241–56. doi:. PMID 14256720. https://archive.org/details/sim_american-journal-of-medicine_1965-02_38_2/page/241.
- ↑ Roskams T (2006). «Liver stem cells and their implication in hepatocellular and cholangiocarcinoma». Oncogene 25 (27): 3818–22. doi:. PMID 16799623.
- ↑ Liu C, Wang J, Ou Q (2004). «Possible stem cell origin of human cholangiocarcinoma». World J Gastroenterol 10 (22): 3374–6. PMID 15484322.
- ↑ Sell S, Dunsford
Η (1989). «Evidence for the stem cell origin of hepatocellular carcinoma and cholangiocarcinoma». Am J Pathol 134 (6): 1347–63. PMID 2474256. PMC 1879951. https://archive.org/details/sim_american-journal-of-pathology_1989-06_134_6/page/1347. - ↑ 34,0 34,1 Sirica A (2005). «Cholangiocarcinoma: molecular targeting strategies for chemoprevention and therapy». Hepatology 41 (1): 5–15. doi:. PMID 15690474.
- ↑ Holzinger F, Z'graggen K, Büchler M (1999). «Mechanisms of biliary carcinogenesis: a pathogenetic multi-stage cascade towards cholangiocarcinoma». Ann Oncol 10 (Suppl 4): 122–6. PMID 10436802.
- ↑ Gores G (2003). «Cholangiocarcinoma: current concepts and insights». Hepatology 37 (5): 961–9. doi:. PMID 12717374. https://archive.org/details/sim_hepatology_2003-05_37_5/page/961.
- ↑ de Groen P, Gores G, LaRusso N, Gunderson L, Nagorney D (1999). «Biliary tract cancers». N Engl J Med 341 (18): 1368–78. doi:. PMID 10536130.
- ↑ 38,0 38,1 Henson D, Albores-Saavedra J, Corle D (1992). «Carcinoma of the extrahepatic bile ducts. Histologic types, stage of disease, grade, and survival rates». Cancer 70 (6): 1498–501. doi:. PMID 1516001.
- ↑ Studies of the performance of serum markers for cholangiocarcinoma (such as carcinoembryonic antigen and CA19-9) in patients with and without primary sclerosing cholangitis include the following:
- Nehls O, Gregor M, Klump B (2004). «Serum and bile markers for cholangiocarcinoma». Semin Liver Dis 24 (2): 139–54. doi:. PMID 15192787. https://archive.org/details/sim_seminars-in-liver-disease_2004-05_24_2/page/139.
- Siqueira E, Schoen R, Silverman W, Martin J, Rabinovitz M, Weissfeld J, Abu-Elmaagd K, Madariaga J, Slivka A, Martini J (2002). «Detecting cholangiocarcinoma in patients with primary sclerosing cholangitis». Gastrointest Endosc 56 (1): 40–7. doi:. PMID 12085033. https://archive.org/details/sim_gastrointestinal-endoscopy_2002-07_56_1/page/40.
- Levy C, Lymp J, Angulo P, Gores G, Larusso N, Lindor K (2005). «The value of serum CA 19-9 in predicting cholangiocarcinomas in patients with primary sclerosing cholangitis». Dig Dis Sci 50 (9): 1734–40. doi:. PMID 16133981. https://archive.org/details/sim_digestive-diseases-and-sciences_2005-09_50_9/page/1734.
- Patel A, Harnois D, Klee G, LaRusso N, Gores G (2000). «The utility of CA 19-9 in the diagnoses of cholangiocarcinoma in patients without primary sclerosing cholangitis». Am J Gastroenterol 95 (1): 204–7. doi:. PMID 10638584. https://archive.org/details/sim_american-journal-of-gastroenterology_2000-01_95_1/page/204.
- ↑ Saini S (1997). «Imaging of the hepatobiliary tract». N Engl J Med 336 (26): 1889–94. doi:. PMID 9197218.
- ↑ Sharma M, Ahuja V (1999). «Aetiological spectrum of obstructive jaundice and diagnostic ability of ultrasonography: a clinician's perspective». Trop Gastroenterol 20 (4): 167–9. PMID 10769604.
- ↑ Bloom C, Langer B, Wilson S (1999). «Role of US in the detection, characterization, and staging of cholangiocarcinoma». Radiographics 19 (5): 1199–218. PMID 10489176.
- ↑ Valls C, Gumà A, Puig I, Sanchez A, Andía E, Serrano T, Figueras J (2000). «Intrahepatic peripheral cholangiocarcinoma: CT evaluation». Abdom Imaging 25 (5): 490–6. doi:. PMID 10931983.
- ↑ Tillich M, Mischinger H, Preisegger K, Rabl H, Szolar D (1998). «Multiphasic helical CT in diagnosis and staging of hilar cholangiocarcinoma». AJR Am J Roentgenol 171 (3): 651–8. PMID 9725291.
- ↑ Zhang Y, Uchida M, Abe T, Nishimura H, Hayabuchi N, Nakashima Y (1999). «Intrahepatic peripheral cholangiocarcinoma: comparison of dynamic CT and dynamic MRI». J Comput Assist Tomogr 23 (5): 670–7. doi:. PMID 10524843.
- ↑ Sugiyama M, Hagi H, Atomi Y, Saito M (1997). «Diagnosis of portal venous invasion by pancreatobiliary carcinoma: value of endoscopic ultrasonography». Abdom Imaging 22 (4): 434–8. doi:. PMID 9157867.
- ↑ Schwartz L, Coakley F, Sun Y, Blumgart L, Fong Y, Panicek D (1998). «Neoplastic pancreaticobiliary duct obstruction: evaluation with breath-hold MR cholangiopancreatography». AJR Am J Roentgenol 170 (6): 1491–5. PMID 9609160.
- ↑ Zidi S, Prat F, Le Guen O, Rondeau Y, Pelletier G (2000). «Performance characteristics of magnetic resonance cholangiography in the staging of malignant hilar strictures». Gut 46 (1): 103–6. doi:. PMID 10601064. PMC 1727781. https://archive.org/details/sim_gut_2000-01_46_1/page/103.
- ↑ Lee M, Park K, Shin Y, Yoon H, Sung K, Kim M, Lee S, Kang E (2003). «Preoperative evaluation of hilar cholangiocarcinoma with contrast-enhanced three-dimensional fast imaging with steady-state precession magnetic resonance angiography: comparison with intraarterial digital subtraction angiography». World J Surg 27 (3): 278–83. doi:. PMID 12607051. https://archive.org/details/sim_world-journal-of-surgery_2003-03_27_3/page/278.
- ↑ Yeh T, Jan Y, Tseng J, Chiu C, Chen T, Hwang T, Chen M (2000). «Malignant perihilar biliary obstruction: magnetic resonance cholangiopancreatographic findings». Am J Gastroenterol 95 (2): 432–40. doi:. PMID 10685746. https://archive.org/details/sim_american-journal-of-gastroenterology_2000-02_95_2/page/432.
- ↑ Freeman M, Sielaff T (2003). «A modern approach to malignant hilar biliary obstruction». Rev Gastroenterol Disord 3 (4): 187–201. PMID 14668691.
- ↑ Szklaruk J, Tamm E, Charnsangavej C (2002). «Preoperative imaging of biliary tract cancers». Surg Oncol Clin N Am 11 (4): 865–76. doi:. PMID 12607576.
- ↑ Weber S, DeMatteo R, Fong Y, Blumgart L, Jarnagin W (2002). «Staging Laparoscopy in Patients With Extrahepatic Biliary Carcinoma: Analysis of 100 Patients». Ann Surg 235 (3): 392–9. doi:. PMID 11882761. PMC 1422445. https://archive.org/details/sim_annals-of-surgery_2002-03_235_3/page/392.
- ↑ Callery M, Strasberg S, Doherty G, Soper N, Norton J (1997). «Staging laparoscopy with laparoscopic ultrasonography: optimizing resectability in hepatobiliary and pancreatic malignancy». J Am Coll Surg 185 (1): 33–9. PMID 9208958. https://archive.org/details/sim_journal-of-the-american-college-of-surgeons_1997-07_185_1/page/33.
- ↑ Länger F, von Wasielewski R, Kreipe HH (2006). «[The importance of immunohistochemistry for the diagnosis of cholangiocarcinomas]» (
σ τ α German). Pathologe 27 (4): 244–50. doi:. PMID 16758167. - ↑ Darwin PE, Kennedy A. Cholangiocarcinoma
σ τ ο eMedicine - ↑ Su C, Tsay S, Wu C, Shyr Y, King K, Lee C, Lui W, Liu T, P'eng F (1996). «Factors influencing postoperative morbidity, mortality, and survival after resection for hilar cholangiocarcinoma». Ann Surg 223 (4): 384–94. doi:. PMID 8633917. PMC 1235134. https://archive.org/details/sim_annals-of-surgery_1996-04_223_4/page/384.
- ↑ Heimbach JK, Gores GJ, Haddock MG, et al. (December 2006). «Predictors of disease recurrence following neoadjuvant chemoradiotherapy and liver transplantation for unresectable perihilar cholangiocarcinoma». Transplantation 82 (12): 1703–7. doi:. PMID 17198263. Αρχειοθετήθηκε από
τ ο πρωτότυπο στις 2013-05-22. https://web.archive.org/web/20130522223146/http://meta.wkhealth.com/pt/pt-core/template-journal/lwwgateway/media/landingpage.htm?issn=0041-1337&volume=82&issue=12&spage=1703. Ανακτήθηκε στις 2012-11-24. - ↑ Todoroki T, Ohara K, Kawamoto T, Koike N, Yoshida S, Kashiwagi H, Otsuka M, Fukao K (2000). «Benefits of adjuvant radiotherapy after radical resection of locally advanced main hepatic duct carcinoma». Int J Radiat Oncol Biol Phys 46 (3): 581–7. doi:. PMID 10701737.
- ↑ Alden M, Mohiuddin M (1994). «The impact of radiation dose in combined external beam and intraluminal Ir-192 brachytherapy for bile duct cancer». Int J Radiat Oncol Biol Phys 28 (4): 945–51. doi:. PMID 8138448.
- ↑ González González D, Gouma D, Rauws E, van Gulik T, Bosma A, Koedooder C (1999). «Role of radiotherapy, in particular intraluminal brachytherapy, in the treatment of proximal bile duct carcinoma». Ann Oncol 10 (Suppl 4): 215–20. PMID 10436826.
- ↑ Pitt H, Nakeeb A, Abrams R, Coleman J, Piantadosi S, Yeo C, Lillemore K, Cameron J (1995). «Perihilar cholangiocarcinoma. Postoperative radiotherapy does not improve survival». Ann Surg 221 (6): 788–97; discussion 797–8. doi:. PMID 7794082. PMC 1234714. https://archive.org/details/sim_annals-of-surgery_1995-06_221_6/page/788.
- ↑ Takada T, Amano H, Yasuda H, Nimura Y, Matsushiro T, Kato H, Nagakawa T, Nakayama T (2002). «Is postoperative adjuvant chemotherapy useful for gallbladder carcinoma? A phase III multicenter prospective randomized controlled trial in patients with resected pancreaticobiliary carcinoma». Cancer 95 (8): 1685–95. doi:. PMID 12365016.
- ↑ 64,0 64,1 National Comprehensive Cancer Network (NCCN) guidelines on evaluation and treatment of hepatobiliary malignancies PDF (216 KB). Accessed March 13, 2007.
- ↑ Vauthey J, Blumgart L (1994). «Recent advances in the management of cholangiocarcinomas». Semin. Liver Dis. 14 (2): 109–14. doi:. PMID 8047893. https://archive.org/details/sim_seminars-in-liver-disease_1994-05_14_2/page/109.
- ↑ Glimelius B, Hoffman K, Sjödén P, Jacobsson G, Sellström H, Enander L, Linné T, Svensson C (1996). «Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer». Ann Oncol 7 (6): 593–600. PMID 8879373. https://archive.org/details/sim_annals-of-oncology_1996-08_7_6/page/593.
- ↑ Choi C, Choi I, Seo J, Kim B, Kim J, Kim C, Um S, Kim J, Kim Y (2000). «Effects of 5-fluorouracil and leucovorin in the treatment of pancreatic-biliary tract adenocarcinomas». Am J Clin Oncol 23 (4): 425–8. doi:. PMID 10955877.
- ↑ Park J, Oh S, Kim S, Kwon H, Kim J, Jin-Kim H, Kim Y (2005). «Single-agent gemcitabine in the treatment of advanced biliary tract cancers: a phase II study». Jpn J Clin Oncol 35 (2): 68–73. doi:. PMID 15709089.
- ↑ Giuliani F, Gebbia V, Maiello E, Borsellino N, Bajardi E, Colucci G (2006). «Gemcitabine and cisplatin for inoperable and/or metastatic biliary tree carcinomas: a multicenter phase II study of the Gruppo Oncologico dell'Italia Meridionale (GOIM)». Ann Oncol 17 (Suppl 7): vii73–7. doi:. PMID 16760299.
- ↑ Bhargava P, Jani C, Savarese D, O'Donnell J, Stuart K, Rocha Lima C (2003). «Gemcitabine and irinotecan in locally advanced or metastatic biliary cancer: preliminary report». Oncology (Williston Park) 17 (9 Suppl 8): 23–6. PMID 14569844.
- ↑ Knox J, Hedley D, Oza A, Feld R, Siu L, Chen E, Nematollahi M, Pond G, Zhang J, Moore M (2005). «Combining gemcitabine and capecitabine in patients with advanced biliary cancer: a phase II trial». J Clin Oncol 23 (10): 2332–8. doi:. PMID 15800324.
- ↑ Philip P, Mahoney M, Allmer C, Thomas J, Pitot H, Kim G, Donehower R, Fitch T, Picus J, Erlichman C (2006). «Phase II study of erlotinib in patients with advanced biliary cancer». J Clin Oncol 24 (19): 3069–74. doi:. PMID 16809731.
- ↑ Ortner M, Caca K, Berr F, Liebetruth J, Mansmann U, Huster D, Voderholzer W, Schachschal G, Mössner J, Lochs
Η (2003). «Successful photodynamic therapy for nonresectable cholangiocarcinoma: a randomized prospective study». Gastroenterology 125 (5): 1355–63. doi:. PMID 14598251. https://archive.org/details/sim_gastroenterology_2003-11_125_5/page/1355. - ↑ Zoepf T, Jakobs R, Arnold J, Apel D, Riemann J (2005). «Palliation of nonresectable bile duct cancer: improved survival after photodynamic therapy». Am J Gastroenterol 100 (11): 2426–30. doi:. PMID 16279895. https://archive.org/details/sim_american-journal-of-gastroenterology_2005-11_100_11/page/2426.
- ↑ Talreja JP, Kahaleh M (September 2010). «Photodynamic therapy for cholangiocarcinoma». Gut Liver 4 Suppl 1: S62–6. doi:. PMID 21103297. PMC 2989550. http://gutnliver.org/journal/journal_view.html?year=2010&vol=4%20Suppl%201&num=00&page=S62.
- ↑ Yamamoto M, Takasaki K, Yoshikawa T (1999). «Lymph Node Metastasis in Intrahepatic Cholangiocarcinoma». Japanese Journal of Clinical Oncology 29 (3): 147–150. doi:. PMID 10225697.
- ↑ Farley D, Weaver A, Nagorney D (1995). «"Natural history" of unresected cholangiocarcinoma: patient outcome after noncurative intervention». Mayo Clin Proc 70 (5): 425–9. doi:. PMID 7537346. https://archive.org/details/sim_mayo-clinic-proceedings_1995-05_70_5/page/425.
- ↑ Grove MK, Hermann RE, Vogt DP, Broughan TA (1991). «Role of radiation after operative palliation in cancer of the proximal bile ducts». Am J Surg 161 (4): 454–458. doi:. PMID 1709795. https://archive.org/details/sim_american-journal-of-surgery_1991-04_161_4/page/454.
- ↑ Studies of surgical outcomes in distal cholangiocarcinoma include:
- Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J (1996). «Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors». Ann Surg 224 (4): 463–73; discussion 473–5. doi:. PMID 8857851. PMC 1235406. https://archive.org/details/sim_annals-of-surgery_1996-10_224_4/page/463.
- Nagorney D, Donohue J, Farnell M, Schleck C, Ilstrup D (1993). «Outcomes after curative resections of cholangiocarcinoma». Arch Surg 128 (8): 871–7; discussion 877–9. PMID 8393652.
- Jang J, Kim S, Park D, Ahn Y, Yoon Y, Choi M, Suh K, Lee K, Park Y (2005). «Actual Long-term Outcome of Extrahepatic Bile Duct Cancer After Surgical Resection». Ann Surg 241 (1): 77–84. PMID 15621994. PMC 1356849. https://archive.org/details/sim_annals-of-surgery_2005-01_241_1/page/77.
- Bortolasi L, Burgart L, Tsiotos G, Luque-De León E, Sarr M (2000). «Adenocarcinoma of the distal bile duct. A clinicopathologic outcome analysis after curative resection». Dig Surg 17 (1): 36–41. doi:. PMID 10720830.
- Fong Y, Blumgart L, Lin E, Fortner J, Brennan M (1996). «Outcome of treatment for distal bile duct cancer». Br J Surg 83 (12): 1712–5. doi:. PMID 9038548. https://archive.org/details/sim_british-journal-of-surgery_1996-12_83_12/page/1712.
- ↑ Studies of outcome in intrahepatic cholangiocarcinoma include:
- Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J (1996). «Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors». Ann Surg 224 (4): 463–73; discussion 473–5. doi:. PMID 8857851. PMC 1235406. https://archive.org/details/sim_annals-of-surgery_1996-10_224_4/page/463.
- Lieser M, Barry M, Rowland C, Ilstrup D, Nagorney D (1998). «Surgical management of intrahepatic cholangiocarcinoma: a 31-year experience». J Hepatobiliary Pancreat Surg 5 (1): 41–7. doi:. PMID 9683753.
- Valverde A, Bonhomme N, Farges O, Sauvanet A, Flejou J, Belghiti J (1999). «Resection of intrahepatic cholangiocarcinoma: a Western experience». J Hepatobiliary Pancreat Surg 6 (2): 122–7. doi:. PMID 10398898.
- Nakagohri T, Asano T, Kinoshita H, Kenmochi T, Urashima T, Miura F, Ochiai T (2003). «Aggressive surgical resection for hilar-invasive and peripheral intrahepatic cholangiocarcinoma». World J Surg 27 (3): 289–93. doi:. PMID 12607053. https://archive.org/details/sim_world-journal-of-surgery_2003-03_27_3/page/289.
- Weber S, Jarnagin W, Klimstra D, DeMatteo R, Fong Y, Blumgart L (2001). «Intrahepatic cholangiocarcinoma: resectability, recurrence pattern, and outcomes». J Am Coll Surg 193 (4): 384–91. doi:. PMID 11584966. https://archive.org/details/sim_journal-of-the-american-college-of-surgeons_2001-10_193_4/page/384.
- ↑ Estimates of survival after surgery for perihilar cholangiocarcinoma include:
- Burke E, Jarnagin W, Hochwald S, Pisters P, Fong Y, Blumgart L (1998). «Hilar Cholangiocarcinoma: patterns of spread, the importance of hepatic resection for curative operation, and a presurgical clinical staging system». Ann Surg 228 (3): 385–94. doi:. PMID 9742921. PMC 1191497. https://archive.org/details/sim_annals-of-surgery_1998-09_228_3/page/385.
- Tsao J, Nimura Y, Kamiya J, Hayakawa N, Kondo S, Nagino M, Miyachi M, Kanai M, Uesaka K, Oda K, Rossi R, Braasch J, Dugan J (2000). «Management of Hilar Cholangiocarcinoma: Comparison of an American and a Japanese Experience». Ann Surg 232 (2): 166–74. doi:. PMID 10903592. PMC 1421125. https://archive.org/details/sim_annals-of-surgery_2000-08_232_2/page/166.
- Chamberlain R, Blumgart L (2000). «Hilar cholangiocarcinoma: a review and commentary». Ann Surg Oncol 7 (1): 55–66. doi:. PMID 10674450.
- Washburn W, Lewis W, Jenkins R (1995). «Aggressive surgical resection for cholangiocarcinoma». Arch Surg 130 (3): 270–6. PMID 7534059.
- Nagino M, Nimura Y, Kamiya J, Kanai M, Uesaka K, Hayakawa N, Yamamoto H, Kondo S, Nishio
Η (1998). «Segmental liver resections for hilar cholangiocarcinoma». Hepatogastroenterology 45 (19): 7–13. PMID 9496478. - Rea D, Munoz-Juarez M, Farnell M, Donohue J, Que F, Crownhart B, Larson D, Nagorney D (2004). «Major hepatic resection for hilar cholangiocarcinoma: analysis of 46 patients». Arch Surg 139 (5): 514–23; discussion 523–5. doi:. PMID 15136352.
- Launois B, Reding R, Lebeau G, Buard J (2000). «Surgery for hilar cholangiocarcinoma: French experience in a collective survey of 552 extrahepatic bile duct cancers». J Hepatobiliary Pancreat Surg 7 (2): 128–34. doi:. PMID 10982604.
- ↑ Kaya M, de Groen P, Angulo P, Nagorney D, Gunderson L, Gores G, Haddock M, Lindor K (2001). «Treatment of cholangiocarcinoma complicating primary sclerosing cholangitis: the Mayo Clinic experience». Am J Gastroenterol 96 (4): 1164–9. doi:. PMID 11316165. https://archive.org/details/sim_american-journal-of-gastroenterology_2001-04_96_4/page/1164.
- ↑ Nakeeb A, Tran K, Black M, Erickson B, Ritch P, Quebbeman E, Wilson S, Demeure M, Rilling W, Dua K, Pitt
Η (2002). «Improved survival in resected biliary malignancies». Surgery 132 (4): 555–63; discission 563–4. doi:. PMID 12407338. https://archive.org/details/sim_surgery_2002-10_132_4/page/555. - ↑ «Introduction». Αρχειοθετήθηκε από
τ ο πρωτότυπο στις 12 Μαρτίου 2009. Ανακτήθηκε στις 24 Νοεμβρίου 2012. - ↑ http://seer.cancer.gov/csr/1975_2005/results_single/sect_01_table.01.pdf
- ↑ Khan S, Taylor-Robinson S, Toledano M, Beck A, Elliott P, Thomas
Η (2002). «Changing international trends in mortality rates for liver, biliary and pancreatic tumours». J Hepatol 37 (6): 806–13. doi:. PMID 12445422. - ↑ Vauthey J, Blumgart L (1994). «Recent advances in the management of cholangiocarcinomas». Semin Liver Dis 14 (2): 109–14. doi:. PMID 8047893. https://archive.org/details/sim_seminars-in-liver-disease_1994-05_14_2/page/109.
- ↑ Cancer Statistics Home Page — National Cancer Institute
- ↑ Multiple independent studies have documented a steady increase in the worldwide incidence of cholangiocarcinoma. Some relevant journal articles include:
- Patel T (2002). «Worldwide trends in mortality from biliary tract malignancies». BMC Cancer 2: 10. doi:. PMID 11991810.
- Patel T (2001). «Increasing incidence and mortality of primary intrahepatic cholangiocarcinoma in the United States». Hepatology 33 (6): 1353–7. doi:. PMID 11391522. https://archive.org/details/sim_hepatology_2001-06_33_6/page/1353.
- Shaib Y, Davila J, McGlynn K, El-Serag
Η (2004). «Rising incidence of intrahepatic cholangiocarcinoma in the United States: a true increase?». J Hepatol 40 (3): 472–7. doi:. PMID 15123362. - West J, Wood H, Logan R, Quinn M, Aithal G (2006). «Trends in the incidence of primary liver and biliary tract cancers in England and Wales 1971–2001». Br J Cancer 94 (11): 1751–8. doi:. PMID 16736026.
- Khan S, Taylor-Robinson S, Toledano M, Beck A, Elliott P, Thomas
Η (2002). «Changing international trends in mortality rates for liver, biliary and pancreatic tumours». J Hepatol 37 (6): 806–13. doi:. PMID 12445422. - Welzel T, McGlynn K, Hsing A, O'Brien T, Pfeiffer R (2006). «Impact of classification of hilar cholangiocarcinomas (Klatskin tumors) on the incidence of intra- and extrahepatic cholangiocarcinoma in the United States». J Natl Cancer Inst 98 (12): 873–5. doi:. PMID 16788161.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- American Cancer Society Detailed Guide to Bile Duct Cancer Αρχειοθετήθηκε 2007-03-10
σ τ ο Wayback Machine.. - Patient information on extrahepatic bile duct tumors, from the National Cancer Institute.
- Cancer.Net: Bile Duct Cancer
- The Cholangiocarcinoma Foundation: a resource for patients, friends, caregivers and loved ones of those affected by bile duct cancer.
- The Alan Morement Memorial Fund, the UK's only charity dedicated to the disease
- Macmillan/Cancerbackup page on Cholangiocarcinoma

