図 ず 水酸化物 すいさんかぶつ 間 あいだ 分子 ぶんし 的 てき 求 もとめ 核 かく 置換 ちかん SN 2 )反応 はんのう 反応 はんのう 座標 ざひょう 図 ず 遷移 せんい 状態 じょうたい 理論 りろん 英 えい Transition state theory 、略称 りゃくしょう TST )は、素 す 化学 かがく 反応 はんのう 反応 はんのう 速度 そくど 説明 せつめい 本 ほん 理論 りろん 反応 はんのう 物 ぶつ 活性 かっせい 化 か 遷移 せんい 状態 じょうたい 複 ふく 合体 がったい 間 あいだ 特別 とくべつ 種類 しゅるい 化学 かがく 平衡 へいこう 擬 なずらえ 平衡 へいこう 準 じゅん 平衡 へいこう 仮定 かてい [1]
TSTは、どのように化学 かがく 反応 はんのう 起 お 定性的 ていせいてき 理解 りかい 主 おも 使 つか 絶対 ぜったい 反応 はんのう 速度 そくど 定数 ていすう 計算 けいさん 当初 とうしょ 目標 もくひょう 成功 せいこう 絶対 ぜったい 反応 はんのう 速度 そくど 計算 けいさん ポテンシャルエネルギー面 めん の正確 せいかく 情報 じょうほう 必要 ひつよう [2] 速度 そくど 定数 ていすう 実験 じっけん 的 てき 決定 けってい 特定 とくてい 反応 はんのう 標準 ひょうじゅん 活性 かっせい 化 か エンタルピー (Δ でるた H ‡ 、Δ でるた ‡ H ɵ とも書 か 標準 ひょうじゅん 活性 かっせい 化 か (英語 えいご 版 ばん Δ でるた S ‡ またはΔ でるた ‡ S ɵ )、および標準 ひょうじゅん 活性 かっせい 化 か ギブズエネルギー (Δ でるた G ‡ またはΔ でるた ‡ G ɵ )の計算 けいさん 成功 せいこう ‡ 表記 ひょうき 興味 きょうみ 値 ね 遷移 せんい 状態 じょうたい 指 さ Δ でるた H ‡ は遷移 せんい 状態 じょうたい 反応 はんのう 物 ぶつ 差 さ
この理論 りろん 年 ねん 当時 とうじ プリンストン大学 ぷりんすとんだいがく ヘンリー・アイリング と(マンチェスター大学 だいがく の)メレディス・グウィン・エヴァンス (英語 えいご 版 ばん マイケル・ポランニー によって同時 どうじ 構築 こうちく [3] [4] 活性 かっせい 合体 がったい 理論 りろん 絶対 ぜったい 速度 そくど 理論 りろん 絶対 ぜったい 反応 はんのう 速度 そくど 理論 りろん 呼 よ [5]
TSTの構築 こうちく 前 まえ 速度 そくど 則 そく 反応 はんのう 障壁 しょうへき 決定 けってい 広 ひろ 使 つか アレニウスの式 しき は経験 けいけん 的 てき 観察 かんさつ 導 みちび 以上 いじょう 反応 はんのう 中 ちゅう 間 あいだ 体 たい 反応 はんのう 物 ぶつ 始原 しげん 系 けい 生成 せいせい 物 ぶつ 生成 せいせい 系 けい 変換 へんかん 関与 かんよ 機構 きこう 的 てき 考察 こうさつ 無視 むし [6] 法則 ほうそく 関連 かんれん 前 ぜん 指数 しすう 因子 いんし (英語 えいご 版 ばん A )と活性 かっせい 化 か E a )を理解 りかい 理論 りろん 発展 はってん 必要 ひつよう アイリングの式 しき をもたらしたTSTはこれら2つの問題 もんだい 解決 かいけつ 成功 せいこう 速度 そくど 則 そく 発表 はっぴょう 年 ねん 式 しき 導 みちび 年 ねん 年 ねん 経過 けいか 間 あいだ 多 おお 科学 かがく 者 しゃ 研究 けんきゅう 者 しゃ 理論 りろん 発展 はってん 大 おお 貢献 こうけん
遷移 せんい 状態 じょうたい 理論 りろん 背景 はいけい 基本 きほん 的 てき 考 かんが 方 かた 以下 いか 通 とお
反応 はんのう 速度 そくど ポテンシャルエネルギー面 めん の鞍点 あんてん 近 ちか 活性 かっせい 複 ふく 合体 がったい 活性 かっせい 合体 がったい 調 しら 研究 けんきゅう 複 ふく 合体 がったい 形成 けいせい 詳細 しょうさい 重要 じゅうよう 鞍点 あんてん 自身 じしん 遷移 せんい 状態 じょうたい 呼 よ 活性 かっせい 複 ふく 合体 がったい 反応 はんのう 物 ぶつ 分子 ぶんし 特別 とくべつ 平衡 へいこう 擬 なずらえ 平衡 へいこう 活性 かっせい 複 ふく 合体 がったい 生成 せいせい 物 ぶつ 変換 へんかん 変換 へんかん 速度 そくど 計算 けいさん 運動 うんどう 論 ろん 使用 しよう TSTの発展 はってん 以下 いか 要約 ようやく 取 と
1884年 ねん ヤコブス・ファント・ホッフ は、可逆 かぎゃく 反応 はんのう 平衡 へいこう 定数 ていすう 温度 おんど 依存 いぞん 性 せい 記述 きじゅつ ファントホッフの式 しき を提唱 ていしょう
A
↽
−
−
⇀
B
{\displaystyle {\ce {{A}<=> {B}}}}
d
ln
K
d
T
=
Δ でるた U
R
T
2
{\displaystyle {\frac {d\ln K}{dT}}={\frac {\Delta U}{RT^{2}}}}
上 うえ 式 しき Δ でるた U は内部 ないぶ 変化 へんか k は反応 はんのう 平衡 へいこう 定数 ていすう R は気体 きたい 定数 ていすう T は熱 ねつ 力学 りきがく 的 てき 温度 おんど 実験 じっけん 結果 けっか 基 もと 年 ねん スヴァンテ・アレニウス は反応 はんのう 速度 そくど 定数 ていすう 同様 どうよう 式 しき 提唱 ていしょう
d
ln
k
d
T
=
Δ でるた E
R
T
2
{\displaystyle {\frac {d\ln k}{dT}}={\frac {\Delta E}{RT^{2}}}}
この式 しき 積分 せきぶん アレニウスの式 しき
k
=
A
e
−
E
a
/
R
T
{\displaystyle k=Ae^{-E_{a}/RT}}
が導 みちび k は速度 そくど 定数 ていすう A は頻度 ひんど 因子 いんし 現在 げんざい 前 ぜん 指数 しすう 因子 いんし 呼 よ 呼 よ E a は活性 かっせい 化 か 見 み 世紀 せいき 初頭 しょとう 多 おお 科学 かがく 者 しゃ 式 しき 受 う 入 い A およびE a の物理 ぶつり 学 がく 的 てき 解釈 かいしゃく 漠然 ばくぜん 化学 かがく 反応 はんのう 速度 そくど 論 ろん 多 おお 研究 けんきゅう 者 しゃ A とE a を化学 かがく 反応 はんのう 必要 ひつよう 分子 ぶんし 運動 うんどう 直接的 ちょくせつてき 結 むす 付 つ 試 こころ 化学 かがく 反応 はんのう 起 お 様々 さまざま 理論 りろん 提唱 ていしょう [要 よう 出典 しゅってん 。
1910年 ねん 化学 かがく 者 しゃ ルネ・マルセラン (英語 えいご 版 ばん 標準 ひょうじゅん 活性 かっせい 化 か 概念 がいねん 導入 どうにゅう
k
∝
exp
(
−
Δ でるた
‡
G
⊖
R
T
)
{\displaystyle k\propto \exp \left({\frac {-\Delta ^{\ddagger }G^{\ominus }}{RT}}\right)}
と書 か
マルスランが彼 かれ 理論 りろん 構築 こうちく 研究 けんきゅう 同 おな 頃 ごろ 化学 かがく 者 しゃ 標準 ひょうじゅん 活性 かっせい 化 か 標準 ひょうじゅん 活性 かっせい 化 か 導入 どうにゅう 彼 かれ 以下 いか 反応 はんのう 速度 そくど 式 しき 提唱 ていしょう
k
∝
exp
(
Δ でるた
‡
S
⊖
R
)
exp
(
−
Δ でるた
‡
H
⊖
R
T
)
{\displaystyle k\propto \exp \left({\frac {\Delta ^{\ddagger }S^{\ominus }}{R}}\right)\exp \left({\frac {-\Delta ^{\ddagger }H^{\ominus }}{RT}}\right)}
しかしながら、この定数 ていすう 本質 ほんしつ 不明 ふめい
1900年 ねん 初頭 しょとう マックス・トラウツ (英語 えいご 版 ばん ウィリアム・ルイス (英語 えいご 版 ばん 気体 きたい 分子 ぶんし 運動 うんどう 論 ろん 基 もと 衝突 しょうとつ 理論 りろん (英語 えいご 版 ばん 使 つか 反応 はんのう 速度 そくど 研究 けんきゅう 衝突 しょうとつ 理論 りろん 反応 はんのう 分子 ぶんし 互 たが 衝突 しょうとつ 剛体 ごうたい 球 だま 扱 あつか 理論 りろん 分子 ぶんし 間 あいだ 衝突 しょうとつ 完全 かんぜん 弾性 だんせい 的 てき 仮定 かてい 変化 へんか 無視 むし
ルイスは彼 かれ 取 と 扱 あつか 以下 いか 式 しき 適用 てきよう 実験 じっけん 値 ち 一致 いっち 得 え
2HI → H2 + I2 しかしながら、その後 ご 同 おな 取 と 扱 あつか 他 た 反応 はんのう 適用 てきよう 理論 りろん 的 てき 結果 けっか 実験 じっけん 結果 けっか 間 あいだ 大 おお 相違 そうい
統計 とうけい 力学 りきがく 構築 こうちく 大 おお 役割 やくわり 果 は 世紀 せいき 中頃 なかごろ ジェームズ・クラーク・マクスウェル 、ルートヴィッヒ・ボルツマン 、レオポルト・プファウントラー (英語 えいご 版 ばん 分子 ぶんし 運動 うんどう 分子 ぶんし 速度 そくど 統計 とうけい 学 がく 的 てき 分布 ぶんぷ 観点 かんてん 反応 はんのう 平衡 へいこう 速度 そくど 議論 ぎろん 複数 ふくすう 論文 ろんぶん 出版 しゅっぱん 事実 じじつ 鑑 かんが 統計 とうけい 力学 りきがく 応用 おうよう 非常 ひじょう 進展 しんてん
フランスの化学 かがく 者 しゃ マクスウェル=ボルツマン分布 ぶんぷ を使 つか 反応 はんのう 速度 そくど 関 かん 式 しき
d
ln
k
d
T
=
a
−
b
T
R
T
2
{\displaystyle {\frac {d\ln k}{dT}}={\frac {a-bT}{RT^{2}}}}
(a およびb はエネルギー項 こう 関連 かんれん 定数 ていすう 得 え 年 ねん
その2年 ねん 後 ご 化学 かがく 反応 はんのう 進行 しんこう 位相 いそう 空間 くうかん 点 てん 運動 うんどう 取 と 扱 あつか 本質 ほんしつ 的 てき 貢献 こうけん 行 おこな 次 つぎ 統計 とうけい 力学 りきがく 的 てき 手順 てじゅん 適用 てきよう 以前 いぜん 熱 ねつ 力学 りきがく 的 てき 考察 こうさつ 自身 じしん 得 え 似 に 式 しき 得 え
1915年 ねん 物理 ぶつり 学者 がくしゃ 重要 じゅうよう 貢献 こうけん 行 おこな 自身 じしん 統計 とうけい 解析 かいせき 基 もと 反応 はんのう 速度 そくど 臨界 りんかい 増量 ぞうりょう 比例 ひれい 結論 けつろん 付 つ 彼 かれ 着想 ちゃくそう リチャード・チェイス・トールマン によってさらに発展 はってん 年 ねん 物理 ぶつり 学者 がくしゃ カール・フェルディナント・ヘルツフェルト (英語 えいご 版 ばん 統計 とうけい 力学 りきがく 平衡 へいこう 定数 ていすう 運動 うんどう 理論 りろん 二 に 原子 げんし 分子 ぶんし 可逆 かぎゃく 的 てき 解離 かいり 逆 ぎゃく 反応 はんのう 速度 そくど 定数 ていすう k −1 に適用 てきよう [7]
AB
⇌
k
−
1
k
1
A
+
B
{\displaystyle {\ce {AB <=>[k_1][k_{-1}] {A}+ {B}}}}
ヘルツフェルトは順 じゅん 反応 はんのう 速度 そくど 定数 ていすう 対 たい 以下 いか 式 しき 得 え [8]
k
1
=
k
B
T
h
(
1
−
e
−
h
ν にゅー
k
B
T
)
exp
(
−
E
⊖
R
T
)
{\displaystyle k_{1}={\frac {k_{\mathrm {B} }T}{h}}\left(1-e^{-{\frac {h\nu }{k_{B}T}}}\right)\exp \left({\frac {-E^{\ominus }}{RT}}\right)}
上 うえ 式 しき
E
⊖
{\displaystyle \textstyle E^{\ominus }}
絶対 ぜったい 零 れい 度 ど 解離 かいり k B はボルツマン定数 ていすう 、h はプランク定数 ていすう 、T は熱 ねつ 力学 りきがく 的 てき 温度 おんど
ν にゅー
{\displaystyle \nu }
結合 けつごう 振動 しんどう 周波数 しゅうはすう 式 しき 重要 じゅうよう 要素 ようそ 因子 いんし k B T /h が速度 そくど 方程式 ほうていしき 初 はじ 登場 とうじょう 非常 ひじょう 重要 じゅうよう
1920年 ねん 化学 かがく 者 しゃ 着想 ちゃくそう 発展 はってん 反応 はんのう 現在 げんざい 活性 かっせい 化 か 呼 よ 反応 はんのう 起 お 全 ぜん 分子 ぶんし 平均 へいきん 全 すべ 反応 はんのう 物 ぶつ 分子 ぶんし 平均 へいきん 引 ひ 等 ひと 結論 けつろん 付 つ
ポテンシャルエネルギー面 めん 概念 がいねん 発展 はってん 非常 ひじょう 重要 じゅうよう 概念 がいねん 基礎 きそ 年 ねん 築 きず 化学 かがく 反応 はんのう 進行 しんこう 原子 げんし 運動 うんどう 量 りょう 距離 きょり 座標 ざひょう 持 も 面 めん 点 てん 記述 きじゅつ 理論 りろん 化 か
1931年 ねん ヘンリー・アイリング とマイケル・ポランニー は以下 いか 反応 はんのう 対 たい 面 めん 構築 こうちく 面 めん 量子力学 りょうしりきがく 的 てき 諸 しょ 原理 げんり 振動 しんどう 周波数 しゅうはすう 解離 かいり 実験 じっけん 基 もと 次元 じげん 図 ず
H + H2 → H2 + H アイリングとポランニーの構築 こうちく 年 ねん 後 ご ユージン・ウィグナー はポテンシャルエネルギー面 めん 上 じょう 反応 はんのう 進行 しんこう 重要 じゅうよう 貢献 こうけん 行 おこな 成果 せいか 重要 じゅうよう 性 せい 初 はじ 面 めん 鞍点 あんてん 鞍部 あんぶ (英語 えいご 版 ばん 概念 がいねん 議論 ぎろん 彼 かれ 反応 はんのう 速度 そくど 鞍部 あんぶ 経 へ 系 けい 運動 うんどう 決定 けってい 結論 けつろん 付 つ
典型 てんけい 的 てき 律 りつ 速 そく 点 てん 最低 さいてい 鞍点 あんてん 初期 しょき 基底 きてい 状態 じょうたい 同 おな 面 めん 上 じょう 位置 いち 仮定 かてい 最近 さいきん 半導体 はんどうたい 絶縁 ぜつえん 体 たい 中 ちゅう 起 お 過程 かてい 誤 あやま 明 あき 材料 ざいりょう 中 ちゅう 初期 しょき 励起 れいき 状態 じょうたい 初期 しょき 基底 きてい 状態 じょうたい 面 めん 上 じょう 鞍点 あんてん 低 ひく 鞍点 あんてん 通過 つうか [9]
アイリング 、ポランニー 、およびエヴァンス によって導入 どうにゅう 最 もっと 重要 じゅうよう 要素 ようそ 活性 かっせい 複 ふく 合体 がったい 反応 はんのう 物 ぶつ 擬 なずらえ 平衡 へいこう 状態 じょうたい 考 かんが 方 かた 結果 けっか 反応 はんのう 速度 そくど 複 ふく 合体 がったい 濃度 のうど 複 ふく 合体 がったい 生成 せいせい 物 ぶつ 変換 へんかん 周波数 しゅうはすう k B T /h )を乗 じょう 正 せい 比例 ひれい 下部 かぶ 式 しき 関数 かんすう 形式 けいしき 厳密 げんみつ 妥当 だとう 性 せい 主張 しゅちょう 示 しめ 鍵 かぎ 統計 とうけい 力学 りきがく 的 てき 因子 いんし k B T /h は正当 せいとう 化 か 下 した 示 しめ 論拠 ろんきょ 式 しき 真 しん 導出 どうしゅつ 構成 こうせい [10]
擬 なずらえ 平衡 へいこう 古典 こてん 的 てき 化学 かがく 平衡 へいこう 異 こと 類似 るいじ 熱 ねつ 力学 りきがく 的 てき 取扱 とりあつか 使 つか 記述 きじゅつ [5] [11] 以下 いか 反応 はんのう 考 かんが
A
+
B
↽
−
−
⇀
[
AB
]
‡
⟶
P
{\displaystyle {\ce {{A}+{B}<=>{[AB]^{\ddagger }}->{P}}}}
図 ず 図 ず ここでは、活性 かっせい 複 ふく 合体 がったい ‡ を含 ふく 系 けい 中 ちゅう 全 すべ 化学 かがく 種 しゅ 間 あいだ 完全 かんぜん 平衡 へいこう 達成 たっせい 統計 とうけい 力学 りきがく 使 つか ‡ の濃度 のうど 濃度 のうど 観点 かんてん 計算 けいさん
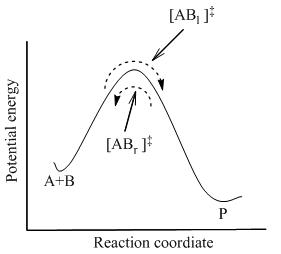
TSTは、反応 はんのう 物 ぶつ 生成 せいせい 物 ぶつ 互 たが 平衡 へいこう 状態 じょうたい 時 とき 活性 かっせい 複 ふく 合体 がったい 反応 はんのう 物 ぶつ 擬 なずらえ 平衡 へいこう 状態 じょうたい 仮定 かてい 図 ず 示 しめ 瞬間 しゅんかん 少数 しょうすう 活性 かっせい 複 ふく 合体 がったい 存在 そんざい 一部 いちぶ 直近 ちょっきん 過去 かこ 反応 はんのう 物 ぶつ l ‡ と呼 よ 左 ひだり 右 みぎ 移動 いどう 残 のこ 直近 ちょっきん 過去 かこ 生成 せいせい 物 ぶつ 分子 ぶんし r ‡ )。
TSTでは、活性 かっせい 複 ふく 合体 がったい 方向 ほうこう 流 なが 互 たが 独立 どくりつ 仮定 かてい 全 すべ 生成 せいせい 物 ぶつ 分子 ぶんし 反応 はんのう 系 けい 突然 とつぜん 取 と 除 のぞ r ‡ の流 なが 止 と 左 ひだり 右 みぎ 流 なが 存在 そんざい 技術 ぎじゅつ 的 てき 正 ただ 言 い 反応 はんのう 物 ぶつ l ‡ (直近 ちょっきん 過去 かこ 反応 はんのう 物 ぶつ 活性 かっせい 複 ふく 合体 がったい 平衡 へいこう 状態 じょうたい
活性 かっせい 複 ふく 合体 がったい 分布 ぶんぷ 従 したが 平衡 へいこう 定数 ていすう 活性 かっせい 複 ふく 合体 がったい 従 したが 分布 ぶんぷ 導出 どうしゅつ 擬 なずらえ 平衡 へいこう 平衡 へいこう 定数 ていすう K ‡ は
K
‡
=
[
AB
]
‡
[
A
]
[
B
]
{\displaystyle K^{\ddagger }={\frac {\ce {[AB]^{\ddagger }}}{\ce {[A][B]}}}}
と書 か
そのため、遷移 せんい 状態 じょうたい ‡ の濃度 のうど
[
AB
]
‡
=
K
‡
[
A
]
[
B
]
{\displaystyle [{\ce {AB}}]^{\ddagger }=K^{\ddagger }[{\ce {A}}][{\ce {B}}]}
である。
したがって、生成 せいせい 物 ぶつ 生成 せいせい 速度 そくど 式 しき
d
[
P
]
d
t
=
k
‡
[
AB
]
‡
=
k
‡
K
‡
[
A
]
[
B
]
=
k
[
A
]
[
B
]
{\displaystyle {\frac {d[{\ce {P}}]}{dt}}=k^{\ddagger }[{\ce {AB}}]^{\ddagger }=k^{\ddagger }K^{\ddagger }[{\ce {A}}][{\ce {B}}]=k[{\ce {A}}][{\ce {B}}]}
となる。上 うえ 式 しき 速度 そくど 定数 ていすう k は
k
=
k
‡
K
‡
{\displaystyle k=k^{\ddagger }K^{\ddagger }}
で与 あた
ここで、k ‡ は活性 かっせい 複 ふく 合体 がったい 生成 せいせい 物 ぶつ 変化 へんか 必要 ひつよう 振動 しんどう 周波数 しゅうはすう 正 せい 比例 ひれい 振動 しんどう 周波数 しゅうはすう
ν にゅー
{\displaystyle \nu }
全 すべ 振動 しんどう 必 かなら 生成 せいせい 物 ぶつ 形成 けいせい 透過 とうか 係数 けいすう 呼 よ 比例 ひれい 定数 ていすう
κ かっぱ
{\displaystyle \kappa }
効果 こうか 説明 せつめい 導入 どうにゅう k ‡ は
k
‡
=
κ かっぱ ν にゅー
{\displaystyle k^{\ddagger }=\kappa \nu }
と書 か
平衡 へいこう 定数 ていすう K ‡ について、統計 とうけい 力学 りきがく 以下 いか 温度 おんど 依存 いぞん 式 しき
K
‡
=
k
B
T
h
ν にゅー
K
‡
′
{\displaystyle K^{\ddagger }={\frac {k_{B}T}{h\nu }}K^{\ddagger '}}
K
‡
′
=:
e
−
Δ でるた
G
‡
R
T
{\displaystyle K^{\ddagger '}=:e^{\frac {-\Delta G^{\ddagger }}{RT}}}
k ‡ とK ‡ についての新 あたら 式 しき 組 く 合 あ 新 あたら 速度 そくど 定数 ていすう 式 しき
k
=
k
‡
K
‡
=
κ かっぱ
k
B
T
h
e
−
Δ でるた
G
‡
R
T
=
κ かっぱ
k
B
T
h
K
‡
′
{\displaystyle k=k^{\ddagger }K^{\ddagger }=\kappa {\frac {k_{B}T}{h}}e^{\frac {-\Delta G^{\ddagger }}{RT}}=\kappa {\frac {k_{B}T}{h}}K^{\ddagger '}}
と書 か
定義 ていぎ Δ でるた G ‡ = Δ でるた H ‡ –T Δ でるた S ‡ であるため、この速度 そくど 定数 ていすう 式 しき 以下 いか 展開 てんかい 式 しき 別 べつ 形式 けいしき 与 あた
k
=
κ かっぱ
k
B
T
h
e
Δ でるた
S
‡
R
e
−
Δ でるた
H
‡
R
T
{\displaystyle k=\kappa {\frac {k_{B}T}{h}}e^{\frac {\Delta S^{\ddagger }}{R}}e^{\frac {-\Delta H^{\ddagger }}{RT}}}
正 ただ 次元 じげん 性 せい 式 しき 単 たん 分子 ぶんし 的 てき 反応 はんのう 追加 ついか 因子 いんし c ⊖ )1–m を持 も 必要 ひつよう
k
=
κ かっぱ
k
B
T
h
e
Δ でるた
S
‡
R
e
−
Δ でるた
H
‡
R
T
(
c
⊖
)
1
−
m
{\displaystyle k=\kappa {\frac {k_{B}T}{h}}e^{\frac {\Delta S^{\ddagger }}{R}}e^{\frac {-\Delta H^{\ddagger }}{RT}}(c^{\ominus })^{1-m}}
上 うえ 式 しき c ⊖ は標準 ひょうじゅん 濃度 のうど –1 、m は分子 ぶんし 度 ど [12]
遷移 せんい 状態 じょうたい 理論 りろん 推論 すいろん 理論 りろん 関係 かんけい [ 編集 へんしゅう ] 遷移 せんい 状態 じょうたい 理論 りろん 得 え 速度 そくど 定数 ていすう 式 しき 実験 じっけん 的 てき 反応 はんのう 速度 そくど 使 つか Δ でるた G ‡ 、Δ でるた H ‡ 、Δ でるた S ‡ 、そしてΔ でるた V ‡ (活性 かっせい 化 か 体積 たいせき 計算 けいさん 使 つか 活性 かっせい 化 か 容量 ようりょう 秩序 ちつじょ 度 ど 出発 しゅっぱつ 物質 ぶっしつ 比較 ひかく 遷移 せんい 状態 じょうたい 特性 とくせい 洞察 どうさつ 与 あた 物理 ぶつり 有機 ゆうき 化学 かがく 反応 はんのう 機構 きこう 解明 かいめい 標準 ひょうじゅん 的 てき 活性 かっせい 化 か 自由 じゆう Δ でるた G ‡ は遷移 せんい 状態 じょうたい 理論 りろん
Δ でるた
G
‡
=
−
R
T
ln
K
‡
′
{\displaystyle \Delta G^{\ddagger }=-RT\ln K^{\ddagger '}}
満 み 定義 ていぎ Δ でるた H ‡ およびΔ でるた S ‡ は次 つぎ 異 こと 温度 おんど Δ でるた G ‡ = Δ でるた H ‡ – T Δ でるた S ‡ を決定 けってい 推定 すいてい
アイリングの式 しき 式 しき 関数 かんすう 形式 けいしき 似 に 活性 かっせい 化 か 表現 ひょうげん 方法 ほうほう 活性 かっせい 化 か 前 ぜん 指数 しすう 因子 いんし 関連付 かんれんづ 式 しき 実験 じっけん 導 みちび 反応 はんのう 機構 きこう 遷移 せんい 状態 じょうたい 数 かず 関係 かんけい 使 つか 巨視的 きょしてき 速度 そくど 化 か 対照 たいしょう 的 てき 活性 かっせい 化 か 少 すく 原理 げんり 的 てき 多 た 段階 だんかい 機構 きこう 全 すべ 遷移 せんい 状態 じょうたい 見出 みいだ 活性 かっせい 化 か Δ でるた H ‡ はしばしばアレニウスの活性 かっせい 化 か E a と同一 どういつ 視 し 等価 とうか 凝縮 ぎょうしゅく 相 しょう 例 たと 溶液 ようえき 相 しょう 単 たん 分子 ぶんし 的 てき 気 き 相反 あいはん 応 おう 段階 だんかい E a = Δ でるた H ‡ + RT である。他 た 気 き 相反 あいはん 応 おう E a = Δ でるた H ‡ + (1 − Δ でるた n ‡ )RT である。(Δ でるた n ‡ は遷移 せんい 状態 じょうたい 形成 けいせい 際 さい 分子 ぶんし 数 すう 変化 へんか [13] 二 に 分子 ぶんし 気 き 相 しょう 過程 かてい E a = Δ でるた H ‡ + 2RT となる。
活性 かっせい 化 か Δ でるた S ‡ は、(反応 はんのう 関与 かんよ 反応 はんのう 摂動 せつどう 受 う 溶媒 ようばい 分子 ぶんし 含 ふく 遷移 せんい 状態 じょうたい 出発 しゅっぱつ 物質 ぶっしつ 比較 ひかく 無秩序 むちつじょ 程度 ていど 与 あた 式 しき 前 ぜん 指数 しすう 因子 いんし A の具体 ぐたい 的 てき 解釈 かいしゃく 与 あた 単 たん 分子 ぶんし 的 てき 一 いち 段階 だんかい 過程 かてい 大 おお 等価 とうか 性 せい A = (k B T /h ) exp(1 + Δ でるた S ‡ /R ) が成 な 立 た 二 に 分子 ぶんし 的 てき 気 き 相反 あいはん 応 おう A = (k B T /h ) exp(2 + Δ でるた S ‡ /R ))。単 たん 分子 ぶんし 過程 かてい 負 まけ 値 ね 基底 きてい 状態 じょうたい 秩序 ちつじょ 硬 かた 遷移 せんい 状態 じょうたい 示 しめ 対 たい 正 せい 値 ね 遷移 せんい 状態 じょうたい 緩 ゆる 結合 けつごう 大 おお 配 はい 座 ざ 的 てき 自由 じゆう 度 ど 両方 りょうほう 一方 いっぽう 持 も 反映 はんえい 次元 じげん 性 せい 理由 りゆう 二 に 分子 ぶんし 的 てき 以上 いじょう 反応 はんのう 選択 せんたく 標準 ひょうじゅん 状態 じょうたい 具体 ぐたい 的 てき 言 い 標準 ひょうじゅん 濃度 のうど 依存 いぞん Δ でるた S ‡ 値 ね 持 も 注意 ちゅうい 重要 じゅうよう 近年 きんねん 文献 ぶんけん –1 (1モーラー)が選 えら 選択 せんたく 量 りょう 体積 たいせき 単位 たんい 我々 われわれ 定義 ていぎ 基 もと 人間 にんげん 産物 さんぶつ 単一 たんいつ 反応 はんのう Δ でるた S ‡ の大 おお 符号 ふごう 自体 じたい 無意味 むいみ 同 おな 標準 ひょうじゅん 状態 じょうたい 決定 けってい 既知 きち 想定 そうてい 機構 きこう 参照 さんしょう 反応 はんのう 値 ね 比較 ひかく 妥当 だとう [14]
活性 かっせい 化 か 体積 たいせき 温度 おんど 一定 いってい 圧力 あつりょく 関 かん Δ でるた G ‡ の偏 へん 微分 びぶん 議論 ぎろん 見出 みいだ
Δ でるた
V
‡
:=
(
∂
Δ でるた
G
‡
/
∂
P
)
T
{\displaystyle \Delta V^{\ddagger }:=(\partial \Delta G^{\ddagger }/\partial P)_{T}}
これは、遷移 せんい 状態 じょうたい 大 おお 結合 けつごう 度合 どあ 関 かん 情報 じょうほう 与 あた 結合 けつごう 的 てき 機構 きこう 負 まけ 活性 かっせい 化 か 体積 たいせき 持 も 対 たい 解離 かいり 的 てき 機構 きこう 正 せい 値 ね 持 も
平衡 へいこう 定数 ていすう 順 じゅん 逆 ぎゃく 速度 そくど 定数 ていすう 間 あいだ 関係 かんけい
K
=
k
1
/
k
−
1
{\displaystyle K=k_{1}/k_{-1}}
考 かんが 式 しき
Δ でるた
G
∘
=
Δ でるた
G
1
‡
−
Δ でるた
G
−
1
‡
{\displaystyle \Delta G^{\circ }=\Delta G_{1}^{\ddagger }-\Delta G_{-1}^{\ddagger }}
ということになる。
TSTのもう1つの暗示 あんじ カーティン–ハメットの原理 げんり (英語 えいご 版 ばん 生成 せいせい 物 ぶつ 得 え 速度 そくど 論 ろん 的 てき 支配 しはい 制御 せいぎょ 反応 はんのう (英語 えいご 版 ばん 生成 せいせい 物 ぶつ 比 ひ 生成 せいせい 物 ぶつ 各 かく 遷移 せんい 状態 じょうたい 差 さ 反映 はんえい 生成 せいせい 物 ぶつ 単一 たんいつ 遷移 せんい 状態 じょうたい 仮定 かてい
[
A
]
[
B
]
=
e
−
Δ でるた Δ でるた
G
‡
/
R
T
{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=e^{-\Delta \Delta G^{\ddagger }/RT}}
(
Δ でるた Δ でるた
G
‡
=
Δ でるた
G
A
‡
−
Δ でるた
G
B
‡
{\displaystyle \Delta \Delta G^{\ddagger }=\Delta G_{\mathrm {A} }^{\ddagger }-\Delta G_{\mathrm {B} }^{\ddagger }}
(上記 じょうき Δ でるた Δ でるた G ‡ についての式 しき 平衡 へいこう 状態 じょうたい 異 こと 化学 かがく 種 しゅ A およびSB から形成 けいせい 追加 ついか
Δ でるた
G
∘
=
G
S
A
∘
−
G
S
B
∘
{\displaystyle \Delta G^{\circ }=G_{\mathrm {S} _{\mathrm {A} }}^{\circ }-G_{\mathrm {S} _{\mathrm {B} }}^{\circ }}
項 こう 存在 そんざい
1.36ルール
熱 ねつ 力学 りきがく 的 てき 支配 しはい 反応 はんのう 生成 せいせい 物 ぶつ 自由 じゆう RT ln 10 ≈ (1.987 × 10–3 kcal/mol K)(298 K)(2.303) ≈ 1.36 kcal/mol の差 さ 毎 ごと 室温 しつおん 298 K )での選択 せんたく 性 せい 倍 ばい
[
A
]
[
B
]
=
10
−
Δ でるた
G
∘
/
(
1.36
k
c
a
l
/
m
o
l
)
{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=10^{-\Delta G^{\circ }/(1.36\ \mathrm {kcal/mol} )}}
(
Δ でるた
G
∘
=
G
A
∘
−
G
B
∘
{\displaystyle \Delta G^{\circ }=G_{\mathrm {A} }^{\circ }-G_{\mathrm {B} }^{\circ }}
類似 るいじ 的 てき 活性 かっせい 化 か 自由 じゆう 差 さ 毎 ごと 室温 しつおん 速度 そくど 論 ろん 支配 しはい 過程 かてい 選択 せんたく 性 せい (英語 えいご 版 ばん 倍 ばい [15]
[
A
]
[
B
]
=
10
−
Δ でるた Δ でるた
G
‡
/
(
1.36
k
c
a
l
/
m
o
l
)
{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=10^{-\Delta \Delta G^{\ddagger }/(1.36\ \mathrm {kcal/mol} )}}
(
Δ でるた Δ でるた
G
‡
=
Δ でるた
G
A
‡
−
Δ でるた
G
B
‡
{\displaystyle \Delta \Delta G^{\ddagger }=\Delta G_{\mathrm {A} }^{\ddagger }-\Delta G_{\mathrm {B} }^{\ddagger }}
概算 がいさん アイリングの式 しき 使 つか 特定 とくてい 温度 おんど Δ でるた G ‡ 、一 いち 次 じ 速度 そくど 定数 ていすう 反応 はんのう 半減 はんげん 期 き 間 あいだ 直接的 ちょくせつてき 関係 かんけい 存在 そんざい 298 K では、Δ でるた G ‡ = 23 kcal/mol反応 はんのう k ≈ 8.4 × 10–5 s–1 の速度 そくど 定数 ていすう t 1/2 ≈ 2.3時 じ 間 あいだ 半減 はんげん 期 き 持 も 数字 すうじ k ~ 10–4 s–1 t 1/2 ~ 2 h丸 まる 大 おお 活性 かっせい 化 か 自由 じゆう 室温 しつおん 一 いち 晩 ばん 終了 しゅうりょう 進行 しんこう 典型 てんけい 的 てき 反応 はんのう 対応 たいおう 比較 ひかく シクロヘキサン のいす反転 はんてん (英語 えいご 版 ばん Δ でるた G ‡ とk ~ 105 s–1 の速度 そくど 定数 ていすう 有 ゆう 室温 しつおん 時間 じかん 速 はや 迅速 じんそく 起 お 動的 どうてき 過程 かてい 反対 はんたい 側 がわ 異性 いせい 化 か Δ でるた G ‡ を持 も k ~ 10–31 s–1 に相当 そうとう 無視 むし 速度 そくど 半減 はんげん 期 き 桁 けた 宇宙 うちゅう 年齢 ねんれい 長 なが [16] 一般 いっぱん 研究 けんきゅう 者 しゃ 化学 かがく 反応 はんのう 起 お 理解 りかい 概念的 がいねんてき 基盤 きばん 与 あた 本 ほん 理論 りろん 広 ひろ 適用 てきよう 限界 げんかい 例 たと 多 た 段階 だんかい 反応 はんのう 個々 ここ 素 す 過程 かてい 適用 てきよう 時 とき 本 ほん 理論 りろん 個々 ここ 中 なか 間 あいだ 体 たい 次 つぎ 段階 だんかい 進 すす 前 まえ 分布 ぶんぷ 達 たっ 十分 じゅうぶん 長寿 ちょうじゅ 命 いのち 仮定 かてい 中間 なかま 体 たい 非常 ひじょう 短 たん 寿命 じゅみょう 時 とき 破綻 はたん 場合 ばあい 反応 はんのう 物 ぶつ 中間 なかま 体 たい 反応 はんのう 軌跡 きせき 運動 うんどう 量 りょう 生成 せいせい 物 ぶつ 選択 せんたく 性 せい 影響 えいきょう 及 およ 可能 かのう 性 せい 反応 はんのう 一 いち 例 れい ドウアティ (英語 えいご 版 ばん 教科書 きょうかしょ 示 しめ 類 るい 熱 ねつ 分解 ぶんかい
遷移 せんい 状態 じょうたい 理論 りろん 原子核 げんしかく 古典 こてん 力学 りきがく 従 したが 振 ふ 舞 ま 仮定 かてい 基 もと [17] 原子 げんし 分子 ぶんし 遷移 せんい 構造 こうぞう 形成 けいせい 十分 じゅうぶん 持 も 衝突 しょうとつ 限 かぎ 反応 はんのう 起 お 仮定 かてい 量子力学 りょうしりきがく 有限 ゆうげん 量 りょう 持 も 障壁 しょうへき 粒子 りゅうし 障壁 しょうへき 向 む 側 がわ 可能 かのう 性 せい 存在 そんざい トンネル効果 こうか )。化学 かがく 反応 はんのう 関 かん 分子 ぶんし 障壁 しょうへき 越 こ 十分 じゅうぶん 持 も 衝突 しょうとつ 反応 はんのう 可能 かのう 性 せい 存在 そんざい 意味 いみ [18] 効果 こうか 大 おお 活性 かっせい 化 か 持 も 反応 はんのう 無視 むし 確 かく 率 りつ 障壁 しょうへき 高 たか 低 ひく 大 おお 比較的 ひかくてき 低 てい 障壁 しょうへき 持 も 反応 はんのう 重要 じゅうよう 現象 げんしょう
遷移 せんい 状態 じょうたい 理論 りろん 高温 こうおん 一部 いちぶ 反応 はんのう 破綻 はたん 本 ほん 理論 りろん 反応 はんのう 系 けい 面 めん 最低 さいてい 鞍点 あんてん 通過 つうか 仮定 かてい 描写 びょうしゃ 比較的 ひかくてき 低温 ていおん 起 お 反応 はんのう 合 あ 高温 こうおん 分子 ぶんし 高 たか 振動 しんどう 占有 せんゆう 運動 うんどう 複雑 ふくざつ 衝突 しょうとつ 結果 けっか 最低 さいてい 鞍点 あんてん 遠 とお 離 はな 遷移 せんい 状態 じょうたい 遷移 せんい 状態 じょうたい 理論 りろん 二 に 原子 げんし 水素 すいそ 水素 すいそ 間 あいだ 単純 たんじゅん 交換 こうかん 反応 はんのう 観測 かんそく [19]
これらの限界 げんかい 考慮 こうりょ 複数 ふくすう 遷移 せんい 状態 じょうたい 理論 りろん 代替 だいたい 理論 りろん 提唱 ていしょう 理論 りろん 簡潔 かんけつ 解説 かいせつ 以下 いか 示 しめ
小正 おばさ 準 じゅん 変 へん 分 ぶん 型 がた 正 せい 準 じゅん 変 へん 分 ぶん 型 がた (英語 えいご 版 ばん 改良 かいりょう 正 ただし 準 じゅん 変 へん 分 ぶん 型 がた 遷移 せんい 状態 じょうたい 必 かなら 鞍点 あんてん 位置 いち 一般 いっぱん 化 か 遷移 せんい 状態 じょうたい 理論 りろん 呼 よ
遷移 せんい 状態 じょうたい 理論 りろん 根本 こんぽん 的 てき 欠陥 けっかん 反応 はんのう 物 ぶつ 生成 せいせい 物 ぶつ 逆 ぎゃく 反 はん 応 おう 遷移 せんい 状態 じょうたい 全 すべ 交差 こうさ 数 かぞ 現実 げんじつ 分子 ぶんし 分割 ぶんかつ 面 めん 越 こ 引 ひ 換 か 複 ふく 数 すう 回 かい 越 こ 本当 ほんとう 一 いち 度 ど 反応 はんのう 未 み 補正 ほせい 速度 そくど 係数 けいすう 上 うえ 界 かい 与 あた 言 い 補正 ほせい 変 へん 分 ぶん 型 がた 遷移 せんい 状態 じょうたい 理論 りろん 固定 こてい 反応 はんのう 速度 そくど 最小 さいしょう 化 か 反応 はんのう 定義 ていぎ 分割 ぶんかつ 面 めん 位置 いち 変動 へんどう [20] 小正 おばさ 準 じゅん 的 てき 取 と 扱 あつか 得 え 速度 そくど 式 しき 積分 せきぶん 正 せい 準 じゅん 熱 ねつ 的 てき 速度 そくど 与 あた 状態 じょうたい 統計 とうけい 学 がく 的 てき 分布 ぶんぷ 考慮 こうりょ 入 い
特定 とくてい 温度 おんど 速度 そくど 定数 ていすう 最小 さいしょう 化 か 分割 ぶんかつ 面 めん 位置 いち 変動 へんどう 遷移 せんい 状態 じょうたい 理論 りろん 発展 はってん
改良 かいりょう 正 ただし 準 じゅん 変 へん 分 ぶん 型 がた [ 編集 へんしゅう ] 正 せい 準 じゅん 変 へん 分 ぶん 型 がた 遷移 せんい 状態 じょうたい 理論 りろん 修正 しゅうせい 下 した 分割 ぶんかつ 面 めん 位置 いち 小正 おばさ 準 じゅん 未満 みまん 速度 そくど 定数 ていすう 寄与 きよ 次 つぎ 高 たか 持 も 反応 はんのう 物 ぶつ 成 な 速度 そくど 定数 ていすう 寄与 きよ 最小 さいしょう 化 か 妥協 だきょう 分割 ぶんかつ 面 めん 選択 せんたく
2つのスピン状態 じょうたい 同時 どうじ 関与 かんよ 反応 はんのう 拡張 かくちょう 非 ひ 断熱 だんねつ 遷移 せんい 状態 じょうたい 理論 りろん (英語 えいご 版 ばん 呼 よ
振動 しんどう 摂動 せつどう 理論 りろん 使 つか 変 へん 分 ぶん 効果 こうか 効果 こうか 半 はん 古典 こてん 的 てき 遷移 せんい 状態 じょうたい 理論 りろん (英語 えいご 版 ばん 形式 けいしき 内 ない 説明 せつめい
^ IUPAC , Compendium of Chemical Terminology , 2nd ed. (the "Gold Book") (1997). オンライン版 ばん transition state theory ".^ Truhlar, D. G. ; Garrett, B. C.; Klippenstein, S. J. (1996). “Current Status of Transition-State Theory”. J. Phys. Chem. 100 (31): 12771–12800. doi :10.1021/jp953748q . ^ Laidler, K.; King, C. (1983). “Development of transition-state theory”. J. Phys. Chem. 87 (15): 2657. doi :10.1021/j100238a002 . ^ Laidler, K.; King, C. (1998). “A lifetime of transition-state theory”. The Chemical Intelligencer 4 (3): 39. ^ a b Laidler, K. J. (1969). Theories of Chemical Reaction Rates . McGraw-Hill
^ Anslyn, E. V.; Dougherty, D. A. (2006). “Transition State Theory and Related Topics”. Modern Physical Organic Chemistry . University Science Books. pp. 365–373. ISBN 1891389319 ^ Herzfeld, K. E. (1919). “Zur Theorie der Reaktionsgeschwindigkeiten in Gasen” . Annalen der Physik 364 (15): 635–667. Bibcode : 1919AnP...364..635H . doi :10.1002/andp.19193641504 . https://zenodo.org/record/1424347 . ^ Keith J. Laidler, Chemical Kinetics (3rd ed., Harper & Row 1987), p.88 ISBN 0-06-043862-2
^ Luo, G.; Kuech, T. F.; Morgan, D. (2018). “Transition state redox during dynamical processes in semiconductors and insulators”. NPG Asia Materials 10 (4): 45–51. arXiv :1712.01686 . Bibcode : 2018npjAM..10...45L . doi :10.1038/s41427-018-0010-0 . ^ 統計 とうけい 力学 りきがく 入門 にゅうもん 的 てき 取扱 とりあつか 式 しき 初歩 しょほ 的 てき 導出 どうしゅつ 以下 いか 文献 ぶんけん 見 み Mechanism and Theory in Organic Chemistry , 3rd ed. (Harper & Row, 1987), pp. 248-253.^ Steinfeld, Jeffrey L.; Francisco, Joseph S.; Hase, William L. (1999). Chemical Kinetics and Dynamics (2nd ed.). Prentice-Hall. pp. 289-293. ISBN 0-13-737123-3 ^ Laidler, Keith J. (1981). “Symbolism and terminology in chemical kinetics” . Pure and Applied Chemistry (IUPAC) 53 : 753-771. http://publications.iupac.org/pac/pdf/1981/pdf/5303x0753.pdf 2019年 ねん 月 がつ 日 にち 閲覧 えつらん ^ Steinfeld, Jeffrey L.; Francisco, Joseph S.; Hase, William L. (1999). Chemical Kinetics and Dynamics (2nd ed.). Prentice-Hall. p. 302. ISBN 0-13-737123-3 ^ Carpenter, Barry K. (1984). Determination of organic reaction mechanisms . New York: Wiley. ISBN 0471893692 . OCLC 9894996 ^ Lowry, Thomas H. (1987). Mechanism and theory in organic chemistry ISBN 0060440848 . OCLC 14214254 . https://archive.org/details/mechanismtheoryi000321 ^ Eliel, Ernest L. (Ernest Ludwig) (1994). Stereochemistry of organic compounds . Wilen, Samuel H., Mander, Lewis N.. New York: Wiley. ISBN 0471016705 . OCLC 27642721 ^ Eyring, H. (1935). “The Activated Complex in Chemical Reactions”. J. Chem. Phys. 3 (2): 107–115. Bibcode : 1935JChPh...3..107E . doi :10.1063/1.1749604 . ^ Masel, R. (1996). Principles of Adsorption and Reactions on Solid Surfaces . New York: Wiley ^ Pineda, J. R.; Schwartz, S. D. (2006). “Protein dynamics and catalysis: The problems of transition state theory and the subtlety of dynamic control” . Phil. Trans. R. Soc. B 361 (1472): 1433–1438. doi :10.1098/rstb.2006.1877 . PMC 1647311 . PMID 16873129 . https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1647311/ . ^ Truhlar, D.; Garrett, B. (1984). “Variational Transition State Theory” . Annu. Rev. Phys. Chem. 35 : 159–189. Bibcode : 1984ARPC...35..159T . doi :10.1146/annurev.pc.35.100184.001111 . https://digital.library.unt.edu/ark:/67531/metadc1209228/ .
Anslyn, Eric V.; Doughtery, Dennis A., Transition State Theory and Related Topics. In Modern Physical Organic Chemistry University Science Books: 2006; pp 365–373
Cleland, W.W., Isotope Effects: Determination of Enzyme Transition State Structure. Methods in Enzymology 1995, 249, 341-373
Laidler, K.; King, C., Development of transition-state theory. The Journal of Physical Chemistry 1983, 87, (15), 2657
Laidler, K., A lifetime of transition-state theory. The Chemical Intelligencer 1998, 4, (3), 39
Radzicka, A.; Woldenden, R., Transition State and Multisubstrate$Analog Inhibitors. Methods in Enzymology 1995, 249, 284-312
Schramm, VL., Enzymatic Transition States and Transition State Analog Design. Annual Review of Biochemistry 1998, 67, 693-720
Schramm, V.L., Enzymatic Transition State Theory and Transition State Analogue Design. Journal of Biological Chemistry 2007, 282, (39), 28297-28300 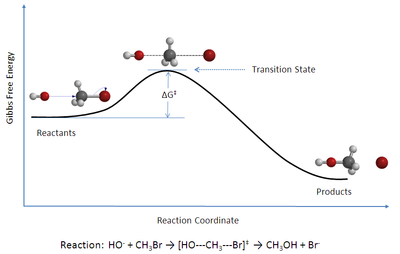








![{\displaystyle {\ce {AB <=>[k_1][k_{-1}] {A}+ {B}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8df558c371c7f125f5833608e30f847abe2601de)



![{\displaystyle {\ce {{A}+{B}<=>{[AB]^{\ddagger }}->{P}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0b873373ba74f1671f87574af29e3a0a9ba9c63d)
![{\displaystyle K^{\ddagger }={\frac {\ce {[AB]^{\ddagger }}}{\ce {[A][B]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1465c535ba1f38d0eb964550468ee6c1f19aeb98)
![{\displaystyle [{\ce {AB}}]^{\ddagger }=K^{\ddagger }[{\ce {A}}][{\ce {B}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a67224b747342a2c608a96509499f845d991e801)
![{\displaystyle {\frac {d[{\ce {P}}]}{dt}}=k^{\ddagger }[{\ce {AB}}]^{\ddagger }=k^{\ddagger }K^{\ddagger }[{\ce {A}}][{\ce {B}}]=k[{\ce {A}}][{\ce {B}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/618074b91e2c1707bac08640100ceed7c7da2214)












![{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=e^{-\Delta \Delta G^{\ddagger }/RT}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ac8276860d8cfb32f02aba8aba55acef114beb8b)


![{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=10^{-\Delta G^{\circ }/(1.36\ \mathrm {kcal/mol} )}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/91b01377882f2cca09a5e47e866e2f82b0a9a222)

![{\displaystyle {\frac {[\mathrm {A} ]}{[\mathrm {B} ]}}=10^{-\Delta \Delta G^{\ddagger }/(1.36\ \mathrm {kcal/mol} )}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b17890458cfb78285761eed11143f5343072c979)