偶联反 应
偶联
偶联
机 理
[编辑]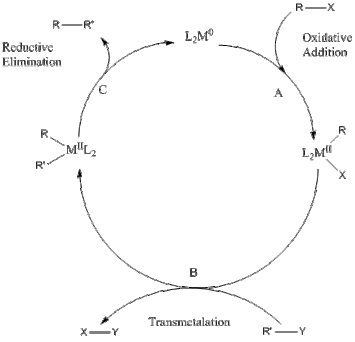
偶联
一项计算化学研究中表明,
另一种假说认为,
催化剂
[编辑]偶联
如下一些关于钴催化的偶联反应的综述[8],钯[9][10][11][12][13]
离去基 团
[编辑]离去
操作 条件
[编辑]虽然
类型
[编辑]| 发现 |
类型 | 催化剂 | 备注 | ||||||
| 1855 | R-X | sp³ | R-X | sp³ | 以鈉 |
||||
| 1869 | RC≡CH | sp | RC≡CH | sp | Cu | 氧气 |
|||
| 乌尔曼反应(Ullmann reaction) | 1901 | Ar-X | sp² | Ar-X | sp² | Cu | 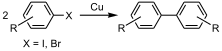
| ||
| 冈伯 |
1924 | Ar-H | sp² | Ar-N2X | sp² | 需碱 |

| ||
| Cadiot-Chodkiewicz偶联 |
1957 | RC≡CH | sp | RC≡CX | sp | Cu | 需碱 |

| |
| Castro-Stephens偶联 |
1963 | RC≡CH | sp | Ar-X | sp² | Cu | |||
| 1967 | R2CuLi | R-X | |||||||
| Cassar |
1970 | 烯烃 | sp² | R-X | sp³ | Pd | 需碱 |
||
| 1972 | Ar-MgBr | sp²/sp³ | Ar-X | sp² | Pd |

| |||
| 赫克 |
1972 | 烯烃 | sp² | R-X | sp² | Pd | 需碱 |
||
| 1975 | RC≡CH | sp | R-X | sp³/sp² | Pd |
需碱 |
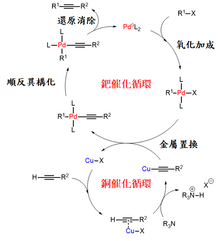
| ||
| 1977 | R-Zn-X | sp³/sp²/sp | R-X | sp³/sp² | Pd |
||||
| 1978 | R-SnR3 | sp³/sp²/sp | R-X | sp³/sp² | Pd | ||||
| 铃木 |
1979 | R-B(OR)2 | sp² | R-X | sp³/sp² | Pd | 需碱 |
||
| Hiyama偶联 |
1988 | R-SiR3 | sp² | R-X | sp³/sp² | Pd | 需碱 |

| |
| Buchwald–Hartwig偶联 |
1994 | R2N-R SnR3 | sp | R-X | sp² | Pd | N-C偶联 |
||
| 1998 | RCO(SEt) | sp2 | R-Zn-I | sp3 | Pd | 
| |||
| 偶联 | |||||||||
杂项反 应
[编辑]
应用
[编辑]许多偶联
参 见
[编辑]参考 资料
[编辑]- ^ Organic Synthesis using Transition Metals Rod Bates ISBN 978-1-84127-107-1
- ^ New Trends in Cross-Coupling: Theory and Applications Thomas Colacot (Editor) 2014 ISBN 978-1-84973-896-5
- ^ The Nobel Prize in Chemistry 2010 - Richard F. Heck, Ei-ichi Negishi, Akira Suzuki. NobelPrize.org. 2010-10-06 [2010-10-06]. (
原始 内容 存 档于2012-10-26). - ^ Palladium-Catalyzed Cross-Coupling: A Historical Contextual Perspective to the 2010 Nobel Prize Dr. Carin C. C. Johansson Seechurn, Dr. Matthew O. Kitching, Dr. Thomas J. Colacot, Prof. Victor Snieckus Angew. Chem. Int. Ed. 2012, 51, 5062-5085. doi:10.1002/anie.201107017
- ^ Hartwig, J. F. Organotransition Metal Chemistry, from Bonding to Catalysis; University Science Books: New York, 2010. ISBN 189138953X
- ^ V. P. Ananikov, D. G. Musaev, K. Morokuma, “Theoretical Insight into the C-C Coupling Reactions of the Vinyl, Phenyl, Ethynyl, and Methyl Complexes of Palladium and Platinum” Organometallics 2005, 24, 715. doi:10.1021/om0490841
- ^ 7.0 7.1 Benny Bogoslavsky, Ophir Levy, Anna Kotlyar, Miri Salem, Faina Gelman and Avi Bino. Do Carbyne Radicals Really Exist in Aqueous Solution?. Angewandte Chemie International Edition. 2012, 51 (1): 90–94. PMID 22031005. doi:10.1002/anie.201103652.
- ^ Cobalt-Catalyzed Cross-Coupling Reactions Grard Cahiez and Alban Moyeux Chem. Rev., 2010, 110 (3), pp 1435–1462 Publication Date (Web): February 11, 2010 (Review) doi:10.1021/cr9000786
- ^ Carbon−Carbon Coupling Reactions Catalyzed by Heterogeneous Palladium Catalysts Lunxiang Yin and Jürgen Liebscher Chem. Rev., 2007, 107 (1), pp 133–173 Publication Date (Web): December 21, 2006 (Article) doi:10.1021/cr0505674
- ^ Advances in Transition Metal (Pd,Ni,Fe)-Catalyzed Cross-Coupling Reactions Using Alkyl-organometallics as Reaction Partners Ranjan Jana, Tejas P. Pathak, and Matthew S. Sigman Chem. Rev., 2011, 111 (3), pp 1417–1492 doi: 10.1021/cr100327p
- ^ Efficient, Selective, and Recyclable Palladium Catalysts in Carbon−Carbon Coupling Reactions rpd Molnr Chem. Rev., 2011, 111 (3), pp 2251–2320 doi:10.1021/cr100355b
- ^ Palladium-Catalyzed Cross-Coupling Reactions of Organoboron Compounds Norio. Miyaura, Akira. Suzuki Chem. Rev., 1995, 95 (7), pp 2457–2483 doi:10.1021/cr00039a007
- ^ Diazonium Salts as Substrates in Palladium-Catalyzed Cross-Coupling Reactions Anna Roglans, Anna Pla-Quintana, and Marcial Moreno-Mañas Chem. Rev., 2006, 106 (11), pp 4622–4643 doi:10.1021/cr0509861
- ^ Nickel-Catalyzed Cross-Couplings Involving Carbon−Oxygen Bonds Brad M. Rosen, Kyle W. Quasdorf, Daniella A. Wilson, Na Zhang, Ana-Maria Resmerita, Neil K. Garg, and Virgil Percec Chem. Rev., 2011, 111 (3), pp 1346–1416 doi:10.1021/cr100259t
- ^ Selected Patented Cross-Coupling Reaction Technologies Jean-Pierre Corbet and Gérard Mignani Chem. Rev., 2006, 106 (7), pp 2651–2710 2006 (Article) doi:10.1021/cr0505268
- ^ Copper-Mediated Coupling Reactions and Their Applications in Natural Products and Designed Biomolecules Synthesis Gwilherm Evano, Nicolas Blanchard and Mathieu Toumi Chem. Rev., 2008, 108 (8), pp 3054–3131 doi:10.1021/cr8002505
- ^ M. Lafrance, C. N. Rowley, T. K. Woo and K. Fagnou. Catalytic Intermolecular Direct Arylation of Perfluorobenzenes. J. Am. Chem. Soc. 2006, 128 (27): 8754–8756. PMID 16819868. doi:10.1021/ja062509l.
- ^ R.H. Crabtree, The Organometallic Chemistry of the Transition Metals 4th Ed.
- ^ Organotransition Metal Chemistry: From Bonding to Catalysis John Hartwig
|
