氧化镓
| 氧化镓 | |
|---|---|
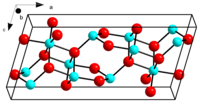
| |
| 别名 | 氧化镓(III) |
| 识别 | |
| CAS |
12024-21-4 |
| PubChem | 5139834 |
| ChemSpider | 4313617 |
| SMILES |
|
| InChI |
|
| InChIKey | QZQVBEXLDFYHSR-OGCFUIRMAC |
| RTECS | LW9650000 |
| Ga2O3 | |
| 187.444 g·mol⁻¹ | |
| 6.44 g/cm3( 5.88 g/cm3( | |
| 熔点 | 1900 °C(2173 K) |
| 难溶 | |
| 危险 | |
| 其他阴离 |
硒化镓 碲化镓 |
| 其他阳离 |
氧化硼 氧化铝 氧化铟 氧化铊 |
| 氧化 氢氧 | |
氧化镓
制 备[编辑]
氧化镓可以通过在
- 2 C + Ga2O3 → Ga2O + 2 CO
- Ga2O3 + 3 C → 2 Ga + 3 CO
- 2 Ga2O + 2 O2 → 2 Ga2O3
- 4 Ga + 3 O2 → 2 Ga2O3
α -Ga2O3可 以通过在65 kbar与 1100℃加 热β -Ga2O3得 到 。其水 合 物 可 以通过在500℃分解 沉淀并老化 的 氢氧化 镓得 到 。γ -Ga2O3通 过在400~500℃迅速 加 热氢氧化镓凝 胶得 到 。多 晶 体 可 以通过直接的 溶剂热反 应制备。[3]δ -Ga2O3由 Ga(NO3)3在 250˚C热分解 得 到 。ε -Ga2O3可 以通过550℃短 暂加热δ -Ga2O3 30分 钟得到 。[1]
化学 性 质[编辑]
氧化镓可以和碱
4羟基
它和氯化氢气
- Ga2O3 + 6 HCl → 2 GaCl3 + 3 H2O
- Ga2O3 + 6 HF → 2 GaF3·3H2O
它可以被氢气还原为氧化亚镓(
- Ga2O3 + 2 H2 → Ga2O + 2 H2O
- Ga2O3 + 4 Ga → 3 Ga2O
参考 文献 [编辑]
- ^ 1.0 1.1 Bailar, J; Emeléus, H; Nyholm, R; Trotman-Dickenson, A. Comprehensive Inorganic Chemistry. 1973, 1, 1091
- ^
郭 彦, 吴强,王 喜章 . 氧化镓纳米 带的合成 和 发光性 质研究 . 无机化学 学 报, 2005. 21(5) - ^ Playford, H. Y; Hannon, A. C; Barney, E. R; Walton, R. I. Chem. Eur. J. 2013, 19, 2803
- ^ The Chemistry of Aluminium, Gallium, Indium and Thallium, Anthony John Downs, 1993, ISBN 075140103X , ISBN 978-0751401035
- ^ Inorganic Reactions and Methods, the Formation of Bonds to Halogens (Part 2), J J Zuckerman, Ed: A P Hagen, eBook, 17 September 2009, Wiley-VCH Verlag GmbH, ISBN 9780470145395
- ^ 无机
化学 丛书第 二 卷 铍 碱土金属 铝 镓分族 .科学 出版 社 . pp 556. 2.12 氧化物 、氢氧化物 - ^ Determination of Gallium in a Cerium Surrogate and in Drops from a Copper Collector by ICP as Model Studies for the Removal of Gallium from Plutonium, HF Koch, LA Girard, DM Roundhill - ATOMIC SPECTROSCOPY, 1999, vol 20, 1, 30
- ^ ADVANCES IN INORGANIC CHEMISTRY AND RADIOCHEMISTRY, Volume 5, The chemistry of Gallium, N.N. Greenwood, ED H. J. Emeleus, A. G. Sharpe 1963, Elsevier, Academic Press
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
