过三氧化氢也称为“三氧化氢”或“三氧化二氢”,其化学式为“H2O3”或“HOOOH”,是氢元素的氧化物。他是一种不稳定的化合物,在水溶液中会分解为水和单线态氧:
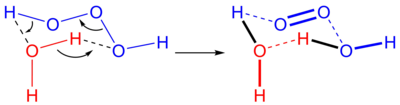
上述反应的逆反应(向水分子中插入单线态氧原子)一般情况下由于单线态氧原子不足而速率小于正反应速率。
理论研究表明,过三氧化氢有顺式和反式共两种异构体,其中反式异构体比顺式异构体更稳定。二阶全活化空间微扰理论(complete active space perturbation theory of second order,CASPT2)预测结果显示,在单激发态中,顺式过三氧化氢寿命最长的激发态为21A",跃迁能为167.43nm,寿命为1.44×10-5s;而反式过三氧化氢寿命最长的激发态为21A,其跃迁能为165.52nm,寿命为2.07×10-5s。[1]
在生命系统中,臭氧是由单线态氧形成的,现在推测其原理是:臭氧是单线态氧与水产生的H2O3的抗体催化产物。[2]
过三氧化氢可由O3和H2O2的反应或水的电解少量制备。用以上两种反应制得的过H2O3的量虽然较少,但已可检测出其存在。
若需获得大量H2O3,则要利用有机还原剂(例如氢化偶氮苯)在有机溶剂中低温还原O3,H2O3也能在有机过三氧化氢分解时产生(ROOOH)。[3]
O3与H2O2反应(过臭氧化)的过程也被称为“过臭氧过程”(Peroxone process)。而O3与H2O2的混合物曾被用作含有各种有机化合物的地下水的处理剂。上述反应也能产生H2O5及一些环状化合物。[4]
光谱学分析已指出H2O3分子具有曲折的结构(H-O-O-O-H),具有C2对称性,其中,H2O3O-O键的键长约为142.8pm,略短于H2O3中的146.4pm。O-H键的键长为96.6pm,H-O-O键角为101.9°,O-O-O键角为106.8°,H-O-O-O二面角为81.2°。[3]
H2O3还可能以多种二聚体及三聚体的形式存在。
H2O3是一种弱电解质,其酸性比H2O2略强,在溶液中可电离产生H+和OOOH-。[5]
其能自发地分解为水与单线态氧。室温下有机溶剂中的H2O3的半衰期约为16min,而H2O3在水中的半衰期只有几毫秒。
H2O3能与有机硫化物反应生成亚砜,但现在对这类反应的了解仍不多。
存在与存在形式
[编辑]由于在生命系统中H2O3像臭氧/过氧化氢混合物一样,也能由人体内的抗体能产生,并利用其强氧化性对抗入侵的细菌等病原体。所以新近的研究认为H2O3是上述混合物中起抗菌作用的活性物质。[2][6]生命系统中H2O3由免疫细胞产生的单线态氧和水反应获得(该化学反应的方向视各物质的浓度而定)。[3][7]
2005年,H2O3被利用微波光谱学在超音速客机中发现,其分子呈现反式构象(trans conformation),其中的O-O键短于H2O2中的O-O键。
计算化学方面的预测表明还可能有包含更多氧原子的链状分子(或多氧化氢)存在,在低温气体中,甚至连具有无数个氧原子的链也可能存在。
在该证据支持下,一项对星际物质中的这类物质的寻找可能将会展开。[5]
- ^ 王连宾、吴文鹏、张敬来. 反式和顺式HOOOH的电子光谱的理论研究. 物理化学学报. 2006, 22 (8): 1079–1084.
- ^ 2.0 2.1 Paul T. Nyffeler, Nicholas A. Boyle, Laxman Eltepu, Chi-Huey Wong, Albert Eschenmoser, Richard A. Lerner, Paul Wentworth Jr. Dihydrogen Trioxide (HOOOH) Is Generated during the Thermal Reaction between Hydrogen Peroxide and Ozone. Angewandte Chemie International Edition. 2004, 43 (35): 4656–4659. PMID 15317003. doi:10.1002/anie.200460457.
- ^ 3.0 3.1 3.2 Božo Plesničar. Progress in the Chemistry of Dihydrogen Trioxide (HOOOH). Acta Chim. Slov. 2005, 52: 1–12.
- ^ Xin Xu and William A. Goddard III. Peroxonechemistry:Formation of H2O3 and ring-(HO2)(HO3) from O3/H2O2.
- ^ 5.0 5.1 Kohsuke Suma, Yoshihiro Sumiyoshi, and Yasuki Endo. The Rotational Spectrum and Structure of HOOOH. J. Am. Chem. Soc. 2005, 127 (43): 14998–14999 [2020-09-19]. PMID 16248618. doi:10.1021/ja0556530. (原始内容存档于2013-05-23).
- ^ A Time-Honored Chemical Reaction Generates an Unexpected Product (页面存档备份,存于互联网档案馆), News & Views, September 13, 2004
- ^ Roald Hoffmann. The Story of O. American Scientist. 2004 [2011-01-14]. (原始内容存档于2016-03-03).

