三氯化镱(化学式:YbCl3)是一種无机化合物。
鐿(Ytterbium),一種鑭系元素,1878年由 Marignac 發現,並以瑞典小鎮(Ytterby)命名。[1]在文獻記載中,直到1946年才由Hoogschagen首次合成YbCl3。[2] 在目前YbCl3是一個現成可用的Yb3+離子來源,這就是為什麼YbCl3的研究具有化學上的重要性。
Yb3+(來自 YbCl3)的價電子組態是 4f135s25p6,這是影響Yb3+化學行為的重要關鍵。Yb3+的大小也影響它的催化性能和生物學上的應用。例如,當Ce+3和Yb+3都有一個未配對f電子時,Ce3+體積比Yb3+大很多,因為當 f 電子較 d 電子缺乏屏蔽作用時,有效核電荷數增加,鑭系元素則會變小。[1] 這就是所謂的鑭系收縮。Yb3+的小體積使其有快速的催化能力,而且原子半徑(0.99 Ǻ)可比得上許多重要的生物離子。[1]
因為許多測量都是在氣態下(YbCl3能以[YbCl6]-3[3]或Yb2Cl6[4]的形態存在)操作,熱力學性質的製表很難完成。Yb2Cl6 的形態是電子碰撞質譜儀發現 (Yb2Cl5+)而獲得。[4] 從大量的低激發態的f-d和f-f電子躍遷產生的額外併發物中獲取實驗數據。[5]儘管有這些問題,YbCl3的熱力學性質已經獲得,而且C3V對稱團已經根據四個主動式紅外震盪確定。[5]
YbCl3 可由 Yb2O3與四氯化碳[6],或熱鹽酸反應製得。[7]
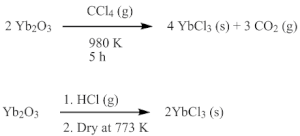
在實務上,有更好的方法來製備實驗用的YbCl3。HCl溶液/氯化銨法是技術等級低且很有效的方法。另外水合YbCl3可利用各種試劑脫水,尤其是氯化三甲基矽烷。其他已發表的方法包括在密閉試管中微細的金屬粉末與氯化汞在高溫下反應。溶解 YbCl3的各種方法也已經被提出,包括了在供體溶劑如THF中與各種鹵烴反應,或以氯化三甲基矽烷或亞硫醯氯在如THF的溶劑中脫水的水合氯化物。
YbCl3,有一個未成對的f電子,為填補4f軌域,可當作路易斯酸。YbCl3的路易斯酸性質,讓YbCl3過渡狀態中配位(通常為[YbCl2]+)催化烷基化反應,如羟醛反应(Aldol reaction)[8]和 Pictet-Spengler反應。[9]

在合成有機化學中Aldol反應是一個多功能的反應。YbCl3催化路易士酸,即幫助Pd(0)催化酮烯醇和乙醛間的decarboxylative Aldol反應。以過渡態A和B表示鐿鹽作為路易士酸的配位方式。[8] 以R = tert-butyl 和
R' = -(CH2)2Ph描述decarboxylative Aldol反應,其反應的產出顯示YbCl3是一種有效的路易士酸催化劑:
金屬鹽類[8]
|
2的产率(%)
|
FeCl3
|
40
|
ZnCl2
|
68
|
CuCl2
|
40
|
LaCl3
|
60
|
YbCl3
|
93
|
Pictet-Spengler反應產生一個有價值的tetrahydro-β-carboline ring system,它可以用於製備吲哚生物鹼。[9] YbCl3催化路易士酸的反應,可以使之獲得更多的產量,並且讓反應時間從4天降低到24小時。[9]
Yb3+的小體積使它有快速的催化作用,但代價是只能選擇性催化特定反應。例如,meso-1,2-diols的mono-acetylation與YbCl3是反應最快的(2 h)。但是mono-acetylated產物的化學選擇性比
CeCl3 (23 h, 85%)低(50%)。[10]
YbCl3 是一種 核磁共振位移試劑,讓和YbCl3接觸的原子核與沒有與位移試劑接觸的原子核產生不同的共振。[11] 一般而言,順磁性離子如(鑭系)+3離子即是可用的位移試劑。[11]YbCl3大大的影響了膜生物學,39K+ and23Na+的移動是建立電化學梯度的關鍵.[11] 神經訊號是一種生命的基礎領域,也許可以利用使用YbCl3的核磁共振技術來探測。YbCl3 也可以用來作為鈣離子探針,和鈉離子探針的裝置相似。[12]
YbCl3也用於追踨動物的消化。一些豬飼料的添加物,像益生菌,即添加在固態飼料或可飲用的液體中。YbCl3 跟隨這些固態食物,並協助確定何種食物狀態是吸收食物添加物的最佳狀態。[13]YbCl3濃度是以ICP(感應耦合電漿)質譜儀定量在0.0009 μg/mL之間。[1]
YbCl3濃度隨著時間改變,以動物對固體微粒的消化流速而定。因為YbCl3可以輕易的和排泄物一起排出體外,且不會改變體重、臟器重量、或血容比,這些都已在實驗鼠上觀察到。[12]
YbCl3的催化性本質也可應用在DNA微陣列技術上,或稱為基因晶片。[14]
YbCl3能讓附著在標的DNA上的螢光劑增加到50-80倍,這能造成傳染病檢測的革命性突破(例如快速檢測肺結核)。[14]
- ^ 1.0 1.1 1.2 1.3 Evans, C.H. Biochemistry of the Lanthanides; Plenum: New York, 1990.
- ^ Hoogschagen, J. Pysica 1946, 11(6), 513-517.
- ^ Gau, W.J.; Sun, I.W. J. Electrochem. Soc. 1996, 143(1), 170-174.
- ^ 4.0 4.1 Chervonnyi, A.D.; Chervonnaya, N.A. Russ. J. Inorg. Chem. (Engl. Transl.) 2004, 49(12), 1889-1897.
- ^ 5.0 5.1 Zasorin, E.Z. Russ. J. Phys. Chem. (Engl. Transl.) 1988, 62(4), 441-447.
- ^ Goryushkin, V.F.; Zalymova, S.A.; Poshevneva, A.I.Russ. J. Inorg. Chem. (Engl. Transl.) 1990, 35(12), 1749-1752.
- ^ Jörg, S.; Seifert, H.J. Termochim. Acta 1998, 318, 29-37.
- ^ 8.0 8.1 8.2 Lou, S.; Westbrook, J.A.; Schaus, S.E. J. Am. Chem. Soc. 2004, 126, 11440-11441.
- ^ 9.0 9.1 9.2 Srinivasan, N.; Ganesan, A. Chem. Commun. 2003, 916-917.
- ^ Clarke, P.A. Tetrahedron Lett. 2002, 43, 4761-4763.
- ^ 11.0 11.1 11.2 Hayer, M.K.; Riddell, F.G. Inorg. Chim. Acta 1984, 92, L37-L39.
- ^ 12.0 12.1 Shinohara, A.; Chiba, M.; Inaba, Y. J. Alloys Cmpds. 2006, 408-412, 405-408.
- ^ Ohashi, Y.; Umesaki, Y.; Ushida, K. Int. J. Food Micro. 2004, 96, 61-66.
- ^ 14.0 14.1 Browne, K.A. J. Am. Chem. Soc. 2002, 124, 7950-7962.



