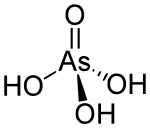
砷酸
IUPAC名 めい
识别
CAS号 ごう
7778-39-4 Y
ChemSpider
229
SMILES
InChI
1/AsH3O4/c2-1(3,4)5/h(H3,2,3,4,5)
InChIKey
DJHGAFSJWGLOIV-UHFFFAOYAY
ChEBI
18231
RTECS
CG0700000
KEGG
C01478
性 せい
化学 かがく 式 しき H3 AsO4
摩 ま 量 りょう 141.94 g/mol g·mol⁻¹
外 そと 白色 はくしょく 半 はん 透明 とうめい 潮解 ちょうかい 晶 あきら 体 からだ
密度 みつど 2.5 g/cm3
熔点
35.5 °C(309 K)
沸点 ふってん ≥ 100 °C 分解 ぶんかい
溶解 ようかい 性 せい 水 みず 16.7 g/100 mL
溶解 ようかい 性 せい 溶于乙 おつ 醇 あつし
pK a
2.19, 6.94, 11.5
结构
分子 ぶんし 四 よん 面体 めんてい
危险性 せい
警示术语
R:R23/25 R45 R50/53
安全 あんぜん S:S53 S45 S60 S61
欧 おう 盟 めい 分 ぶん T+ C N
NFPA 704
闪点
不 ふ 可燃 かねん
相 あい
其他阴离子 こ
磷酸
其他阳离子 こ
砷酸钠
相 あい 化学 かがく 品 ひん 亚砷酸 さん 五 ご 二 に
若 わか 非 ひ 注 ちゅう 明 あかり 所有 しょゆう 数 すう 据 すえ 均 ひとし 出自 しゅつじ 标准状 じょう 下 した
砷酸 为砷 (V)的 てき 含氧酸 さん ,分子 ぶんし 式 しき 3 AsO4 。三 さん 元 げん 中 ちゅう 强酸 きょうさん 酸性 さんせい 他 た 性 せい 磷酸 。
制 せい 取 と [ 编辑 ] 由 ゆかり 五 ご 二 に 水 すい
A
s
2
O
5
+
3
H
2
O
⇌
2
H
3
A
s
O
4
{\displaystyle \mathrm {As_{2}O_{5}+3\ H_{2}O\rightleftharpoons 2\ H_{3}AsO_{4}} }
反 はん 可 か 向 こう 左 ひだり 加入 かにゅう 五 ご 二 に 作 さく 吸水 きゅうすい 又 また 可 か 酸 さん 五 ご 二 に
砷酸也可由 ゆかり 砷 或 ある 三 さん 二 に 被 ひ 硝酸 しょうさん 應 おう 會 かい 生成 せいせい 副產物 ふくさんぶつ 三 さん 二 に 反 はん 以下 いか 可 か 析出 せきしゅつ 半 はん 水 みず 合 ごう 物 ぶつ 板 いた 状 じょう 以上 いじょう 析出 せきしゅつ 三 さん 5 As3 O10 )。[1] [2]
A
s
+
5
H
N
O
3
⟶
5
N
O
2
+
H
2
O
+
H
3
A
s
O
4
{\displaystyle \mathrm {As+5\ HNO_{3}\longrightarrow 5\ NO_{2}+H_{2}O+H_{3}AsO_{4}} }
A
s
2
O
3
+
2
H
N
O
3
+
3
H
2
O
⟶
{\displaystyle \mathrm {As_{2}O_{3}+2\ HNO_{3}+3\ H_{2}O\longrightarrow } }
N
2
O
3
+
2
H
3
A
s
O
4
⋅
1
2
H
2
O
{\displaystyle \mathrm {N_{2}O_{3}+2\ H_{3}AsO_{4}\cdot {\tfrac {1}{2}}H_{2}O} }
反應 はんのう 結束 けっそく 後 ご 若 わか 將 はた 所得 しょとく 液體 えきたい 冷 ひや 可 か 得 え 到 いた 色 しょく 結晶 けっしょう 形式 けいしき 析出 せきしゅつ 的 てき 的 てき 半 はん 水 みず 合 ごう 物 ぶつ 3 AsO4 ·½H2 O。如果進 しん 還 かえ 可 か 獲得 かくとく 的 てき 二水 にすい 合 ごう 物 ぶつ 3 AsO4 ·2H2 O[2]
砷酸二水 にすい 合 ごう 物 ぶつ 3 AsO4 · 2H2 O)只 ただ 可 か 通 どおり 下 しも 数 すう 天 てん 得 え 到 いた [3]
五 ご 二 に 可 か 緩慢 かんまん 與 あずか 水 みず 反應 はんのう 生成 せいせい 元 もと 或 ある 焦 こげ 與 あずか 冷水 れいすい 反應 はんのう 同樣 どうよう 可 か 生成 せいせい 的 てき 質 しつ 可 か 與 あずか 臭 ぐさ 應 おう 生成 せいせい
2 As + 3 H2 O + 5 O3 → 2 H3 AsO4 + 5 O2 性 せい [ 编辑 ] 物理 ぶつり 性 せい [ 编辑 ] 砷酸固体 こたい 在 ざい 空 そら 水 すい 合 ごう 物 ぶつ 3 AsO4 · ½H2 O 或 ある 3 AsO4 · 2H2 O (於 −30 °C)。平 ひら 脱水 だっすい 三 さん 5 As3 O10 )。加 か 分解 ぶんかい 2 O5 · 1.66H2 O。在 ざい 部 ぶ 失 しつ 水 すい [1]
3
H
3
A
s
O
4
⟶
Δ でるた
H
5
A
s
3
O
10
+
2
H
2
O
{\displaystyle {\rm {3H_{3}AsO_{4}\ {\overset {\mathit {\rm {\Delta }}}{\longrightarrow }}\ H_{5}As_{3}O_{10}+2H_{2}O}}}
饱和水溶液 すいようえき
毒性 どくせい 亚砷酸 さん ,但 ただし 高 だか LD50 (兔 うさぎ [4] 与 あずか 日本 にっぽん 被 ひ 列 れつ 医 い 外 がい 毒物 どくぶつ
化学 かがく 性質 せいしつ [ 编辑 ] 無 む 水物 みずもの 結晶 けっしょう 水 すい 忽 ゆるがせ 略 りゃく [5]
H3 AsO4 (s)
⇄
{\displaystyle \rightleftarrows \ }
3 AsO4 (aq), Δ でるた H °= 3.8 kJ mol-1 砷酸水溶液 すいようえき 的 てき 性 せい 不 ふ 强 つよし 但 ただし 比 ひ 同族 どうぞく 的 てき 强 きょう 第 だい 周期 しゅうき 元素 げんそ 的 てき 酸 さん 相似 そうじ 硒酸 、高 こう 化 か 性 せい 均 ひとし 强 きょう 硫酸 りゅうさん 与 あずか 高 こう [6]
H3 AsO4 (aq) + 2 H+ (aq) + 2 e- = H3 AsO3 (aq) + H2 O(l), E °= 0.575 V 例 れい 酸 さん 可 か 将 はた 子 こ
H3 AsO4 + 2 H+ + 2 I− → H3 AsO3 + I2 + H2 O 此外还有焦 こげ 4 As2 O7 )与 あずか 多 た n+2 Asn O3n+1 、(HAsO3 )n )。这两者 しゃ 酸 さん 根 ね 在 ざい 水溶液 すいようえき 中 ちゅう 都 みやこ 是 ただし 不 ふ 的 てき 遇 ぐう 水 すい 分解 ぶんかい 酸 さん 焦 こげ 与 あずか 多 た 固 かた 的 てき
水溶液 すいようえき 中 ちゅう 的 てき 電離 でんり 平衡 へいこう [ 编辑 ] 砷酸分子 ぶんし 在 ざい 水溶液 すいようえき 中分 なかぶん 三 さん 步 ほ 解 かい 第一步 だいいっぽ 强 きょう mol dm-3 水溶液 すいようえき 的 てき 電離 でんり 度 ど 約 やく 第 だい 在 ざい 酸性 さんせい 溶液 ようえき 中 ちゅう 可 か
H3 AsO4 (aq) + H2 O(l)
⇄
{\displaystyle \rightleftarrows \ }
3 O+ (aq) + H2 AsO4 - (aq), pK a1 = 2.24
H2 AsO4 - (aq) + H2 O(l)
⇄
{\displaystyle \rightleftarrows \ }
3 O+ (aq) + HAsO4 2- (aq), pK a2 = 6.96
HAsO4 2- (aq) + H2 O(l)
⇄
{\displaystyle \rightleftarrows \ }
3 O+ (aq) + AsO4 3- (aq), pK a3 = 11.50 与 あずか 解 かい 標準 ひょうじゅん 焓 、吉 よし 布 ぬの 与 あずか 熵 变值列 れつ 在 ざい 下面 かめん [5]
Δ でるた
H
∘
{\displaystyle {\Delta }H^{\circ }}
Δ でるた
G
∘
{\displaystyle {\Delta }G^{\circ }}
Δ でるた
S
∘
{\displaystyle {\Delta }S^{\circ }}
第 だい 一 いち 解離 かいり -7.07 kJ mol-1
12.84 kJ mol-1
-66.9 J mol- K-1
第 だい 二 に 解離 かいり 3.22 kJ mol-1
38.57 kJ mol-1
-118.7 J mol-1 K-1
第 だい 三 さん 解離 かいり 18.20 kJ mol-1
66.19 kJ mol-1
-161.1 J mol-1 K-1
砷酸根 ね [ 编辑 ] 砷酸根 ね 砷酸电离可 か 三 さん 正 せい 根 ね 4 3- )、一氢砷酸根离子(HAsO4 2- )与 あずか 2 AsO4 - )。三种阴离子的盐类均已获得。正 せい 根 ね 四 よん 面体 めんてい 根 ね 酸 さん 液 えき 中有 ちゅうう 微弱 びじゃく 的 てき 性 せい
砷酸盐 [ 编辑 ] 各 かく 酸 さん 通 どおり 不同 ふどう 的 てき 中和 ちゅうわ 可 か 金属 きんぞく 分解 ぶんかい 亦 また 可 か 得 とく 不可 ふか 淀 よどみ
焦 こげ 4 As2 O7 )与 あずか 焦 こげ 不同 ふどう 不可 ふか 通 どおり 酸 さん 加 か 脱水 だっすい 制 せい 得 え 只 ただ 能 のう 由 よし 失 しつ 水 すい 得 え 到 いた
2
N
a
2
H
A
s
O
4
⟶
Δ でるた
N
a
4
A
s
2
O
7
+
H
2
O
{\displaystyle {\rm {2Na_{2}HAsO_{4}\ {\overset {\mathit {\rm {\Delta }}}{\longrightarrow }}\ Na_{4}As_{2}O_{7}+H_{2}O}}}
2
C
a
H
A
s
O
4
⟶
Δ でるた
C
a
2
A
s
2
O
7
+
H
2
O
{\displaystyle {\rm {2CaHAsO_{4}\ {\overset {\mathit {\rm {\Delta }}}{\longrightarrow }}\ Ca_{2}As_{2}O_{7}+H_{2}O}}}
砷酸钠(Na3 AsO4 )水溶液 すいようえき 呈 てい 一 いち 2 HAsO4 )水溶液 すいようえき 呈 てい 弱 じゃく 二 に 2 AsO4 )水溶液 すいようえき 弱酸 じゃくさん 性 せい
砷酸钙(Ca3 (AsO4 )2 )用作 ようさく 殺虫 さっちゅう 作 さく 除草 じょそう 物 ぶつ 效果 こうか [1]
正 せい 金属 きんぞく 可 か 水 すい 金属 きんぞく
砷酸钙 (Ca3 (AsO4 )2 )砷酸钠 (Na3 AsO4 )砷酸盐矿物 ぶつ [ 编辑 ] 钴华 砷酸盐矿物 ぶつ 可 か 由 よし 的 てき 硫化 りゅうか 化 か 生成 せいせい 由 よし 物 ぶつ 中 ちゅう 的 てき 根 ね 被 ひ 根 ね 替 がえ 得 とく 物 ぶつ 例 れい 子 こ
水 みず 2 (AsO4 )(OH))橄榄铜矿 ,Olivenite (Cu2 (AsO4 )(OH))钴华 ,Erythrite (Co3 (AsO4 )2 ・8H2 O)镍華 ,Annaberigite (Ni3 (AsO4 )2 ・8H2 O)臭 におい 葱 ねぎ 石 せき 4 ・2H2 O)绿铅矿 ,Mimetite (Pb5 Cl(AsO4 )3 )應用 おうよう [ 编辑 ] 砷酸可用 かよう 作 さく 木材 もくざい 防腐 ぼうふ 劑 ざい 廣 こう 譜 ふ 生物 せいぶつ 殺 ころせ 滅 めつ 劑 ざい 玻璃 はり 和金 わきん 屬 ぞく 的 てき 整理 せいり 劑 ざい 並 なみ 可 か 參與 さんよ 合成 ごうせい 部分 ぶぶん 染料 せんりょう 但 ただし 毒性 どくせい 強烈 きょうれつ 故 こ 業 ぎょう 應用 おうよう 了 りょう 限 げん 制 せい 選 せん 兔 うさぎ 作爲 さくい 實驗 じっけん 對象 たいしょう 時 じ 的 てき 半 はん 致死 ちし 量 りょう 爲 ため [7]
参考 さんこう [ 编辑 ]
^ 1.0 1.1 1.2 化学 かがく 大 だい 辞典 じてん 編集 へんしゅう 委員 いいん 会 かい 化学 かがく 大 だい 辞典 じてん 共立 きょうりつ 出版 しゅっぱん 年 ねん ^ 2.0 2.1 G. Brauer (编). Arsenic Acid. Handbook of Preparative Inorganic Chemistry 1 2nd. New York: Academic Press. 1963: 601. ^ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 601.
^ Merck Index 13th
^ 5.0 5.1 D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982)
^ FA コットン, G. ウィルキンソン著 ちょ 中原 なかはら 勝 まさる 儼 げん 訳 やく 無機 むき 化学 かがく 培風館 ばいふうかん 年 ねん 原書 げんしょ
^ Joachimoglu, G. Biochemische Zeitschrift. 1915, 70 : 144.