出典: フリー百科事典『ウィキペディア(Wikipedia)』
印刷用ページはサポート対象外です。表示エラーが発生する可能性があります。ブラウザーのブックマークを更新し、印刷にはブラウザーの印刷機能を使用してください。
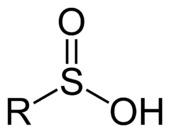 スルフィン酸の一般構造式
スルフィン酸の一般構造式
スルフィン酸(スルフィンさん、sulfinic acid)とは、有機硫黄化合物の一種で、構造式が R-S(=O)OH と表される一連のオキソ酸のこと。
性質
スルフィン酸は一般に、スルホン酸と同程度の強酸性を示す。しかし、化学的にはやや不安定で、不均化を起こしてスルホン酸とスルフェン酸に変わる。スルフェン酸はさらに不安定であり、不均化や付加などを起こす。
金属塩の形では比較的安定となり、芳香族スルフィン酸のナトリウム塩は市販品として入手可能である。
命名法
IUPAC命名法においてスルフィン酸は、例えばベンゼンスルフィン酸 (benzenesulfinic acid, C6H5-S(=O)OH) のように、母骨格名に接尾辞「スルフィン酸」を添えて表す。-S(=O)OH 部位は、スルフィノ基 (sulfino group) と呼ばれ、対応する接頭辞は「スルフィノ」である。
合成
通常、塩化スルホニルを金属亜鉛などで還元し[1]、得られる亜鉛の塩を酸で分解してスルフィン酸とする。


亜硫酸ナトリウムなど、他の還元剤を用いる手法も知られる。
反応
スルフィン酸に塩基を作用させると、共役塩基であるスルフィナートアニオンが発生する。

このスルフィナートアニオンは求核剤として振る舞う。例えばハロゲン化アルキルと反応すると、炭素-硫黄結合が生成してスルホンが得られる。

この反応では、HSAB則 で堅いとされる求電子剤を用いた場合は特に、炭素が酸素と結合したスルフィン酸エステル (R-S(=O)OR') が副生物となる。
参考文献
- Smith, M. B.; March, J. in March's Advanced Organic Chemistry, 5th ed., 2001, Wiley.
- ^ 例: Whitmore, F. C.; Hamilton, F. H. Org. Synth., Coll. Vol. 1, p.492 (1941); Vol. 2, p.89 (1922). オンライン版
関連項目





