超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 超 ちょう 原子 げんし 価 か 分子 ぶんし 英 えい hypervalent molecule )とは、形式 けいしき 的 てき 原子 げんし 価 か 殻 から 以上 いじょう 電子 でんし 持 も 典型 てんけい 元素 げんそ 含有 がんゆう 化合 かごう 物 ぶつ 分子 ぶんし 状態 じょうたい 典型 てんけい 元素 げんそ 超 ちょう 原子 げんし 価 か 状態 じょうたい 超 ちょう 原子 げんし 価 か 取 と 言 い 五 ご 塩化 えんか
PCl
5
{\displaystyle {\ce {PCl5}}}
六 ろく 化 か 硫黄 いおう
SF
6
{\displaystyle {\ce {SF6}}}
三 さん 化物 ばけもの
I
3
−
{\displaystyle {\ce {I3^-}}}
超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 例 れい リン酸 さん (
PO
4
3
−
{\displaystyle {\ce {PO4^{3-}}}}
超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 代表 だいひょう 例 れい 挙 あ 近年 きんねん 解析 かいせき 結果 けっか 超 ちょう 原子 げんし 価 か 状態 じょうたい 寄与 きよ 少 すく 指摘 してき [1] 超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 酸化 さんか 数 すう 最 もっと 低 ひく 状態 じょうたい 族 ぞく 元素 げんそ 持 も 化合 かごう 物 ぶつ 1969年 ねん に初 はじ 定義 ていぎ [2]
いくつかの特殊 とくしゅ 超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 存在 そんざい
超 ちょう 原子 げんし 価 か 分子 ぶんし 性質 せいしつ 分類 ぶんるい 関 かん 議論 ぎろん ギルバート・ルイス およびアーヴィング・ラングミュア と1920年代 ねんだい 化学 かがく 結合 けつごう 性質 せいしつ 関 かん 議論 ぎろん 遡 さかのぼ [3] 超 ちょう 原子 げんし 価 か 描写 びょうしゃ 二 に 中心 ちゅうしん 二 に 電子 でんし 結合 けつごう 重要 じゅうよう 性 せい 主張 しゅちょう 分子 ぶんし 説明 せつめい 拡張 かくちょう 則 そく 用 もち 一方 いっぽう 則 そく 優勢 ゆうせい 性 せい 支持 しじ 則 そく 破 やぶ 超 ちょう 原子 げんし 価 か 説明 せつめい 結合 けつごう 用 もち 好 この 例 たと
SF
4
2
+
{\displaystyle {\ce {SF4^{2+}}}}
2
F
−
{\displaystyle {\ce {2F^-}}}
1920年代 ねんだい 末 まつ 年代 ねんだい 二 に 中心 ちゅうしん 一 いち 電子 でんし 結合 けつごう 存在 そんざい 主張 しゅちょう 拡張 かくちょう 則 そく 結合 けつごう 性 せい 必要 ひつよう 超 ちょう 原子 げんし 価 か 分子 ぶんし 結合 けつごう 合理 ごうり 的 てき 説明 せつめい 当時 とうじ 受 う 入 い [3] 年代 ねんだい 年代 ねんだい ピメンテル (英語 えいご 版 ばん 三 さん 中心 ちゅうしん 四 よん 電子 でんし 結合 けつごう 考 かんが 世 よ 広 ひろ 考 かんが 数 すう 十 じゅう 年 ねん 前 まえ 提示 ていじ 試 こころ 本質 ほんしつ 的 てき 同 おな 概念 がいねん 三 さん 中心 ちゅうしん 四 よん 電子 でんし 結合 けつごう 局在 きょくざい 化 か 非 ひ 結合 けつごう 性 せい 電子 でんし 残 のこ 共 とも 線 せん 的 てき 二 に 中心 ちゅうしん 一 いち 電子 でんし 結合 けつごう 成 な 別 べつ 見方 みかた [3]
実際 じっさい 超 ちょう 原子 げんし 価 か 有機 ゆうき 分子 ぶんし 調製 ちょうせい 試 こころ 世紀 せいき 前半 ぜんはん ヘルマン・シュタウディンガー とゲオルク・ウィッティヒ によって始 はじ 彼 かれ 現存 げんそん 原子 げんし 価 か 理論 りろん 挑 いど 窒素 ちっそ 中心 ちゅうしん 超 ちょう 原子 げんし 価 か 分子 ぶんし 調製 ちょうせい 成功 せいこう [4] 超 ちょう 原子 げんし 価 か 理論 りろん 的 てき 基礎 きそ 研究 けんきゅう 詳 くわ 説明 せつめい [2]
1990年 ねん 第 だい 周期 しゅうき 元素 げんそ 超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 中 ちゅう 結合 けつごう 軌道 きどう 混成 こんせい 役割 やくわり 決定的 けっていてき 排除 はいじょ 影響 えいきょう 力 りょく 大 おお 研究 けんきゅう 発表 はっぴょう 長 なが 間 あいだ 分子 ぶんし 軌道 きどう 理論 りろん 用 もち 分子 ぶんし 描写 びょうしゃ 論争 ろんそう 混乱 こんらん 的 てき 混乱 こんらん 一部 いちぶ 化合 かごう 物 ぶつ 描写 びょうしゃ 使 つか 基底 きてい 関数 かんすう 系 けい 関数 かんすう 含 ふく 事実 じじつ 起因 きいん 不合理 ふごうり 高 たか 歪 いが 構造 こうぞう 得 え 分子 ぶんし 波動 はどう 関数 かんすう 対 たい 関数 かんすう 寄与 きよ 大 おお 事実 じじつ 軌道 きどう 結合 けつごう 関与 かんよ 意味 いみ 歴史 れきし 的 てき 解釈 かいしゃく 原子 げんし 価 か 結合 けつごう 法 ほう 観点 かんてん 軌道 きどう 軌道 きどう 軌道 きどう 混成 こんせい 3 dとsp3 d2 混成 こんせい 軌道 きどう 結合 けつごう 関与 かんよ 軌道 きどう 超 ちょう 原子 げんし 価 か 関係 かんけい 結論 けつろん 付 つ [5]
超 ちょう 原子 げんし 価 か 言葉 ことば 化学 かがく 的 てき 結合 けつごう 様式 ようしき 関 かん 何 なん 情報 じょうほう 示 しめ 言 い 理由 りゆう 年 ねん 超 ちょう 配 はい 位 い 言葉 ことば 提案 ていあん
超 ちょう 原子 げんし 価 か 概念 がいねん 電子 でんし 局在 きょくざい 化 か 役割 やくわり 分析 ぶんせき 行 おこな 非難 ひなん 受 う 超 ちょう 原子 げんし 価 か 結合 けつごう 根本 こんぽん 的 てき 違 ちが 無 な 超 ちょう 原子 げんし 価 か 言葉 ことば 使 つか 理由 りゆう 無 な 結論 けつろん [6]
PF5 のような電気 でんき 的 てき 陰性 いんせい 配 はい 位 い 子 こ 超 ちょう 配 はい 位 い 化合 かごう 物 ぶつ 中心 ちゅうしん 原子 げんし 電子 でんし 引 ひ 抜 ぬ 非 ひ 局在 きょくざい 化 か 中心 ちゅうしん 原子 げんし 実質 じっしつ 的 てき 電子 でんし 数 すう 電子 でんし 以下 いか 示 しめ 見方 みかた 5 のようなフッ素 ふっそ 構成 こうせい 要素 ようそ 超 ちょう 配 はい 位 い 化合 かごう 物 ぶつ 水素 すいそ 類縁 るいえん 体 たい ホスホラン PH5 は不安定 ふあんてい 化合 かごう 物 ぶつ 事 こと 合致 がっち
熱 ねつ 力学 りきがく 計算 けいさん 上 うえ 性 せい 程度 ていど 説明 せつめい
PF
4
+
F
−
{\displaystyle {\ce {PF4^+F^-}}}
三 さん 化 か
PF
3
{\displaystyle {\ce {PF3}}}
フッ素 ふっそ
F
2
{\displaystyle {\ce {F2}}}
反 はん 応 おう 生成 せいせい 際 さい 発熱 はつねつ 反応 はんのう 対 たい
PH
4
+
H
−
{\displaystyle {\ce {PH4^+H^-}}}
生成 せいせい 際 さい [7]
Durrantは、Atoms in molecules (英語 えいご 版 ばん 理論 りろん 得 え 原子 げんし 電荷 でんか 解析 かいせき 基 もと 超 ちょう 原子 げんし 価 か 代替 だいたい 定義 ていぎ 提唱 ていしょう [8] 方法 ほうほう 観測 かんそく 電荷 でんか 分布 ぶんぷ 再現 さいげん 妥当 だとう 性 せい 共有 きょうゆう 結合 けつごう 性 せい 共鳴 きょうめい 構造 こうぞう 任意 にんい 組合 くみあわ 得 え 任意 にんい 原子 げんし 形式 けいしき 共有 きょうゆう 電子 でんし 数 すう 原子 げんし 価 か 電子 でんし 当 とう 量 りょう γ がんま 呼 よ 定義 ていぎ 特定 とくてい 原子 げんし γ がんま 値 ね 大 おお 原子 げんし 超 ちょう 原子 げんし 価 か 代替 だいたい 定義 ていぎ 用 もち 定義 ていぎ 超 ちょう 原子 げんし 価 か 5 、SO4 2− 、XeF4 といった多 おお 化学 かがく 種 しゅ 中心 ちゅうしん 原子 げんし 電子 でんし 引 ひ 抜 ぬ 強 つよ 結合 けつごう 超 ちょう 原子 げんし 価 か 超 ちょう 配 はい 位 い 再 さい 分類 ぶんるい 一方 いっぽう 則 そく 満足 まんぞく 結合 けつごう 通常 つうじょう 書 か オゾン O3 、亜 あ 酸化 さんか 窒素 ちっそ トリメチルアミン-N -オキシド (CH3 )3 NOといった一部 いちぶ 化合 かごう 物 ぶつ 正真正銘 しょうしんしょうめい 超 ちょう 原子 げんし 価 か 分 わ リン酸 さん PO4 3− (γ がんま 非 ひ 超 ちょう 原子 げんし 価 か オルト硝酸塩 しょうさんえん NO4 3− (γ がんま 超 ちょう 原子 げんし 価 か γ がんま 計算 けいさん 例 れい 以下 いか 示 しめ
リン酸 さん 硝酸 しょうさん 原子 げんし 価 か 電子 でんし 当 とう 量 りょう 計算 けいさん 超 ちょう 原子 げんし 価 か 分子 ぶんし 結合 けつごう [ 編集 へんしゅう ] 超 ちょう 原子 げんし 価 か 分子 ぶんし 幾何 きか 構造 こうぞう 初期 しょき 考察 こうさつ 原子 げんし 結合 けつごう VSEPR模型 もけい によってうまく説明 せつめい 親 した 取 と 決 き 戻 もど 基 もと 5 ならびにAB6 型 かた 分子 ぶんし 三角 さんかく 両 りょう 錐 きり 八 はち 面体 めんてい 構造 こうぞう 取 と 観察 かんさつ 結合 けつごう 角 かく 結合 けつごう 長 ちょう オクテット則 そく の見掛 みか 違反 いはん 説明 せつめい 代替 だいたい 模型 もけい 提唱 ていしょう
1950年代 ねんだい 超 ちょう 原子 げんし 価 か 結合 けつごう 拡張 かくちょう 原子 げんし 価 か 殻 から 表現 ひょうげん 配 はい 位 い 配 はい 位 い 分子 ぶんし 中心 ちゅうしん 原子 げんし 原子 げんし 軌道 きどう 加 くわ 原子 げんし 軌道 きどう 利用 りよう 分子 ぶんし 構造 こうぞう 説明 せつめい 提示 ていじ ab initio 計算 けいさん 研究 けんきゅう 進歩 しんぽ 超 ちょう 原子 げんし 価 か 結合 けつごう 軌道 きどう 寄与 きよ 結合 けつごう 性質 せいしつ 描写 びょうしゃ 小 ちい 明 あき 描写 びょうしゃ 重要 じゅうよう 性 せい 度合 どあ 低 ひく 現在 げんざい 見 み [5] 配 はい 位 い 6 の場合 ばあい 軌道 きどう 結合 けつごう 形成 けいせい 関与 かんよ 硫黄 いおう 原子 げんし フッ素 ふっそ 原子 げんし 間 あいだ 電荷 でんか 移動 いどう 適切 てきせつ 共鳴 きょうめい 構造 こうぞう 超 ちょう 原子 げんし 価 か 説明 せつめい 示 しめ 下記 かき 参照 さんしょう
オクテット則 そく 改良 かいりょう 超 ちょう 原子 げんし 価 か 結合 けつごう 結合 けつごう 性 せい 含 ふく 試 こころ 改良 かいりょう 一 ひと 年 ねん 定性的 ていせいてき 分子 ぶんし 軌道 きどう 使 つか 超 ちょう 原子 げんし 価 か 結合 けつごう 描写 びょうしゃ 三 さん 中心 ちゅうしん 四 よん 電子 でんし 結合 けつごう 概念 がいねん 提唱 ていしょう 結合 けつごう 中心 ちゅうしん 原子 げんし 上 じょう 原子 げんし 軌道 きどう 中心 ちゅうしん 原子 げんし 両側 りょうがわ 配 はい 位 い 子 こ 原子 げんし 軌道 きどう 組 く 合 あ 与 あた 分子 ぶんし 軌道 きどう 描写 びょうしゃ 電子 でんし 対 たい 中心 ちゅうしん 原子 げんし 結合 けつごう 関与 かんよ 分子 ぶんし 軌道 きどう 占 し 目 め 電子 でんし 対 たい 非 ひ 結合 けつごう 性 せい 配 はい 位 い 子 こ 原子 げんし 軌道 きどう 成 な 分子 ぶんし 軌道 きどう 占 し 則 そく 保 たも 模型 もけい 支持 しじ [3]
三 さん 中心 ちゅうしん 四 よん 電子 でんし 結合 けつごう 定性的 ていせいてき 模型 もけい 超 ちょう 原子 げんし 価 か 分子 ぶんし 完全 かんぜん 描写 びょうしゃ 量子力学 りょうしりきがく 的 てき 手法 しゅほう 使 つか 分子 ぶんし 軌道 きどう 理論 りろん 結果 けっか 生 しょう 例 たと 六 ろく 化 か 硫黄 いおう LCAO (原子 げんし 軌道 きどう 線形 せんけい 結合 けつごう 硫黄 いおう 軌道 きどう 硫黄 いおう 軌道 きどう フッ素 ふっそ 軌道 きどう 基底 きてい 関数 かんすう 系 けい 取 と 合計 ごうけい 個 こ 分子 ぶんし 軌道 きどう 得 え 最低 さいてい 完全 かんぜん 占有 せんゆう 結合 けつごう 性 せい 中間 ちゅうかん 的 てき 完全 かんぜん 占有 せんゆう 非 ひ 結合 けつごう 性 せい 最 もっと 高 たか 持 も 空 そら 反 はん 結合 けつごう 性 せい 個 こ 価 あたい 電子 でんし 全 すべ 占 し 軌道 きどう 得 え フッ素 ふっそ 電気 でんき 的 てき 陰性 いんせい 配 はい 位 い 原子 げんし 含 ふく X 6 分子 ぶんし 安定 あんてい 配置 はいち 6 が形成 けいせい 説明 せつめい 結合 けつごう 非 ひ 結合 けつごう 性 せい g )は6つ全 すべ フッ素 ふっそ 原子 げんし 上 じょう 等 ひと 局在 きょくざい 化 か
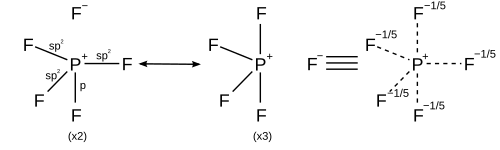
配 はい 位 い 子 こ 中心 ちゅうしん 超 ちょう 原子 げんし 価 か 原子 げんし 電気 でんき 的 てき 陰性 いんせい 超 ちょう 原子 げんし 価 か 化合 かごう 物 ぶつ 共鳴 きょうめい 構造 こうぞう 共有 きょうゆう 電子 でんし 対 たい 結合 けつごう 使 つか 描 えが 則 そく 従 したが 結合 けつごう 得 え 例 たと 五 ご 化 か 5 )では、5つの共鳴 きょうめい 構造 こうぞう 共有 きょうゆう 結合 けつごう 結合 けつごう 結合 けつごう 性 せい 重 おも 置 お 使 つか 生成 せいせい 則 そく 満 み 観測 かんそく 三角 さんかく 両 りょう 錐 きり 分子 ぶんし 構造 こうぞう 位 い 位 い 結合 けつごう 長 ちょう 長 なが 事実 じじつ 説明 せつめい [9]
五 ご 化 か 位 い 結合 けつごう 持 も 共鳴 きょうめい 構造 こうぞう 位 い 結合 けつごう 持 も 共鳴 きょうめい 構造 こうぞう 存在 そんざい 六 ろく 化 か 硫黄 いおう 配 はい 位 い 分子 ぶんし 結合 けつごう 同 おな 結合 けつごう 長 ちょう 上述 じょうじゅつ 合理 ごうり 化 か 適応 てきおう 性 せい 硫黄 いおう フッ素 ふっそ 結合 けつごう 等 ひと 分布 ぶんぷ 共有 きょうゆう 結合 けつごう 結合 けつごう 持 も 共鳴 きょうめい 構造 こうぞう 生成 せいせい
六 ろく 化 か 硫黄 いおう 隣合 となりあ cis )位置 いち 結合 けつごう 持 も 共鳴 きょうめい 構造 こうぞう 反対 はんたい 側 がわ trans )の位置 いち 結合 けつごう 持 も 共鳴 きょうめい 構造 こうぞう 存在 そんざい スピン結合 けつごう 原子 げんし 価 か 結合 けつごう 理論 りろん ジアゾメタン に適用 てきよう 得 え 軌道 きどう 解析 かいせき 中心 ちゅうしん 窒素 ちっそ 共有 きょうゆう 構造 こうぞう 持 も 化学 かがく 構造 こうぞう 観点 かんてん 解釈 かいしゃく
ジアゾメタンの化学 かがく 構造 こうぞう 式 しき 超 ちょう 原子 げんし 価 か 窒素 ちっそ 示 しめ この結果 けっか 著者 ちょしゃ 以下 いか 興味深 きょうみぶか 結論 けつろん 至 いた [10]
我々 われわれ 皆 みな 学部 がくぶ 生 せい 時 とき 教 おそ 反 はん 窒素 ちっそ 原子 げんし 実際 じっさい 共有 きょうゆう 結合 けつごう 形成 けいせい 軌道 きどう 状態 じょうたい 何 なん 関係 かんけい
^ M. Fugel, L. A. Malaspina, R. Pal, S. P. Thomas, M. W. Shi, M. A. Spackman, K. Sugimoto and S. Grabowsky (2019). “Revisiting a Historycal Concept by Using Quantum Crystallography: Are Phosphate, Sulfate and Perchlorate Anions Hypervalent?”. Chem. Eur. J. 25 : 6523-6532. doi :10.1002/chem.201806247 . ^ a b Musher, J. I. (1969). “The Chemistry of Hypervalent Molecules”. Angew. Chem. Int. Ed. Engl. 8 : 54-68. doi :10.1002/anie.196900541 . doi :10.1002/anie.196901311 )
^ a b c d Jensen, W. (2006). “The Origin of the Term "Hypervalent"”. J. Chem. Ed. 83 (12): 1751. Bibcode : 2006JChEd..83.1751J . doi :10.1021/ed083p1751 . Link
^ Kin-ya Akiba. Chemistry of Hypervalent Compounds . New York: Wiley VCH. ISBN 0-471-24019-2 ^ a b Magnusson, E. (1990). “Hypercoordinate molecules of second-row elements: d functions or d orbitals?”. J. Am. Chem. Soc. 112 : 7940–7951. doi :10.1021/ja00178a014 .
^ Gillespie, R. J.; Silvi, B. The octet rule and hypervalence: two misunderstood concepts. Coord. Chem. Rev. 2002 , 233-234 , 53-62. doi :10.1016/S0010-8545(02)00102-9
^ Predicting the Stability of Hypervalent Molecules Mitchell, Tracy A.; Finocchio, Debbie; Kua, Jeremy. J. Chem. Educ. 2007 , 84, 629. Link ^ Durrant, M. C. (2015). “A quantitative definition of hypervalency”. Chemical Science 6 : 6614–6623. doi :10.1039/C5SC02076J . ^ Curnow, Owen J. (1998). “A Simple Qualitative Molecular-Orbital/Valence-Bond Description of the Bonding in Main Group "Hypervalent" Molecules”. Journal of Chemical Education 75 (7): 910–915. Bibcode : 1998JChEd..75..910C . doi :10.1021/ed075p910 . ^ Gerratt, Joe (1997). “Modern valence bond theory”. Chemical Society Reviews 26 (2): 87–100. doi :10.1039/CS9972600087 .