维基百科 ひゃっか 自由 じゆう 的 てき 百科 ひゃっか 全 ぜん
托 たく 品 ひん 是 ぜ 一 いち 莨 たばこ 生物 せいぶつ 通常 つうじょう 情 じょう 状 じょう 用作 ようさく 合成 ごうせい 阿 おもね 托 たく 品 ひん 硫酸 りゅうさん 中 ちゅう 有 ゆう 机 つくえ 合成 ごうせい 史上 しじょう 一 いち 提 ひさげ 的 てき 一 いち 生物 せいぶつ 分子 ぶんし [ 1] [ 2]
用 よう 托 たく 品 ひん 存在 そんざい 下 か 与 あずか 碳酸二 に 甲 かぶと 反 はん 生成 せいせい 2-甲 きのえ 基 もと 托 たく 品 ひん ,然 しか 后 きさき 使 し 在 ざい 雷 かみなり 尼 あま 存在 そんざい 下 か 加 か 生成 せいせい 甲 きのえ 基 はじめ 芽 め 子 こ 最 さい 后 きさき 将 はた 甲 きのえ 基 はじめ 芽 め 子 こ 苯甲酰氯 在 ざい 吡啶 存在 そんざい 下 か 酯化反 はん ,就可以得到 いた 可 か
托 たく 品 ひん 早 はや 的 てき 全 ぜん 合成 ごうせい 是 ぜ 由 ゆかり 里 さと 夏 なつ 德 いさお 施 ほどこせ 泰 たい 特 とく 在 ざい 年 ねん 完成 かんせい 的 てき
维尔施 ほどこせ 泰 たい 特 とく 合成 ごうせい 法 ほう 合成 ごうせい 托 たく 品 ひん
里 さと 夏 なつ 德 いさお 施 ほどこせ 泰 たい 特 とく 年 ねん 诺贝尔化学 がく 得 とく 主 ぬし 环庚酮 作 さく 始原 しげん 料 りょう 尽 つき 管 かん 路 ろ 每 ごと 但 ただし 由 よし 多 た 使 つかい 率 りつ 大 だい 大 だい 降 くだ 低 てい 只 ただ 有 ゆう [ 3] 当然 とうぜん 在 ざい 世 せい 能 のう 人工 じんこう 合成 ごうせい 出 で 的 てき 化合 かごう 物 ぶつ 已 やめ 机 つくえ 合成 ごうせい 化学 かがく 的 てき 早期 そうき 在 ざい 室 しつ 装 そう 配 はい 天然 てんねん 的 てき 重要 じゅうよう 事件 じけん 之 の 一 いち 是 ぜ 有 ゆう 机 つくえ 合成 ごうせい 在 ざい 的 てき 着 ぎ 多 た 步 ふ 全 ぜん 合成 ごうせい 的 てき
在 ざい 合成 ごうせい 托 たく 品 ひん 前 まえ 施 ほどこせ 泰 たい 特 とく 在 ざい 年 ねん 已 やめ 成功 せいこう 品 ひん 原料 げんりょう 首 しゅ 次 じ 成功 せいこう 地 ち 合成 ごうせい 了 りょう 可 か 了 りょう 可 か 的 てき [ 4]
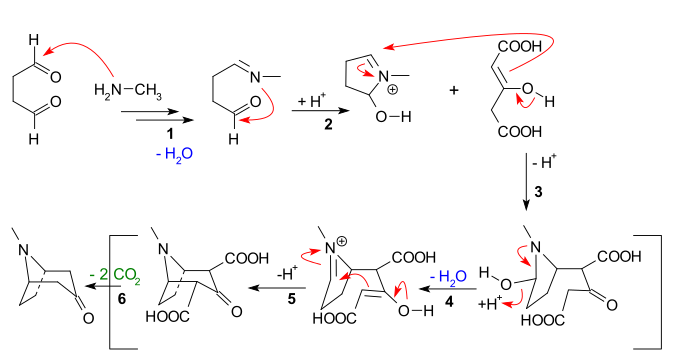
1917年 ねん 罗伯特 とく 创造了 りょう 的 てき 托 たく 品 ひん 合成 ごうせい 法 ほう 是 ぜ 有 ゆう 机 つくえ 合成 ごうせい 中 ちゅう 的 てき 路 ろ 一 いち 的 てき 丁 ひのと 二 に 甲 きのえ 和 わ 3-氧代戊 つちのえ 二 に 酸 さん 为原料 りょう 在 ざい 条件下 じょうけんか 利用 りよう 曼尼希 まれ 反 はん ,仅通过三 さん 步 ほ 反 はん 一 いち 合成 ごうせい 了 りょう 托 たく 品 ひん 可 か [ 5]
托 たく 品 ひん 合成 ごうせい
该反应的机 つくえ 理 り
一 いち 胺 对醛 的 てき 亲核加 か 成 なり ,而后失 しつ 水 すい 生成 せいせい 亚胺 ;亚胺分子 ぶんし 内 ない 的 てき 加 か 成 なり 出 で 第 だい 一 いち
烯醇负离子 こ 与 あずか 丙 へい 曼尼希 まれ 反 はん ;失 しつ 水 すい 生成 せいせい 分子 ぶんし 内 ない 希 まれ 反 はん 生成 せいせい 第 だい 二 に 脱去 だっきょ 生成 せいせい 托 たく 品 ひん
Robinson合成 ごうせい 托 たく 品 ひん 机 つくえ 理 り
最近 さいきん 采 さい 用 よう 的 てき 2-碘酰基 もと 酸 さん (IBX)试剂,利用 りよう 一 いち 反 はん 将 はた 醇 あつし 环庚醇 あつし )氧化成 かせい 同 どう 形成 けいせい α あるふぁ β べーた 不 ふ 一 いち 步 ほ 加入 かにゅう 甲 きのえ 可 か 直接 ちょくせつ 生成 せいせい 托 たく 品 ひん 似 に 物 ぶつ
在 ざい 生物 せいぶつ 体内 たいない 用 よう 建 けん 可 か 的 てき 托 たく 品 ひん 生物 せいぶつ 是 ぜ L -谷 たに 或 ある L -精 せい 料 りょう 合成 ごうせい 的 てき [ 6] 首 くび 先 さき 基 もと 酸 さん 先 さき 通 どおり 基 もと 的 てき 或 ある 脱 だつ 用 よう 生成 せいせい L -鸟氨酸 さん ,然 しか 后 きさき 酸 さん 脱 だつ 生成 せいせい 腐 くさ 接着 せっちゃく 腐 くさ 的 てき 一 いち 原子 げんし 被 ひ 甲 きのえ 基 はじめ 化 か 生成 せいせい N -甲 きのえ 基 はじめ 腐 くさ N -甲 きのえ 基 はじめ 腐 くさ 甲 きのえ 丁 ひのと 化 か 夫 おっと N -甲 きのえ 基 はじめ Δ でるた 1 -吡咯啉盐正 せい
此后,N -甲 きのえ 基 はじめ Δ でるた 1 -吡咯啉盐正 せい 与 あずか 乙 おつ 克 かつ 得 とく 到 いた 在 ざい 位 くらい 取 と 代 だい 的 てき 但 ただし 中 ちゅう 只 ただ 有 ゆう S )-异构体 たい 能 のう 生成 せいせい 莨 たばこ 的 てき 骨 ほね 架 か 得 とく 到 いた 丁 ひのと 二 に 酸 さん 的 てき 物 ぶつ [ 7] 后 きさき 者 しゃ 重 じゅう 新 しん 正 せい 生 せい 分子 ぶんし 内 ない 曼尼希 まれ 反 はん ),产生托 たく 品 ひん 位 い 被 ひ 基 もと 取 と 代 だい 的 てき 接着 せっちゃく 基 もと 被 ひ 水 みず 解 かい 生成 せいせい 再 さい 被 ひ 甲 きのえ 基 はじめ 化 か 作用 さよう 下 か 双 そう 得 とく 到 いた 甲 きのえ 基 はじめ 芽 め 子 こ 最 さい 后 きさき 甲 きのえ 基 はじめ 芽 め 子 こ 丙 へい 肉桂 にっけい 酸 さん 路 みち 生成 せいせい 的 てき [ 8] [ 9]
^ R. Robinson. A synthesis of tropinone. Journal of the Chemical Society , Transaction. 1917, 111 : 762–768. doi:10.1039/CT9171100762 ^ The Art and Science of Total Synthesis at the Dawn of the Twenty-First Century K. C. Nicolaou, Dionisios Vourloumis, Nicolas Winssinger, and Phil S. Baran Angew. Chem. Int. Ed. 2000 , 39, 44 ± 122
^ Smit, W. et al. (1998) Organic Synthesis, The Science behind the Art. Cambridge: The Royal Society of Chemistry.
^ Andrew J. Humphrey and David O'Hagan. Tropane alkaloid biosynthesis. A century old problem unresolved. Natural Products Reports 2001 , 18 , 494-502.doi :10.1039/b001713m
^ Arthur J. Birch. Investigating a Scientific Legend: The Tropinone Synthesis of Sir Robert Robinson, F.R.S. Notes and Records of the Royal Society of London , 1993 , 47 , 277-296.
^ Leete E, Marion L, Sspenser ID. Biogenesis of hyoscyamine. Nature. October 1954, 174 (4431): 650–1. PMID 13203600 ^ Dewick, P. M. Medicinal Natural Products. Chicester: Wiley-Blackwell. 2009. ISBN 978-0-4707-4276-1 ^ E. Leete, J. A. Bjorklund and S. H. Kim. The biosynthesis of the benzoyl moiety of cocaine . Phytochemistry. 1988, 27 : 2553. doi:10.1016/0031-9422(88)87026-2 ^ [Tropinone字典 じてん (英文 えいぶん . [2011-12-27 ] . (原始 げんし 内容 ないよう 存 そん 字典 じてん (英文 えいぶん ]