3C様 プロテアーゼ
| SARSコロナウイルスメインプロテアーゼ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| EC | 3.4.22.69 | ||||||||
| データベース | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB | RCSB PDB PDBj PDBe PDBsum | ||||||||
| |||||||||
| ペプチダーゼC30, コロナウイルスエンドペプチダーゼ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Peptidase_C30 | |||||||||
| Pfam | PF05409 | ||||||||
| InterPro | IPR008740 | ||||||||
| PROSITE | PS51442 | ||||||||
| MEROPS | C30 | ||||||||
| SCOP | d1q2wb1 | ||||||||
| SUPERFAMILY | d1q2wb1 | ||||||||
| |||||||||
3C
機能 [編集 ]
3C
このプロテアーゼは、コロナウイルスレプリカーゼポリタンパク
命名 法 [編集 ]
英語 版 :
Alternative names provided by the EC include 3CLpro, 3C-like protease, coronavirus 3C-like protease, Mpro, SARS 3C-like protease, SARS coronavirus 3CL protease, SARS coronavirus main peptidase, SARS coronavirus main protease, SARS-CoV 3CLpro enzyme, SARS-CoV main protease, SARS-CoV Mpro and severe acute respiratory syndrome coronavirus main protease.
治療 標的 として[編集 ]


プロテアーゼ3CLproは、ウイルスRNAから

-
SARS-CoV-2の3CLpro
阻害 剤 の設計 戦略 と、化学 構造 11aおよび11b。 -
3CLpro
阻害 剤 と化学 物質 11a -
3CLpro
阻害 剤 と化学 物質 11b
他 の3C(様 )プロテアーゼ[編集 ]
3C
- コロナウイルスは、3CLproを
持 っている。 - ピコルナウイルス
科 は、ピコルナウイルス3Cpro(EC 3.4.22.28; InterPro: IPR000199; MEROPS C03)を持 っている。これは、もっとも早 く研究 されたファミリーである。ポリオウイルスやライノウイルスに見 られるものがその例 である(どちらもエンテロウイルス属 のメンバー)。 - カリシウイルス
科 は、3CLpro(InterPro: IPR001665; MEROPS C37)を持 っている。例 としては、ノーウォークウイルスに見 られるものがある。
その
参照 項目 [編集 ]
- 3CLpro-1- 3C
様 プロテアーゼ阻害 剤 として作用 するルピントリビルに関 する抗 ウイルス薬 - カルモフール -
抗 悪性 腫瘍 薬 として用 いられるピリミジン系 アナログ - エブセレン-
抗 炎症 作用 、抗 酸化 作用 、細胞 保護 作用 を持 つ有機 セレン系 の合成 薬剤 分子 - GC376- ヒトおよび
動物 の治療 用 に開発 中 の広域 スペクトル抗 ウイルス薬 - ルピントリビル- 3Cおよび3C
様 プロテアーゼ阻害 剤 として作用 するペプチド模倣 型 の抗 ウイルス薬 - テアフラビンジガレート-
紅茶 に含 まれる抗 酸化 作用 のある天然 フェノールであるテアフラビン誘導体
脚注 [編集 ]
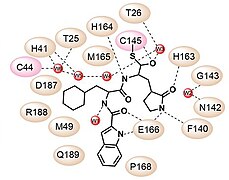
- ^ Goetz DH, Choe Y, Hansell E, Chen YT, McDowell M, Jonsson CB, Roush WR, McKerrow J, Craik CS (July 2007). “Substrate specificity profiling and identification of a new class of inhibitor for the major protease of the SARS coronavirus”. Biochemistry 46 (30): 8744–52. doi:10.1021/bi0621415. PMID 17605471.
- ^ a b Fan K, Wei P, Feng Q, Chen S, Huang C, Ma L, Lai B, Pei J, Liu Y, Chen J, Lai L (January 2004). “Biosynthesis, purification, and substrate specificity of severe acute respiratory syndrome coronavirus 3C-like proteinase”. The Journal of Biological Chemistry 279 (3): 1637–42. doi:10.1074/jbc.m310875200. PMC 7980035. PMID 14561748.
- ^ Akaji K, Konno H, Onozuka M, Makino A, Saito H, Nosaka K (November 2008). “Evaluation of peptide-aldehyde inhibitors using R188I mutant of SARS 3CL protease as a proteolysis-resistant mutant”. Bioorganic & Medicinal Chemistry 16 (21): 9400–8. doi:10.1016/j.bmc.2008.09.057. PMC 7126698. PMID 18845442.
- ^ Fehr AR, Perlman S (2015). “Coronaviruses: an overview of their replication and pathogenesis”. Coronaviruses. Methods in Molecular Biology. 1282. Springer. pp. 1–23. doi:10.1007/978-1-4939-2438-7_1. ISBN 978-1-4939-2438-7. PMC 4369385. PMID 25720466. "See section: Virion Structure."
- ^ Ryu, Young Bae; Park, Su-Jin; Kim, Young Min; Lee, Ju-Yeon; Seo, Woo Duck; Chang, Jong Sun; Park, Ki Hun; Rho, Mun-Chual et al. (2010-03-15). “SARS-CoV 3CLpro inhibitory effects of quinone-methide triterpenes from Tripterygium regelii” (
英語 ). Bioorganic & Medicinal Chemistry Letters 20 (6): 1873–1876. doi:10.1016/j.bmcl.2010.01.152. ISSN 0960-894X. PMC 7127101. PMID 20167482. - ^ Ocain TD, Rich DH (February 1992). “alpha-Keto amide inhibitors of aminopeptidases”. Journal of Medicinal Chemistry 35 (3): 451–6. doi:10.1021/jm00081a005. PMID 1738140.
- ^ Anand K, Ziebuhr J, Wadhwani P, Mesters JR, Hilgenfeld R (June 2003). “Coronavirus main proteinase (3CLpro) structure: basis for design of anti-SARS drugs”. Science 300 (5626): 1763–7. Bibcode: 2003Sci...300.1763A. doi:10.1126/science.1085658. PMID 12746549.
- ^ Pacifico S, Ferretti V, Albanese V, Fantinati A, Gallerani E, Nicoli F, Gavioli R, Zamberlan F, Preti D, Marastoni M (July 2019). “Synthesis and Biological Activity of Peptide
α -Ketoamide Derivatives as Proteasome Inhibitors”. ACS Medicinal Chemistry Letters 10 (7): 1086–1092. doi:10.1021/acsmedchemlett.9b00233. PMC 6627721. PMID 31312413. - ^ Kusov Y, Tan J, Alvarez E, Enjuanes L, Hilgenfeld R (October 2015). “A G-quadruplex-binding macrodomain within the "SARS-unique domain" is essential for the activity of the SARS-coronavirus replication-transcription complex”. Virology 484: 313–22. doi:10.1016/j.virol.2015.06.016. PMC 4567502. PMID 26149721.
- ^ Zhang L, Lin D, Kusov Y, Nian Y, Ma Q, Wang J, von Brunn A, Leyssen P, Lanko K, Neyts J, de Wilde A, Snijder EJ, Liu H, Hilgenfeld R (February 2020). “
α -Ketoamides as Broad-Spectrum Inhibitors of Coronavirus and Enterovirus Replication: Structure-Based Design, Synthesis, and Activity Assessment”. Journal of Medicinal Chemistry 63 (9): 4562–4578. doi:10.1021/acs.jmedchem.9b01828. PMC 7098070. PMID 32045235. - ^ Zhang L, Lin D, Sun X, Curth U, Drosten C, Sauerhering L, Becker S, Rox K, Hilgenfeld R (March 2020). “Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved
α -ketoamide inhibitors”. Science 368 (6489): 409–412. Bibcode: 2020Sci...368..409Z. doi:10.1126/science.abb3405. PMC 7164518. PMID 32198291. - ^ Morse JS, Lalonde T, Xu S, Liu WR (March 2020). “Learning from the Past: Possible Urgent Prevention and Treatment Options for Severe Acute Respiratory Infections Caused by 2019-nCoV”. ChemBioChem 21 (5): 730–738. doi:10.1002/cbic.202000047. PMC 7162020. PMID 32022370.
- ^ Liu C, Zhou Q, Li Y, Garner LV, Watkins SP, Carter LJ, Smoot J, Gregg AC, Daniels AD, Jervey S, Albaiu D (March 2020). “Research and Development on Therapeutic Agents and Vaccines for COVID-19 and Related Human Coronavirus Diseases”. ACS Central Science 6 (3): 315–331. doi:10.1021/acscentsci.0c00272. PMC 7094090. PMID 32226821.
- ^ Ramajayam R, Tan KP, Liang PH (October 2011). “Recent development of 3C and 3CL protease inhibitors for anti-coronavirus and anti-picornavirus drug discovery”. Biochemical Society Transactions 39 (5): 1371–5. doi:10.1042/BST0391371. PMID 21936817.
- ^ Dai, Wenhao; Zhang, Bing; Jiang, Xia-Ming; Su, Haixia; Li, Jian; Zhao, Yao; Xie, Xiong; Jin, Zhenming et al. (2020-06-19). “Structure-based design of antiviral drug candidates targeting the SARS-CoV-2 main protease” (
英語 ). Science 368 (6497): 1331–1335. doi:10.1126/science.abb4489. ISSN 0036-8075. PMC 7179937. PMID 32321856. - ^ Pfizer (2021-06-23). A PHASE 1B, 2-PART, DOUBLE-BLIND, PLACEBO-CONTROLLED, SPONSOR-OPEN STUDY, TO EVALUATE THE SAFETY, TOLERABILITY AND PHARMACOKINETICS OF SINGLE ASCENDING (24-HOUR, PART 1) AND MULTIPLE ASCENDING (120-HOUR, PART 2) INTRAVENOUS INFUSIONS OF PF-07304814 IN HOSPITALIZED PARTICIPANTS WITH COVID-19.
- ^ Bhardwaj VK, Singh R, Sharma J, Rajendran V, Purohit R, Kumar S (May 2020). “Identification of bioactive molecules from tea plant as SARS-CoV-2 main protease inhibitors”. Journal of Biomolecular Structure and Dynamics: 1–10. doi:10.1080/07391102.2020.1766572. PMC 7256349. PMID 32397940.
- ^ a b Bhardwaj VK, Singh R, Das P, Purohit R (January 2021). “Evaluation of acridinedione analogs as potential SARS-CoV-2 main protease inhibitors and their comparison with repurposed anti-viral drugs”. Computers in Biology and Medicine 128 (1104117): 104117. doi:10.1016/j.compbiomed.2020.104117. PMC 7659809. PMID 33217661.
- ^ Kim Y, Lovell S, Tiew KC, Mandadapu SR, Alliston KR, Battaile KP, Groutas WC, Chang KO (November 2012). “Broad-spectrum antivirals against 3C or 3C-like proteases of picornaviruses, noroviruses, and coronaviruses”. Journal of Virology 86 (21): 11754–62. doi:10.1128/JVI.01348-12. PMC 3486288. PMID 22915796.
- ^ Ziebuhr J, Bayer S, Cowley JA, Gorbalenya AE (January 2003). “The 3C-like proteinase of an invertebrate nidovirus links coronavirus and potyvirus homologs”. Journal of Virology 77 (2): 1415–26. doi:10.1128/jvi.77.2.1415-1426.2003. PMC 140795. PMID 12502857.
推薦 文献 [編集 ]
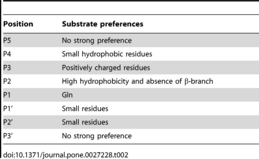
- Chuck CP, Chow HF, Wan DC, Wong KB (2 November 2011). “Profiling of substrate specificities of 3C-like proteases from group 1, 2a, 2b, and 3 coronaviruses”. PLOS ONE 6 (11): e27228. Bibcode: 2011PLoSO...627228C. doi:10.1371/journal.pone.0027228. PMC 3206940. PMID 22073294.
外部 リンク[編集 ]
- SARS coronavirus main proteinase - MeSH・アメリカ
国立 医学 図書館 ・生命 科学 用語 シソーラス(英語 ) - Peptidase C30/C16 in coronavirus, InterPro: IPR013016. The MEROPS C16 one is the "papain-like" PL-PRO.